Stent

Stent – implant medyczny stosowany do utrzymania światła poszerzanych naczyń krwionośnych lub narządów rurowych. Ma kształt walca i strukturę cienkiej siateczki, najczęściej zbudowaną ze stali nierdzewnej 316 LVM, stopu chromowo-kobaltowego albo włókien syntetycznych umieszczana wewnątrz naczynia krwionośnego lub narządu rurowego w celu przywrócenia jego drożności. Elastyczność zapewnia specjalna konstrukcja z falistymi połączeniami zygzakowatych drucików (ang. strut) stanowiących właściwe rusztowanie o waściwościach auksetycznych[1][2].
Rodzaje stentów[edytuj | edytuj kod]
Stent wieńcowy jest używany najczęściej w angioplastyce tętnic wieńcowych, podczas których stosuje się stent z gołego metalu (BMS), stent uwalniający lek (DES), stent wchłanialny, biodegradowalny (resorbowalny), stent do podwójnej terapii. Zastosowanie stentu było przełomem w kardiologii interwencyjnej choroby niedokrwiennej serca. Duży wkład w rozwój leczenia choroby wieńcowej z zastosowaniem stentów ma Julio Palmaz[3]. Obecnie w Polsce ponad 80% zabiegów angioplastyki wieńcowej przebiega z implantacją stentu aby zapobiec ich ponownemu zamknięciu po rozszerzeniu (PTCA) (dane Polskiego Towarzystwa Kardiologicznego). Zmiażdżycowane naczynie jest słabsze, a umieszczenie wewnątrz niego stentu (rusztowania) zabezpiecza przed „zapadnięciem się” osłabionych ścian[2].
Cewnik zakończony niewielkim balonem, na który nałożony jest stent, wprowadza się do tętnicy wieńcowej poprzez nakłucie tętnicy biodrowej, ramiennej lub promieniowej. Balonik ten, poza utrzymywaniem stentu, umożliwia jednocześnie udrożnienie tętnicy, zgniatając blaszkę miażdżycową zwężającą jej światło. Cały proces trwa około 30 minut. Zabieg wykonuje się w pracowni radiologicznej, monitorując na bieżąco położenie stentu w naczyniu wieńcowym. Gdy stent zostanie już wprowadzony do docelowego fragmentu tętnicy rozpręża się balon wprowadzając do niego płyn izotoniczny. Następnie usuwa się cewnik, pozostawiając sam stent.

Stenty naczyniowe są powszechnym sposobem leczenia zaawansowanej miażdżycy tętnic obwodowych i naczyń mózgowych. Stentowanie tętnic szyjnych i mózgowych jest metodą leczenia w ostrym niedokrwiennym udarze mózgu. Typowe miejsca leczone stentami naczyniowymi obejmują tętnice szyjną, biodrową i udową. Ze względu na zewnętrzną kompresję i siły mechaniczne działające w tych miejscach, elastyczne materiały stentów, takie jak nitinol, są stosowane w większości miejsc umieszczenia stentów obwodowych. W 1986 Jacques Puel w Tuluzie, Francja i Ulrich Sigwart w Lozannie, Szwajcaria równolegle zaczęli stosować jako pierwsi w świecie stenty do stabilizacji efektu endoplastyki balonowej w naczyniach obwodowych i wieńcowych[4][5].

Stentgraft (proteza naczyniowa) to rodzaj stentu naczyniowego z powłoką z tkaniny, która tworzy zamkniętą rurkę, ale jest rozszerzalna jak goły stent metalowy. Stenty pokryte są stosowane w zabiegach chirurgicznych wewnątrznaczyniowych, takich jak naprawa tętniaka. Stentgrafty z fenestracją są obecnie powszechnie stosowane w otwartych i wewnątrznaczyniowych zabiegach aortalnych w celu dostarczenia życiowym organom organizmu niezbędnego dopływu utlenionej krwi. Są również stosowane w leczeniu zwężeń w przeszczepach naczyniowych i przetokach stosowanych do hemodializy[2].
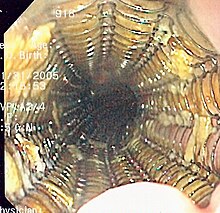
Stenty okrężnicy i stenty przełyku to paliatywne leczenie zaawansowanego raka okrężnicy i przełyku w celu utrzymania drożności tych organów.

Stent do drenażu dróg żółciowych i drenażu trzustki zapewniają drenaż trzustki i żółci z pęcherzyka żółciowego, trzustki i dróg żółciowych do dwunastnicy np. we wstępującym zapaleniu dróg żółciowych w niedrożności z powodu kamieni żółciowych.

Stent moczowodowy służy do zapewnienia drożności moczowodu, który może być zablokowany np. kamieniem nerkowym, lub guzem w procesie nowotworowym. Zapobiega uszkodzeniu zablokowanej nerki do czasu wykonania procedury usunięcia kamienia.
Stenty dróg oddechowych, stosowane w leczeniu zwężeń krtaniowo-tchawiczych, mogą być zrobione z silikonu lub metalu[6]. Dzielą się one na dwa typy: samorozprężalne stenty wewnątrzkrtaniowe/wewnątrztchawicze oraz stenty T w postaci rurki z zewnętrznym ramieniem. Te pierwsze powinny być zakładane jedynie w leczeniu krótkoterminowym lub paliatywnym ze względu na tendencję do migrowania i prowokowanie narastania ziarniny, co skutkuje złymi długoterminowymi efektami leczenia, utrudnia także dalsze leczenie chirurgiczne[7][8][9].
Etymologia i historia[edytuj | edytuj kod]
Pochodzenie słowa stent wywodzi się prawdopodobnie od nazwiska londyńskiego dentysty Charlesa Stenta, znanego ze swoich prac w dziedzinie ulepszania produkcji protez[1].
Pierwsze znane użycie słowa „stent” do opisania tego elementu miało miejsce w 1916, kiedy holenderski chirurg plastyczny opisał, w jaki sposób użył masy wyciskowej wynalezionej w 1856 przez Stenta jako matrycy, wokół której formowana była tkanka w procesie odbudowy strzaskanej twarzy[10].
Pierwsze (samorozprężające się) „stenty” wprowadził w praktyce medycznej w 1986 Ulrich Sigwart w Lozannie. Były początkowo nazywane „Wallstents” od nazwiska ich wynalazcy, Hansa Wallsténa[11].
Jako że stent jest ciałem obcym w naczyniu krwionośnym, po jakimś czasie wokół niego dochodzi do tworzenia neointimy – tkanki nowo tworzonej w wyniku drażnienia ściany naczynia przez ciało obce. Narastająca tkanka stopniowo zawęża światło naczynia (tak zwana restenoza), aż wreszcie doprowadza do całkowitego jego zamknięcia. Aby temu zapobiec, wprowadzono do leczenia stenty uwalniające substancje antyproliferacyjne, które zmniejszały ryzyko ponownego zamknięcia naczynia. Stenty te nazywane są stentami uwalniającymi leki – DES (Drug Eluting Stent). Stosowanymi substancjami antyproliferacyjnymi są ewerolimus (EES) i paklitaksel (PES). Obecność substancji antyproliferacyjnej ma jednak również niekorzystne działanie, gdyż utrudnia epitelializację, przez co sprzyja późnej zakrzepicy w stencie. Objawy zmusiły ośrodki badawcze do dalszych prac, w wyniku których powstały tzw. stenty podwójnej terapii (ang. dual therapy stent).
W 2006 po raz pierwszy zaprezentowano stenty uwalniające leki, które ulegając jednak stopniowemu wchłanianiu (ADES, Absorable Drug Eluting Stent), mają nie mieć wspomnianych niekorzystnych działań. Na kongresie Amerykańskiego Towarzystwa Kardiologicznego w Nowym Orleanie w marcu 2007 przedstawiono wyniki badania ABSORB[12][13] oceniające wyniki kliniczne terapii z użyciem wchłanialnych stentów uwalniających ewerolimus. Szkielet stentu był wykonany z polimeru na bazie kwasu mlekowego. Stwierdzono, że wchłanialne stenty uwalniające ewerolimus odznaczają się najlepszą skutecznością i bezpieczeństwem stosowania[14]. W innym badaniu stwierdzono jednak, że w przypadku takich stentów obserwuje się częstsze występowanie zakrzepów[15]. W analizie opublikowanej przez Cochrane Library stwierdzono, że stenty uwalniające leki powodują mniej poważnych powikłań niż stenty zwykłe[16][17][18].
W 2011 firma Abbott otrzymała zezwolenie na używanie w Stanach Zjednoczonych stentów („Absorb”) wchłanianych przez organizm po tym, jak produkt dostał oznaczenie CE w grudniu 2010[19]. W 2017 firma Abbott wycofała swoje wchłanialne stenty z rynku z powodu powikłań wymagających dalszych badań laboratoryjnych i klinicznych[20].
Zobacz też[edytuj | edytuj kod]
Przypisy[edytuj | edytuj kod]
- ↑ a b Ariel Roguin: Stent: The Man and Word Behind the Coronary Metal Prosthesis. Circulation, 2011, 4, 2, 206-209. www.ahajournals.org. [dostęp 2022-02-01].
- ↑ a b c Stenty - charakterystyka, rodzaje i możliwe powikłania.. www.medonet.pl. [dostęp 2022-02-01].
- ↑ Schatz RA, Palmaz JC, Tio FO, Garcia F, Garcia O, Reuter SR. Balloon-expandable intracoronary stents in the adult dog. Circulation. 1987; 76: 450–457. scholars.uthscsa.edu. [dostęp 2022-02-01].
- ↑ Sigwart U, Puel J, Mirkovitch V, Joffre F, Kappenberger L. Intravascular stents to prevent occlusion and restenosis after transluminal angioplasty. N Engl J Med. 1987; 316: 701–706.. www.nejm.org. [dostęp 2022-02-01].
- ↑ Jason H. Rogers and John R. Laird Overview of New Technologies for Lower Extremity Revascularization. Circulation, 2007, 116, 18, 2072-2085.. www.ahajournals.org. [dostęp 2022-01-31].
- ↑ Badr Eldin Mostafa, Chiraz Chaouch-Mberek, Ahmed El Halafawi, Jāmiʻat ʻAyn Shams: Tracheal Stenosis: diagnosis and treatment. Faculty of Medicine, Ain Shams University, 2012, s. 37. (ang.).
- ↑ Rosen i Simpson 2018 ↓, s. 41–47.
- ↑ Rosen i Simpson 2018 ↓, s. 205–214.
- ↑ Witold Szyfter, Małgorzata Wierzbicka, Tomasz Pastusiak, Małgorzata Leszczyńska. Leczenie zwężeń krtaniowo-tchawiczych. „Postępy w chirurgii głowy i szyi”. 2, s. 30–41, 2009.
- ↑ M E Ring. How a dentist's name became a synonym for a life-saving device: the story of Dr. Charles Stent. Journal of the History of Dentistry 2001, 49 (2): 77-80.. read.qxmd.com. [dostęp 2022-02-01].
- ↑ Hans Wallstén, inventor of the stent. www.invivomagazine.com. [dostęp 2022-02-01].
- ↑ Pokaz slajdów z prezentacji badania na Kongresie AHA.
- ↑ Pdf przedstawiający wstępne wyniki badania. acc07.acc.org. [zarchiwizowane z tego adresu (2007-09-27)]..
- ↑ Ankur Kalra, Hasan Rehman, Sahil Khera et al. New-Generation Coronary Stents: Current Data and Future Directions. „Curr Atheroscler Rep”. 19, 20 February 2017. DOI: 10.1007/s11883-017-0654-1. [dostęp 2017-03-14]. (ang.).
- ↑ Wykrzykowska JJ, Kraak RP, Hofma SH et al. Bioresorbable Scaffolds versus Metallic Stents in Routine PCI. „N Engl J Med.”, 2017 Mar 29. DOI: 10.1056/NEJMoa1614954. [dostęp 2017-04-13]. (ang.).
- ↑ Joshua Feinberg i inni, Drug-eluting stents versus bare-metal stents for acute coronary syndrome, „The Cochrane Library”, 2017, DOI: 10.1002/14651858.CD012481.pub2.
- ↑ WINDECKER S, REMONDINO A, EBERLI FR et al.: Sirolimus- or paclitaxel-eluting stents for coronary artery revascularisation. N. Engl. J. Med. (2005) 353:663-670. www.semanticscholar.org. [dostęp 2022-01-25].
- ↑ Adam Witkowski, Maksymilian P. Opolski, Dariusz Dudek et al.: Stanowisko grupy ekspertów dotyczące zastosowania stentów oraz balonów uwalniających leki antyproliferacyjne u pacjentów z chorobą wieńcową przyjęte przez Asocjację Interwencji Sercowo−Naczyniowych i Polskie Towarzystwo Kardiologiczne. Kardiologia Polska2011; 69, supl. I: 1–36. silo.tips. [dostęp 2022-01-26].
- ↑ Abbott Gets Approval for Dissolvable Stent, www.foxnews.com.
- ↑ Abbott to restrict Absorb bioresorbable stent in Europe. www.drugdeliverybusiness.com. [dostęp 2022-01-23].
Bibliografia[edytuj | edytuj kod]
- Clark A. Rosen, C. Blake Simpson, Techniki chirurgiczne w laryngologii, Otwock: Medisfera, 2018, ISBN 978-83-63367-18-3.
