Alkohole aromatyczne
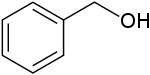
Alkohole aromatyczne – grupa organicznych związków chemicznych, alkoholi zbudowanych z układu aromatycznego i grupy hydroksyalkilowej, tj. grupy alkilowej z przyłączoną grupą hydroksylową, −OH. Różnią się tym od fenoli, że grupa −OH nie jest bezpośrednio połączona z pierścieniem. Najprostszym alkoholem aromatycznym jest fenylometanol (alkohol benzylowy).
Niektóre z nich w postaci wolnej lub w postaci estrów występują naturalnie w roślinach jako substancje zapachowe. Niektóre mają znaczenie w przemyśle perfumeryjnym[1][niewiarygodne źródło?][2].
Tak jak inne alkohole, dzielą się na I-rzędowe (np. alkohol benzylowy, PhCH
2OH), II-rzędowe (np. difenylometanol, Ph
2CHOH) i III-rzędowe (np. trifenylometanol, Ph
3COH).
- Proste alkohole aromatyczne
-
I-rzędowy: fenylometanol (alkohol benzylowy)
-
II-rzędowy: difenylometanol (benzhydrol)
-
III-rzędowy: trifenylometanol (alkohol trytylowy)
Podobnie jak alkohole alifatyczne, alkohole aromatyczne z metalami alkalicznymi tworzą alkoholany. Przykładem takiego związku jest fenylometanolan sodu, który można otrzymać w reakcji[2]:
- 2C
6H
5CH
2OH + 2Na → 2C
6H
5CH
2ONa + H
2↑
W przeciwieństwie do I-rzędowych alkoholi alifatycznych, I-rzędowe alkohole aromatyczne reagują na zimno z kwasem solnym dając odpowiednie chlorki, np[3].
- C
6H
5CH
2OH + HCl → C
6H
5CH
2Cl + H
2O
Otrzymywanie[edytuj | edytuj kod]
Przykładowe reakcje otrzymywania alkoholi aromatycznych[3]:
Reakcja Cannizzaro[edytuj | edytuj kod]
Reakcja Cannizzaro pozwala na otrzymywanie I-rzędowych alkoholi aromatycznych. W metodzie tej na aldehydy aromatyczne działa się stężonym roztworem zasady sodowej lub potasowej, np.
Wadą takiej syntezy jest fakt, że docelowy alkohol powstaje tylko z połowy użytego aldehydu, druga połowa utlenia się natomiast do kwasu (w tym przypadku benzoesowego). Problem ten można obejść stosując tzw. krzyżową reakcją Cannizzaro, tj. prowadząc reakcję w obecności niewielkiego nadmiaru formaldehydu, który będzie selektywnie utleniał się do kwasu mrówkowego, a aldehyd aromatyczny w całości ulegnie redukcji do alkoholu. Przykładem może być reakcja aldehydu p-toluilowego z wodorotlenkiem potasu i formaldehydem prowadząca do alkoholu p-metylobenzylowego i mrówczanu potasu:
- CH
3C
6H
4CHO + HCHO + KOH → CH
3C
6H
4CH
2OH + HCOOK
Redukcja ketonów[edytuj | edytuj kod]
Drugorzędowe alkohole aromatyczne można otrzymać przez redukcję odpowiednich ketonów aromatycznych, np. za pomocą pyłu cynkowego i NaOH jako źródła wodoru in statu nascendi, np.
- (C
6H
5)
2CO + 2[H] → (C
6H
5)
2CHOH
Ze związków Grignarda[edytuj | edytuj kod]
Do syntezy III-rzędowych alkoholi aromatycznych można wykorzystać reakcję aromatycznych związków Grignarda z estrami aromatycznymi. W pierwszym etapie powstaje III-rzędowy alkoholan, który poddaje się hydrolizie do alkoholu, np.
- 2C
6H
5MgBr + C
6H
5COOC
2H
5 → (C
6H
5)
3COMgBr + MgBrOC
2H
5 - (C
6H
5)
3COMgBr + H
2O → (C
6H
5)
3COH + MgBrOH
Przypisy[edytuj | edytuj kod]
- ↑ Alkohole nienasycone i aromatyczne [online] [dostęp 2013-08-22] [zarchiwizowane z adresu 2014-03-24].
- ↑ a b Ilustrowana encyklopedia dla wszystkich. Chemia, Warszawa: Wydawnictwa Naukowo-Techniczne, 1990, s. 9.
- ↑ a b Arthur I. Vogel, Preparatyka organiczna, Warszawa: Wydawnictwa Naukowo-Techniczne, 1964, s. 826.