Odczynnik Dessa-Martina
| |||||||||||||||||||
 Model cząsteczki uwidaczniający budowę pseudooktaedryczną z centralnym atomem jodu | |||||||||||||||||||
| |||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||
| Wzór sumaryczny |
C13H13IO8 | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
424,14 g/mol | ||||||||||||||||||
| Wygląd |
białe kryształy[3] | ||||||||||||||||||
| Identyfikacja | |||||||||||||||||||
| Numer CAS | |||||||||||||||||||
| PubChem | |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||
Odczynnik Dessa-Martina, DMP – organiczny związek chemiczny z grupy związków jodoorganicznych typu hiperwalencyjnego[4]. Nazwa zwyczajowa pochodzi od nazwisk dwóch amerykańskich chemików, Daniela Benjamina Dessa i Jamesa Cullena Martina, którzy otrzymali go w 1983 roku[3].
Budowa[edytuj | edytuj kod]
Cząsteczka DMP zawiera resztę kwasu 2-jodoksybenzoesowego związaną z trzema resztami octanowymi w potrójny układ bezwodnikowy. Obecność grup octanowych umożliwia rozpuszczanie związku w rozpuszczalnikach organicznych, podczas gdy wyjściowy kwas jest praktycznie nierozpuszczalny[1].
Cząsteczka ma budowę pseudooktaedryczną Ψ-Oc[1][4]. Jej struktura została ustalona rentgenograficznie w roku 2012. Cztery bezwodnikowe atomy tlenu leżą w płaszczyźnie wokół centralnego atomu jodu, a wierzchołki oktaedru zajmuje atom węgla pierścienia benzenowego i wolna para elektronowa, która w krysztale skoordynowana jest z karbonylowym atomem tlenu sąsiedniej cząsteczki, tworząc wiązanie halogenowe[4].
Otrzymywanie[edytuj | edytuj kod]
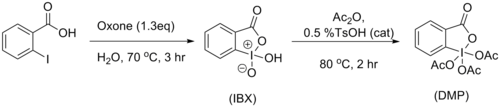
Związek można otrzymać z kwasu 2-jodobenzoesowego. W pierwszym etapie utlenia się go do cyklicznego kwasu 2-jodoksybenzoesowego za pomocą nadtlenosiarczanu potasu, KHSO
5 (soli monopotasowej kwasu Caro, tzw. oksonu). Uzyskany związek poddaje się acetylowaniu[4]. Reakcję prowadzi się np. mieszając kilkanaście godzin gęstą zawiesinę substratu w mieszaninie bezwodnika octowego i kwasu octowego. Szybkość procesu zależy od stopnia rozdrobnienia kwasu 2-jodoksybenzoesowego; można ją zwiększyć przez ogrzewanie[1]. Reakcja przebiega znacząco szybciej, gdy prowadzi się ją z użyciem samego bezwodnika octowego w obecności katalitycznej ilości TsOH[6]:
Po stwierdzeniu za pomocą spektroskopii NMR, że acetylowanie zaszło całkowicie, rozpuszczalniki usuwa się pod zmniejszonym ciśnieniem[1] lub poprzez odsączenie produktu i przemycie go eterem[6]. Produkt otrzymuje się zazwyczaj w postaci drobnokrystalicznej. W celu otrzymania większych kryształów roztwór związku odparowuje się powoli w ciągu kilku dni w strumieniu azotu[4].
Zastosowanie[edytuj | edytuj kod]
Służy m.in. do utleniania alkoholi – pierwszorzędowych do aldehydów, drugorzędowych do ketonów[1][7]:
W porównaniu do tradycyjnych utleniaczy (np. dichromianu potasu) cechuje się krótszymi czasami reakcji, większą wydajnością i łagodniejszymi warunkami reakcji (temperatura pokojowa, pH neutralne)[7].
Uwagi[edytuj | edytuj kod]
Przypisy[edytuj | edytuj kod]
- ↑ a b c d e f g h Daniel B. Dess, J.C. Martin, A useful 12-I-5 triacetoxyperiodinane (the Dess-Martin periodinane) for the selective oxidation of primary or secondary alcohols and a variety of related 12-I-5 species, „Journal of the American Chemical Society”, 113 (19), 1991, s. 7277–7287, DOI: 10.1021/ja00019a027 (ang.).
- ↑ Henri A. Favre, Warren H. Powell, Nomenklatura związków organicznych. Rekomendacje IUPAC i nazwy preferowane 2013, Komisja Terminologii Chemicznej Polskiego Towarzystwa Chemicznego (tłum.), wyd. 5, Narodowy Komitet Międzynarodowej Unii Chemii Czystej i Stosowanej, [2023], s. 125, 535.
- ↑ a b c D.B. Dess, J.C. Martin, Readily accessible 12-I-5 oxidant for the conversion of primary and secondary alcohols to aldehydes and ketones, „Journal of Organic Chemistry”, 48 (22), 1983, s. 4155–4156, DOI: 10.1021/jo00170a070 (ang.).
- ↑ a b c d e f Albert Schröckeneder i inni, The crystal structure of the Dess–Martin periodinane, „Beilstein Journal of Organic Chemistry”, 8 (1), 2012, s. 1523–1527, DOI: 10.3762/bjoc.8.172 (ang.).
- ↑ Kenneth W. Henderson, William J. Kerr, Jennifer H. Moir, Magnesium amide base-mediated enantioselective deprotonation processes, „Tetrahedron”, 58 (23), 2002, s. 4573–4587, DOI: 10.1016/s0040-4020(02)00364-2 (ang.).
- ↑ a b Robert E. Ireland, Longbin Liu, An improved procedure for the preparation of the Dess-Martin periodinane, „Journal of Organic Chemistry”, 58 (10), 1993, s. 2899–2899, DOI: 10.1021/jo00062a040 (ang.).
- ↑ a b John McMurry, Chemia organiczna, t. 3, Warszawa: Wydawnictwo Naukowe PWN, 2017, ISBN 978-83-01-19455-0, OCLC 1005176465.