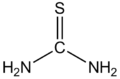
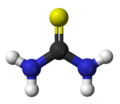
Tiomocznik
| |||||||||||||||||||||||||
 próbka związku | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||
| Wzór sumaryczny |
CH4N2S | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
(H2N)2C=S | ||||||||||||||||||||||||
| Masa molowa |
76,12 g/mol | ||||||||||||||||||||||||
| Wygląd |
białe krystaliczne ciało stałe[1] | ||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||
Tiomocznik (tiokarbamid, amid kwasu tiokarbaminowego) – organiczny związek chemiczny, będący siarkowym analogiem mocznika (zawiera atom siarki zamiast atomu tlenu).
Otrzymywanie[edytuj | edytuj kod]
Tiomocznik można otrzymać przez ogrzewanie tiocyjanianu amonu (rodanku amonu, NH4SCN):
Zastosowanie[edytuj | edytuj kod]
Stosowany w przemyśle farmaceutycznym w syntezie leków (witamina B1), do produkcji barwników, tworzyw sztucznych. W analizie chemicznej służy do wykrywania jonów bizmutu i telluru(IV). Jest antyhormonem tyroksyny.
Przypisy[edytuj | edytuj kod]
- ↑ PTCL Safety web site: Safety data for thiourea. [dostęp 2008-09-16]. (ang.).
- ↑ a b Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4.
- ↑ a b c d Małgorzata Galus: Tablice chemiczne. Warszawa: Wydawnictwo Adamantan, 2008. ISBN 978-83-7350-105-8.
Kontrola autorytatywna (rodzaj indywiduum chemicznego):