Sybutramina
| |||||||||||||||
| |||||||||||||||
| Ogólne informacje | |||||||||||||||
| Wzór sumaryczny |
C17H26ClN | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
279,8 g/mol | ||||||||||||||
| Identyfikacja | |||||||||||||||
| Numer CAS | |||||||||||||||
| PubChem | |||||||||||||||
| DrugBank | |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||
| Klasyfikacja medyczna | |||||||||||||||
| ATC | |||||||||||||||
| |||||||||||||||
| |||||||||||||||
Sybutramina, sibutramina – organiczny związek chemiczny stosowany jako lek anorektyczny (hamujący łaknienie) w leczeniu otyłości (obesitas). Mechanizm działania polega na hamowaniu wychwytu zwrotnego noradrenaliny, serotoniny i dopaminy.
Farmakokinetyka[edytuj | edytuj kod]
W przeważającym stopniu lek wywiera efekt poprzez swoje metabolity. Sybutramina oraz jej metabolity nie wykazują działania cholinolitycznego, przeciwhistaminowego; charakteryzuje się małym powinowactwem do receptorów serotoninowych, adrenergicznych, dopaminowych, benzodiazepinowych i kwasu glutaminowego.
Nie hamuje MAO. Podana doustnie wchłania się szybko, równoczesne spożywanie posiłku zwalnia wchłanianie. Podlega efektowi pierwszego przejścia przez wątrobę, jest metabolizowana w obecności izoenzymu cytochromu P-450 (3A4) do czynnych farmakologicznie metabolitów (demetylowe pochodne M-1 i M-2), które są inaktywowane w wyniku hydroksylacji i koniugacji do nieaktywnych M-5 i M-6. Czas po którym sybutramina osiąga maksymalne stężenie we krwi (tmax) wynosi 1,2 h, tmax czynnych metabolitów – 3 h.
Z białkami surowicy sybutramina wiąże się w 97%, metabolity M-1 i M-2 w 94%. Stężenie stacjonarne metabolitów jest osiągane w ciągu 4 dni stosowania leku i jest w przybliżeniu 2 razy większe niż po podaniu pojedynczej dawki. t½ metabolitów wynosi odpowiednio 14 i 16 h i nie ulega zmianie podczas dłuższego stosowania. Lek jest wydalany głównie z moczem w postaci nieczynnych metabolitów.
Działania niepożądane[edytuj | edytuj kod]
Stosowanie sybutraminy powoduje wzrost ryzyka wystąpienia zawałów serca oraz udarów, zwłaszcza u osób ze schorzeniami układu krążenia[3].
Do innych działań niepożądanych sybutraminy należą: wzrost ciśnienia tętniczego krwi[4], przyśpieszone bicie serca, bezsenność, niepokój, wahania nastroju, u osób z zaburzeniami psychicznymi mogą wystąpić myśli samobójcze, obniżenie progu drgawkowego i wzrost ryzyka wystąpienia napadów padaczkowych, uderzenia gorąca, potliwość, nudności, biegunki, zaburzenia widzenia, parestezje, uczucie suchości w ustach, ryzyko uzależnienia od sybutraminy[5].
Przeciwwskazania[edytuj | edytuj kod]
Przyjmowanie preparatów zawierających sybutraminę bez konsultacji z lekarzem, może prowadzić do powikłań stanowiących istotne zagrożenie dla zdrowia i życia. Stosowanie sybutraminy jest przeciwwskazane w następujących sytuacjach:
- zaburzenia psychiczne, w tym zaburzenia depresyjne, choroba afektywna dwubiegunowa, zaburzenia psychotyczne, w tym schizofrenia, zaburzenia jedzenia
- nadciśnienie tętnicze
- nadciśnienie płucne
- choroby serca, w tym choroba niedokrwienna serca, stan po zawale serca, niedomykalność zastawek serca
- choroby tętnic obwodowych
- stan po udarze mózgu lub przemijających atakach niedokrwiennych mózgu
- u osób powyżej 65 roku życia
- padaczka
- nadczynność tarczycy
- guz chromochłonny
- jaskra z zamkniętym kątem przesączania
- retencja moczu związana z przerostem prostaty
- nadwrażliwością na sybutraminę
Interakcje[edytuj | edytuj kod]
Sybutramina może powodować poważne, zagrażające życiu interakcje z różnymi lekami, w tym lekami przeciwdepresyjnymi takimi jak inhibitory monoaminooksydazy, selektywne blokery wychwytu zwrotnego serotoniny, czy też blokery wychwytu zwrotnego serotoniny i noradrenaliny.
Historia i dostępność na rynku[edytuj | edytuj kod]
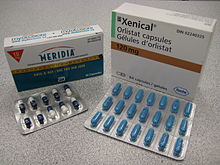
Dostępna w postaci chlorowodorku sybutraminy, została wprowadzona do lecznictwa w 1997 roku – wypierając powoli starsze leki anorektyczne, które wykazują wiele działań niepożądanych (np. mazindol – Mazindol, Teronac, deksfenfluraminę – Isolipan, chlorowodorek chlorfenterminy – Avipron, fenterminę – Adipex).
21 stycznia 2010 roku Komitet ds. Produktów Leczniczych u Ludzi (Comittee for Medicinal Products for Human Use) działający w ramach Europejskiej Agencji Leków (EMA) zalecił zawieszenie pozwolenia na dopuszczenie do obrotu na rynkach Unii Europejskiej wszystkich preparatów zawierających sybutraminę. Było to związane z wynikami badania SCOUT (Sibutramine Cardiovascular OUTcomes), które wykazało wzrost z 10,0% do 11,4% ryzyka wystąpienia zawału mięśnia serca nie skutkującego zgonem, udaru mózgu nie skutkującego zgonem, zatrzymania czynności serca z pozytywnie zakończoną resuscytacją lub zgonu z przyczyn sercowo-naczyniowych, u pacjentów powyżej 54. roku życia obciążonych chorobą układu krążenia lub cukrzycą typu 2 przyjmujących sybutraminę w porównaniu z placebo[6][7][8]. Wzrost ryzyka związany był głównie ze zwiększeniem częstości zawału serca lub udaru mózgu, które nie skutkowały zgonem[7]. Osobom stosującym lek zalecono zgłoszenie się do lekarza[6].
Preparaty zawierające chlorowodorek sybutraminy, które były dostępne w Polsce:
- leki oryginalne:
- Meridia 10, Meridia 15 – kaps. 0,01 g, 0,015 g
- leki generyczne:
- Zelixa – tabl.powl. 0,01 g, 0,015 g
- Lindaxa 10, Lindaxa 15 – kaps. 0,01 g, 0,015 g
- Afibron – kaps. 0,01 g, 0,015 g
- Reduce – kaps. 0,015 g
- dostępne jako suplementy diety, rozprowadzane nielegalnie:
- Meizitang – 0,030 g
- Lida – 0,030 g
Po wycofaniu z oficjalnego rynku sybutramina jest jednym z najczęściej wykrywanych nielegalnych dodatków do „naturalnych” suplementów diety wspomagających chudnięcie[9].
Przypisy[edytuj | edytuj kod]
- ↑ a b c Sibutramine, [w:] DrugBank, University of Alberta, DB01105 [dostęp 2023-08-31] (ang.).
- ↑ Sibutramine hydrochloride monohydrate, karta charakterystyki produktu Sigma-Aldrich, Merck, 26 kwietnia 2022, numer katalogowy: S9944 [dostęp 2023-08-31]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ David E. Arterburn, Paul K. Crane, David L. Veenstra, The efficacy and safety of sibutramine for weight loss: a systematic review, „Archives of Internal Medicine”, 164 (9), 2004, s. 994–1003, DOI: 10.1001/archinte.164.9.994, PMID: 15136309 (ang.).
- ↑ K. Johansson i inni, Long-term changes in blood pressure following orlistat and sibutramine treatment: a meta-analysis, „Obesity Reviews: An Official Journal of the International Association for the Study of Obesity”, 11 (11), 2010, s. 777–791, DOI: 10.1111/j.1467-789X.2009.00693.x, PMID: 20025693 (ang.).
- ↑ M. Florentin, E.N. Liberopoulos, M.S. Elisaf, Sibutramine-associated adverse effects: a practical guide for its safe use, „Obesity Reviews: An Official Journal of the International Association for the Study of Obesity”, 9 (4), 2008, s. 378–387, DOI: 10.1111/j.1467-789X.2007.00425.x, PMID: 18034790 (ang.).
- ↑ a b European Medicines Agency recommends suspension of marketing authorisations for sibutramine, London: European Medicines Agency, 21 stycznia 2010, EMA/39408/2010 [dostęp 2010-02-15] [zarchiwizowane z adresu 2010-04-01] (ang.).
- ↑ a b Bezpośredni komunikat skierowany do pracowników ochrony zdrowia dotyczący zawieszenia pozwoleń na dopuszczenie do obrotu sibutraminy ze względu na wzrost ryzyka powikłań sercowo-naczyniowych zaobserwowanych w badaniu SCOUT, Warszawa: Abbott Laboratories Poland, 27 stycznia 2010 [zarchiwizowane z adresu 2010-10-09].
- ↑ Christian Torp-Pedersen i inni, Cardiovascular responses to weight management and sibutramine in high-risk subjects: an analysis from the SCOUT trial, „European Heart Journal”, 28 (23), 2007, s. 2915–2923, DOI: 10.1093/eurheartj/ehm217 (ang.).
- ↑ Ronnie Cohen, No Wonder It Works So Well: There May Be Viagra In That Herbal Supplement, [w:] NPR [online] [dostęp 2018-10-14] (ang.).

