Kwasy karboksylowe
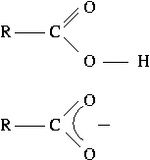
Kwasy karboksylowe – grupa organicznych związków chemicznych zawierająca grupę karboksylową.
Atom wodoru w grupie karboksylowej może się łatwo odszczepiać w formie jonu wodorowego, co zgodnie z teorią Arrheniusa nadaje tym związkom charakter kwasowy:
- RCOOH + H
2O ⇄ RCOO−
+ H
3O+
Kwasy karboksylowe tworzą chętnie wiązania wodorowe z grupą aminową, hydroksylową i innymi.
Kwasy karboksylowe z krótkimi grupami alkilowymi są dobrze rozpuszczającymi się w wodzie cieczami o ostrym, nieprzyjemnym zapachu i toksycznych właściwościach. Wraz ze wzrostem długości grupy alkilowej wzrasta temperatura topnienia tych kwasów (prawidłowość tę widać dla kwasów wyższych niż kwas heksanowy[1]). Kwasy karboksylowe zawierające poniżej 10 atomów węgla są cieczami w temperaturze pokojowej, a zawierające 10 lub więcej atomów węgla, ciałami stałymi. Kwasy monokarboksylowe zawierające 4–28 atomów węgla o prostym łańcuchu noszą nazwę kwasów tłuszczowych (czasem pojęcie kwasów tłuszczowych rozszerza się na wszystkie alifatyczne niecykliczne kwasy karboksylowe)[2].
Otrzymywanie[edytuj | edytuj kod]
Kwasy karboksylowe otrzymuje się zwykle w reakcjach utleniania odpowiednich alkoholi lub aldehydów:

Dogodnymi metodami otrzymywania kwasów karboksylowych są również hydroliza nitryli i dekarboksylacja kwasów dikarboksylowych.
Charakterystyczne reakcje[edytuj | edytuj kod]
Kwasy karboksylowe ulegają takim samym reakcjom jak zwykłe kwasy nieorganiczne. Tworzą one sole z zasadami nieorganicznymi i organicznymi. Reagują również z alkoholami tworząc estry. Estry kwasów tłuszczowych z gliceryną nazywane są tłuszczami.
Tworzenie chlorków kwasowych[edytuj | edytuj kod]
W wyniku reakcji z trichlorkiem fosforu (PCl3) lub chlorkiem tionylu (SOCl2) przechodzą w chlorki kwasowe:

Odwadnianie[edytuj | edytuj kod]
Inną charakterystyczną reakcją dla kwasów karboksylowych jest reakcja odwadniania, w wyniku której powstaje bezwodnik kwasowy:

Redukcja do alkoholi[edytuj | edytuj kod]
Pod wpływem tetrahydroglinianu litu kwasy karboksylowe redukują się do odpowiednich alkoholi. W pierwszym etapie tej reakcji tworzy się kompleksowa sól kwasu karboksylowego:

W dalszych etapach następują kolejne przeniesienia anionów wodorkowych od glinu do atomu węgla grupy karboksylowej, przy czym anion karboksylanowy redukuje się najpierw do aldehydu, a następnie do alkoholanu:

Otrzymany alkoholan poddaje się następnie hydrolizie w celu wydzielenia wolnego alkoholu:

Ważniejsze kwasy karboksylowe[edytuj | edytuj kod]
Kwasy monokarboksylowe[edytuj | edytuj kod]
- kwas mrówkowy
- kwas octowy
- kwas propionowy
- kwas masłowy
- kwas walerianowy
- kwas pelargonowy CH3(CH2)7COOH.
Aromatyczne z innymi grupami funkcyjnymi, np. hydroksykwasy
Kwasy dikarboksylowe[edytuj | edytuj kod]
Aromatyczne
Z innymi grupami funkcyjnymi
Inne kwasy karboksylowe[edytuj | edytuj kod]
Trikarboksylowe z innymi grupami funkcyjnymi
Zobacz też[edytuj | edytuj kod]
Przypisy[edytuj | edytuj kod]
- ↑ Robert T. Morrison, Robert N. Boyd: Chemia organiczna. T. 1. Warszawa: PWN, 1985, s. 668. ISBN 83-01-04166-8.
- ↑ Fatty acids, [w:] A.D. McNaught, A. Wilkinson, Compendium of Chemical Terminology (Gold Book), S.J. Chalk (akt.), International Union of Pure and Applied Chemistry, wyd. 2, Oxford: Blackwell Scientific Publications, 1997, DOI: 10.1351/goldbook.F02330, ISBN 0-9678550-9-8 (ang.).
