Powłoka elektronowa: Różnice pomiędzy wersjami
| [wersja przejrzana] | [wersja przejrzana] |
Nie podano opisu zmian |
Nie podano opisu zmian |
||
| Linia 2: | Linia 2: | ||
[[Plik:Electron shell 056 Barium.svg|thumb|Powłoki elektronowe atomu [[bar (pierwiastek)|baru]]]] |
[[Plik:Electron shell 056 Barium.svg|thumb|Powłoki elektronowe atomu [[bar (pierwiastek)|baru]]]] |
||
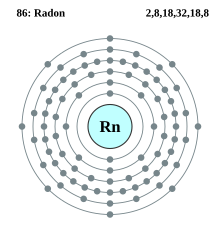
[[Plik:Electron shell 086 Radon.svg|thumb|Powłoki elektronowe atomu [[radon]]u, [[liczba atomowa]] – 86]] |
[[Plik:Electron shell 086 Radon.svg|thumb|Powłoki elektronowe atomu [[radon]]u, [[liczba atomowa]] – 86]] |
||
'''Powłoka elektronowa''' – zbiór [[stan kwantowy|stanów kwantowych]] o tej samej wartości [[główna liczba kwantowa|głównej |
'''Powłoka elektronowa''' – zbiór [[stan kwantowy|stanów kwantowych]] o tej samej wartości [[główna liczba kwantowa|głównej liczby kwantowej]]. |
||
W [[chemia|chemii]] za powłokę elektronową wokół danego [[atom]]u uważa się zbiór [[orbital atomowy|orbitali atomowych]] mających tę samą główną liczbę kwantową ''n''. Kolejnym wartościom ''n'' przypisane są kolejne powłoki: K, L, M, N, O, P i Q. Powłoki składają się z różnej liczby podpowłok elektronowych, odpowiadających określonym rodzajom orbitali atomowych: |
W [[chemia|chemii]] za powłokę elektronową wokół danego [[atom]]u uważa się zbiór [[orbital atomowy|orbitali atomowych]] mających tę samą główną liczbę kwantową ''n''. Kolejnym wartościom ''n'' przypisane są kolejne powłoki: K, L, M, N, O, P i Q. Powłoki składają się z różnej liczby podpowłok elektronowych, odpowiadających określonym rodzajom orbitali atomowych: |
||
| Linia 63: | Linia 63: | ||
* i (''l'' = 6): 26 elektronów |
* i (''l'' = 6): 26 elektronów |
||
Wbrew informacjom podawanym przez niektóre źródła, nie wszystkie [[Helowce|gazy szlachetne]] mają całkowicie zapełnione powłoki elektronowe. Np. [[argon]] ma w powłoce M zapełnione podpowłoki s i p, nie ma natomiast elektronów d. Maksymalnie zapełniona powłoka elektronowa nie musi być energetycznie korzystna – pierwsze odstępstwo od tej zasady obserwuje się dla atomu [[potas]]u, w którym ostatni elektron wchodzi na podpowłokę 4s, a nie 3d. Jest tak dlatego, że przy dużych liczbach atomowych wzrasta rola oddziaływania spin-orbita w porównaniu z oddziaływaniami elektrostatycznymi{{r|Hermann}}. |
Wbrew informacjom podawanym przez niektóre źródła, nie wszystkie [[Helowce|gazy szlachetne]] mają całkowicie zapełnione powłoki elektronowe. Np. [[argon]] ma w powłoce M zapełnione podpowłoki s i p, nie ma natomiast elektronów d. Maksymalnie zapełniona powłoka elektronowa nie musi być energetycznie korzystna – pierwsze odstępstwo od tej zasady obserwuje się dla atomu [[potas]]u, w którym ostatni elektron wchodzi na podpowłokę 4s, a nie 3d. Jest tak dlatego, że przy dużych liczbach atomowych wzrasta rola oddziaływania spin-orbita w porównaniu z [[oddziaływanie elektrostatyczne|oddziaływaniami elektrostatycznymi]]{{r|Hermann}}. |
||
== Zobacz też == |
== Zobacz też == |
||
Wersja z 13:42, 17 lip 2015


Powłoka elektronowa – zbiór stanów kwantowych o tej samej wartości głównej liczby kwantowej.
W chemii za powłokę elektronową wokół danego atomu uważa się zbiór orbitali atomowych mających tę samą główną liczbę kwantową n. Kolejnym wartościom n przypisane są kolejne powłoki: K, L, M, N, O, P i Q. Powłoki składają się z różnej liczby podpowłok elektronowych, odpowiadających określonym rodzajom orbitali atomowych:
- K – jeden orbital s – może pomieścić maksymalnie 2 elektrony
- L – jeden s i 3 orbitale p – może pomieścić maksymalnie 8 elektronów
- M – jeden s, 3 p i 5 d – może pomieścić maksymalne 18 elektronów
- N – jeden s, 3 p, 5 d i 7 f – może pomieścić maksymalne 32 elektrony
- itd.
| Symbol powłoki | główna liczba kwantowa n |
2n2 (maksymalna liczba elektronów) |
podpowłoki |
|---|---|---|---|
| K | 1 | 2 | s |
| L | 2 | 8 | s, p |
| M | 3 | 18 | s, p, d |
| N | 4 | 32 | s, p, d, f |
| O | 5 | 50 | s, p, d, f, g |
| P | 6 | 72 | s, p, d, f, g, h |
| Q | 7 | 98 | s, p, d, f, g, h, i |
Maksymalna liczba elektronów na podpowłokach (zgodnie ze wzorem n = 4l + 2, gdzie l to poboczna liczba kwantowa):
- s (l = 0): 2 elektrony
- p (l = 1): 6 elektronów
- d (l = 2): 10 elektronów
- f (l = 3): 14 elektronów
- g (l = 4): 18 elektronów
- h (l = 5): 22 elektrony
- i (l = 6): 26 elektronów
Wbrew informacjom podawanym przez niektóre źródła, nie wszystkie gazy szlachetne mają całkowicie zapełnione powłoki elektronowe. Np. argon ma w powłoce M zapełnione podpowłoki s i p, nie ma natomiast elektronów d. Maksymalnie zapełniona powłoka elektronowa nie musi być energetycznie korzystna – pierwsze odstępstwo od tej zasady obserwuje się dla atomu potasu, w którym ostatni elektron wchodzi na podpowłokę 4s, a nie 3d. Jest tak dlatego, że przy dużych liczbach atomowych wzrasta rola oddziaływania spin-orbita w porównaniu z oddziaływaniami elektrostatycznymi[1].
Zobacz też
Przypisy
Bibliografia
- Adam Bielański: Chemia ogólna i nieorganiczna. Warszawa: Państwowe Wydaw. Naukowe, 1981, s. 81–89. ISBN 83-01-02626-X.
- ↑ Błąd w przypisach: Błąd w składni elementu
<ref>. Brak tekstu w przypisie o nazwieHermannBŁĄD PRZYPISÓW
