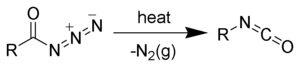Przegrupowanie Curtiusa
Przegrupowanie Curtiusa (Reakcja Curtiusa lub Degradacja Curtiusa), po raz pierwszy zdefiniowana przez Theodora Curtiusa, jest to reakcja chemiczna, w której azydki acylowe ulegają przegrupowaniu do izocyjanianów[1][2][3].
Izocyjaniany mogą zostać wyłapane przez różne nukleofile. Często dodaje się wody w celu zhydrolizowania izocyjanianu do aminy[4].
Reakcja ta w obecności tert-butanolu generuje grupę blokującą aminy - Boc - szeroko stosowaną w syntezie organicznej. W reakcji tej tworzy się uretan 5[5][6].
Azydki takie 3 można łatwo otrzymać z kwasów karboksylowych 1 przy użyciu azydku difenylofosforylu 2[7][8][9].
Mechanizm reakcji[edytuj | edytuj kod]
Pierwszym etapem przegrupowania Curtiusa jest odłączenie cząsteczki azotu w postaci gazowej z utworzeniem acylowego nitrenu 2. Jednocześnie, utworzony nitren przegrupowuje się od razu do odpowiedniego izocyjanianu (3) przez migrację grupy alkilowej R na atom azotu.
Zastosowanie[edytuj | edytuj kod]
W odmianie zwanej degradacja Darapsky'ego przegrupowanie Curtiusa zachodzi na etapie przejścia z α-cyjanoestru do aminokwasu[10][11][12].
Zobacz też[edytuj | edytuj kod]
Przypisy[edytuj | edytuj kod]
- ↑ Theodor Curtius. Ueber Stickstoffwasserstoffsäure (Azoimid) N3H. „Berichte der deutschen chemischen Gesellschaft”. 23, s. 3023 - 3033, 1890. DOI: 10.1002/cber.189002302232. (niem.).
- ↑ Theodor Curtius. Hydrazide und Azide organischer Säuren I. Abhandlung. „Journal für Praktische Chemie”. 50, s. 275 - 294, 1894. DOI: 10.1002/prac.18940500125. (niem.).
- ↑ Eric F. V. Scriven, Kenneth Turnbull. Azides: their preparation and synthetic uses. „Chemical Reviews”. 88, s. 297–368, 1988. DOI: 10.1021/cr00084a001. (ang.).
- ↑ Carl Kaiser, Joseph Weinstock. AMINES FROM MIXED CARBOXYLIC-CARBONIC ANHYDRIDES: 1-PHENYLCYCLOPENTYLAMINE. „Organic Syntheses”. Coll. Vol. 6, s. 910, 1988. (ang.).
- ↑ Hélène Lebel and Olivier Leogane. Boc-Protected Amines via a Mild and Efficient One-Pot Curtius Rearrangement. „Organic Letters”. 7, s. 4107–4110, 2005. DOI: 10.1021/ol051428b. ISSN 1523-7052. (ang.).
- ↑ David J. am Ende, Keith M. DeVries, Pamela J. Clifford, and Steven J. Brenek. A Calorimetric Investigation To Safely Scale-Up a Curtius Rearrangement of Acryloyl Azide. „Org. Process Res. Dev.”. 2, s. 382–392, 1998. DOI: 10.1021/op970115w. (ang.).
- ↑ Takayuki Shioiri, Shun-ichi Yamada. DIPHENYL PHOSPHORAZIDATE. „Organic Syntheses”. Coll. Vol. 7, s. 206, 1990.
- ↑ T. Shioiri, K. Ninomiya, S. Yamada. Diphenylphosphoryl azide. New convenient reagent for a modified Curtius reaction and for peptide synthesis. „J. Am. Chem. Soc.”. 94, s. 6203–6205, 1972. DOI: 10.1021/ja00772a052. (ang.).
- ↑ K. Ninomiya, T. Shioiri, S. Yamada. Phosphorus in organic synthesis—VII: Diphenyl phosphorazidate (DPPA). A new convenient reagent for a modified curtius reaction. „Tetrahedron”. 30, s. 2151-2157, 1974. DOI: 10.1016/S0040-4020(01)97352-1.
- ↑ August Darapsky. Darstellung von alpha-Aminosäuren aus Alkyl-cyanessigsäuren. „Journal für Praktische Chemie”. 146, s. 250-267, 1936. DOI: 10.1002/prac.19361460806. (niem.).
- ↑ August Darapsky. Über Hydrazinosäuren. „Journal für Praktische Chemie”. 146, s. 219 - 249, 1936. DOI: 10.1002/prac.19361460805. (niem.).
- ↑ chempensoftware.com - Ce site est en vente! - Portail d'informations [online], www.chempensoftware.com [dostęp 2017-11-26] [zarchiwizowane z adresu 2008-05-02].
Bibliografia[edytuj | edytuj kod]
- John McMurry: Chemia Organiczna. T. 4. Warszawa: Wydawnictwo Naukowe PWN, 2003, s. 956-959. ISBN 83-01-14103-4.
- Louis F. Fieser: Advanced Organic Chemistry. New York: Reinhold Publishing Corporation, Chapman & Hall, Ltd., London, 1962, s. 501-502, seria: Library of Congress Catalog Card Number: 61-14594.
- Jonathan Clayden, Nick Greeves, Stauart Warren, Peter Wothers: Organic Chemistry. New York: OXFORD University Press Inc., 2007, s. 1073. ISBN 978-0-19-850346-0.