Nerwiakowłókniakowatość typu 2
| neurofibromatosis | |
| Klasyfikacje | |
| ICD-10 | |
|---|---|
Nerwiakowłókniakowatość typu 2 (zespół MISME, ang. neurofibromatosis, type II, NF2, bilateral acoustic neurofibromatosis, BANF, MISME syndrome, multiple inherited schwannomas, meningiomas, and ependymomas) – choroba genetyczna o dziedziczeniu autosomalnym dominującym, przypominająca obrazem klinicznym nerwiakowłókniakowatość typu 1. NF2 spowodowana jest mutacjami w genie NF2 w locus 22q12.2 kodującym neurofibrominę-2, zwaną także merliną.
Historia[edytuj | edytuj kod]
Pierwsze doniesienia o nietypowych przypadkach choroby Recklinghausena pojawiły się w latach 20. i 30. XX wieku. W 1933 Gardner i Frazie opisali pięciopokoleniową rodzinę, w której 38 członków miało utratę słuchu z powodu obustronnych nerwiaków, a 15 z nich dodatkowo straciło wzrok[1]. Inne rodziny opisali Worster-Drought i wsp. w 1937[2], Feiling i Ward w 1920[3], Moyes w 1968[4]. Forster-Drought przypomniał w 1937 roku doniesienie Wisharta z 1822 roku, będące prawdopodobnie pierwszym opisem NF2[5]. Opisany pacjent, Michael Blair, zgłosił się do Wisharta, wówczas prezydenta Królewskiego Towarzystwa Chirurgicznego w Edynburgu, z obustronną głuchotą. Od urodzenia miał niezwykły kształt czaszki i wykrytą około 4. miesiąca życia utratę wzroku w prawym oku. W autopsji stwierdzono guzy opony twardej mózgu i „guz wielkości małego orzecha, bardzo twardy, przyczepiony do obu [nerwów przedsionkowych] w miejscu ich wejścia do przewodu słuchowego wewnętrznego”.
W 1986 Seizinger ustalił locus genu na 22 chromosomie[6], Wertelecki i wsp. uściślili locus na 22q11[7]. Dwa typy choroby: Gardnera i Wisharta, wyróżnił Evans w 1992 roku.
Etiologia[edytuj | edytuj kod]
Choroba spowodowana jest mutacjami w genie NF2 w locus 22q12.2 kodującym białko merlinę. Gen NF2 ma mniejszą długość niż NF1; składa się z 16 konstytutywnych i jednego alternatywnie wycinanego eksonu. Alternatywny splicing owocuje przynajmniej dwiema formami białka o odmiennej ekspresji tkankowej. Funkcja białka polega na pośredniczeniu w interakcjach między środowiskiem zewnętrznym komórki a cytoszkieletem.
Objawy i przebieg[edytuj | edytuj kod]
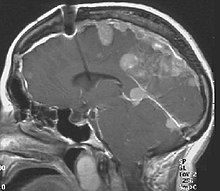



W obrazie klinicznym NF2 można wyróżnić trzy grupy objawów, obejmujące:
- zmiany nowotworowe
- zmiany skórne
- zmiany oczne.
- Guzy nowotworowe
- jednostronne (6%) i obustronne (85%)[8] schwannomata nerwu przedsionkowego (VS). Schwannoma mogą też wychodzić z innych nerwów czaszkowych, częste są schwannoma nerwu okoruchowego i trójdzielnego (29% pacjentów, zazwyczaj obustronnie; rzadko wymaga leczenia chirurgicznego);
- meningioma mózgowia
- meningioma rdzenia przedłużonego
- gwiaździaki
- wyściółczaki (2,5%)[8]. Glejaki włosowatokomoórkowe (gąbczaki) i wyściółczaki zwykle są zlokalizowane w pniu mózgu i górnym odcinku szyjnym rdzenia kręgowego; często współwystępują z jamistością rdzenia lub opuszki. Niekiedy uciskają rdzeń.
Glejaki nerwu wzrokowego nie występują częściej u pacjentów z NF2, w przeciwieństwie do NF1[9].
- Neuropatia obwodowa (3%[8]-10-15%[10]), będąca najprawdopodobniej powikłaniem uciskających nerw mnogich guzków przylegających nerwów obwodowych;
- Obwodowe schwannomata pojedyncze (68%), liczne (10%)[8]
- Plamy cafe au lait (40%[10]) – wyjątkowo jest ich kilka, są mniejsze niż w NF1, nigdy nie występują zmiany barwnikowe w okolicy dołu pachowego.
- Zmiany oczne
- zaćma (81%)[8]
- hamartomata i zmiany barwnikowe siatkówki (ang. combined pigment epithelial and retinal hamartoma, CEPRH – 9%)[8]
- oponiak osłonek nerwu wzrokowego (ang. optic nerve sheath meningioma, ONSM; częstość nieznana; w grupie pacjentów z ONSM NF2 rozpoznano u 2-8%[11].
Obraz kliniczny NF2 jest odmienny u dzieci i u dorosłych. U pacjentów pediatrycznych najczęściej rozpoznaje się zaćmę (60-80%), schwannoma nerwu przedsionkowego (43%), oponiaki i guzy rdzenia (31%), schwannomata skóry (8%), opadanie stopy spowodowane obwodową neuropatią (3%) i mononeuropatię twarzową (19%).
Klinicznie wyróżniono podtypy choroby:
- postać umiarkowaną (typ Gardnera) z początkiem około 25. roku życia, dominującymi objawami spowodowanymi VS i słabo wyrażonymi objawami skórnymi, oraz
- postać ciężką (typ Wisharta) z początkiem przed 25. rokiem życia i VS tylko u połowy chorych; zwykle przebiega szybko i wiąże się z wczesnym zgonem.
Rozpoznanie[edytuj | edytuj kod]
Opracowano kryteria rozpoznania NF2 (NIH Consensus)[12][13]. Pacjent może mieć postawione kliniczne rozpoznanie NF2, jeśli spełnia następujące kryteria:
- Obustronne schwannoma nerwu przedsionkowego potwierdzone histopatologicznie lub widoczne w MRI ze wzmocnieniem kontrastowym, lub
- Krewny I° z rozpoznaniem NF2 i
- Jednostronny guz schwannoma nerwu przedsionkowego lub
- Meningioma albo glioma albo schwannoma albo podtorebkowe zmętnienie soczewki albo zwapnienia śródmózgowe lub
- Jednostronny schwannoma nerwu przedsionkowego i przynajmniej dwa z wymienionych:
- meningioma
- glioma
- schwannoma
- podtorebkowe zmętnienie soczewki
- zwapnienia śródmózgowe, lub
- Dwa lub więcej meningioma, i przynajmniej jedno z wymienionych:
- glioma
- schwannoma
- podtorebkowe zmętnienie soczewki
- zwapnienia śródmózgowe.
Leczenie i opieka nad pacjentami[edytuj | edytuj kod]
Pacjenci z rozpoznaną NF2 powinni być objęci specjalistyczną opieką lekarską w referencyjnych ośrodkach. Panel badań oferowanych tym pacjentom powinien obejmować:
- ocenę dermatologiczną z dokumentacją zmian
- ukierunkowane badanie okulistyczne
- pełną ocenę neurologiczną
- badanie laryngologiczne z obiektywną oceną słuchu
- MRI mózgowia i rdzenia ze wzmocnieniem kontrastowym.
Badania powinny być powtarzane co roku i częściej w przypadku nowych dolegliwości.
Weryfikacja rozpoznania możliwa jest przy użyciu technik molekularnych wykrywających mutacje w genie NF2.
Subkliniczne zmiany oczne pojawiają się stosunkowo wcześnie, stąd niektóre ośrodki zalecają podjęcie monitorowania okulistycznego już około 10. roku życia.
Klasyfikacja ICD10[edytuj | edytuj kod]
| kod ICD10 | nazwa choroby |
|---|---|
| ICD-10: D33 | Niezłośliwy nowotwór mózgu i innych części centralnego systemu nerwowego |
| ICD-10: D33.0 | Mózg, nadnamiotowe |
| ICD-10: D33.1 | Mózg, podnamiotowe |
| ICD-10: D33.2 | Mózg, nieokreślony |
| ICD-10: D33.3 | Nerwy czaszkowe |
| ICD-10: D33.4 | Rdzeń kręgowy |
| ICD-10: D33.7 | Inne określone części centralnego systemu nerwowego |
| ICD-10: D33.9 | Centralny system nerwowy, nieokreślony |
Przypisy[edytuj | edytuj kod]
- ↑ Gardner WJ, Frazier CH. Hereditary bilateral acoustic tumors. „J Hered”. 22, s. 7-8, 1933.
- ↑ Worster-Drought C, Dickson WEC, McMenemey WH. Multiple meningeal and perineural tumors with analogous changes in the glia and ependyma (neurofibroblastomatosis). „Brain”. 60, s. 85-117, 1937.
- ↑ Feiling A, Ward E. A familial form of acoustic tumour. „Brit Med J”. 1, s. 496-497, 1920.
- ↑ Moyes PD. Familial bilateral acoustic neuroma affecting 14 members from four generations. „J Neurosurg”. 29, s. 78-82, 1968. PMID: 5674095.
- ↑ Wishart JH. Case of tumours in the skull, dura mater, and brain. „Edinburgh Med Surg J”. 18, s. 393-397, 1822.
- ↑ Seizinger BR, Rouleau G, Ozelius LJ, Lane AH, St George-Hyslop P, Huson S, Gusella JF, Martuza RL. Common pathogenetic mechanism for three tumor types in bilateral acoustic neurofibromatosis. „Science”. 236, s. 317-319, 1987. PMID: 3105060.
- ↑ Wertelecki W, Rouleau GA, Superneau DW, Forehand LW, Williams JP, Haines JL, Gusella JF. Neurofibromatosis 2: clinical and DNA linkage studies of a large kindred. „New England Journal of Medicine”. 319, s. 278-283, 1988. PMID: 3134615.
- ↑ a b c d e f Phakomatoses. W: Huson SM, Korf B: Emery's and Rimoin's Principles and Practice of Medical Genetics. T. vol. III. Londyn: Churchill-Livingstone, 2002, s. 3162-3202. ISBN 0-443-06434-2.
- ↑ Evans DGR, Baser ME, O’Reilly B, et al. Management of the patient and family with neurofi bromatosis 2: a consensus conference statement. Br J Neurosurg 2005; 19: 5–12.
- ↑ a b Ferner RE. Neurofibromatosis 1 and neurofibromatosis 2: a twenty first century perspective. „Lancet Neurol”. 6. 4, s. 340-51, 2007. DOI: 10.1016/S1474-4422(07)70075-3. PMID: 17362838.
- ↑ Bosch MM, Wichmann WW, Boltshauser E, Landau K. Optic nerve sheath meningiomas in patients with neurofibromatosis type 2. „Arch Ophthalmol”. 124. 3, s. 379-85, 2006. PMID: 16534058.
- ↑ National Institutes of Health Consensus Development Conference Statement on Neurofibromatosis. „Arch Neurol”. 45, s. 575-579, 1987. PMID: 3128965.
- ↑ Evans DGR, Huson SM, Donnai D, Neary W, Blair V, Newton V, Strachan T, Harris R. A genetic study of type 2 neurofibromatosis in the United Kingdom. II. Guidelines for genetic counselling. „J Med Genet”. 29, s. 847-852, 1992. PMID: 1479599.
Bibliografia[edytuj | edytuj kod]
- Nerwiakowłókniakowatość typu 2 (NF2). W: Stanisław Zajączek: Nowotwory dziedziczne 2002. Profilaktyka, diagnostyka, leczenie. Jan Lubiński (red.). Poznań: Termedia Wydawnictwa Medyczne, 2002, s. 135-139. ISBN 83-916594-1-0.
- Susan Bayliss Mallory, Alanna Bree, Peggy Chern: Dermatologia pediatryczna. Diagnostyka i leczenie. Lublin: Wydawnictwo Czelej, 2007, s. 388. ISBN 978-83-60608-31-9.
- Ferner RE. Neurofibromatosis 1 and neurofibromatosis 2: a twenty first century perspective. „Lancet Neurol”. 6. 4, s. 340-51, 2007. DOI: 10.1016/S1474-4422(07)70075-3. PMID: 17362838.
- McLaughlin ME, Pepin SM, Maccollin M, Choopong P, Lessell S. Ocular pathologic findings of neurofibromatosis type 2. „Arch Ophthalmol”. 125. 3, s. 389-94, 2007. PMID: 17353411.
- Baser ME, R Evans DG, Gutmann DH. Neurofibromatosis 2. „Curr Opin Neurol”. 16. 1, s. 27-33, 2003. PMID: 12544854.
- Evans DG, Sainio M, Baser ME. Neurofibromatosis type 2. „J Med Genet”. 37. 12, s. 897-904, 2000. PMID: 11106352.
- Desouza CE, Nagpal RD. Neurofibromatosis 2 (bilateral acoustic schwannomas). What is it? A review of literature and an update. „J Postgrad Med”. 38. 1, s. 27-31, 1992. PMID: 1512722.
Linki zewnętrzne[edytuj | edytuj kod]
- NEUROFIBROMATOSIS, TYPE II; NF2 w bazie Online Mendelian Inheritance in Man (ang.)
- D Gareth Evans: Neurofibromatosis 2. GeneReviews.
- Forum osób chorych na NF2
