Aromataza
Wygląd
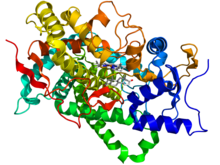
Aromataza (syntetaza estrogenowa, CYP19A1; EC 1.14.14.14) – enzym z klasy oksydoreduktaz[2], z rodziny cytochromu P450[3]. Katalizuje aromatyzację pierścienia A androgenów (testosteronu i androstendionu) i przekształcenie ich w estrogeny, odpowiednio w 17β-estradiol (E2) i estron (E1)[2][4][5][6].
Sumaryczny zapis katalizowanych reakcji[2]:
- testosteron + 3NADPH + 3H+
+ 3O
2 ⇄ 17β-estradiol + mrówczan + 4H
2O + 3NADP+ - androstendion + 3NADPH + 3H+
+ 3O
2 ⇄ estron + mrówczan + 4H
2O + 3NADP+
W obu przypadkach proces polega na zajściu trzech kolejnych hydroksylacji[2].

Ludzka aromataza zbudowana jest z 503 reszt aminokwasowych i hemu. Jest jedynym enzymem u kręgowców, który przekształca androgeny w estrogeny, a w związku z tym inhibitory aromatazy stanowią ważną grupę leków raka piersi zależnego od estrogenów[1].
Przypisy
[edytuj | edytuj kod]- ↑ a b Debashis Ghosh i inni, Structural basis for androgen specificity and oestrogen synthesis in human aromatase, „Nature”, 457 (7226), 2009, s. 219–223, DOI: 10.1038/nature07614, PMID: 19129847, PMCID: PMC2820300 [dostęp 2022-05-24] (ang.).
- ↑ a b c d EC 1.14.14.14 ExPASy Proteomics Server
- ↑ CYP19A1 cytochrome P450 family 19 subfamily A member 1 [ Homo sapiens (human) ] [online], National Library of Medicine [dostęp 2022-05-24] (ang.).
- ↑ Krzysztof Kula i inni, Znaczenie fizjologiczne estrogenów u mężczyzn - przełom w endokrynologii, „Endokrynologia Polska”, 53 (3), 2005, s. 314-321 [dostęp 2022-05-24].
- ↑ Robert Kincaid Murray, Daryl K. Granner, Victor W. Rodwell, Biochemia Harpera ilustrowana, wyd. VI uaktualnione, Warszawa: Wydawnictwo Lekarskie PZWL, 2008, s. 542–544, ISBN 978-83-200-3573-5.
- ↑ R.J. Santen i inni, History of aromatase: saga of an important biological mediator and therapeutic target, „Endocrine Reviews”, 30 (4), 2009, s. 343–375, DOI: 10.1210/er.2008-0016, PMID: 19389994 [dostęp 2022-05-24] (ang.).




