Konfiguracja D i L

Konfiguracja D i L (konfiguracja względna) – sposób określania i nazywania izomerów optycznych związków chemicznych poprzez analizę korelacyjną względem aldehydu glicerynowego.
Przed poznaniem struktury przestrzennej obu stereoizomerów aldehydu glicerynowego przyjęto, że ten który w projekcji Fischera ma grupę hydroksylową po lewej stronie oznaczany będzie literą „L” a ten z grupą OH po prawej literą „D”. Późniejsze badania potwierdziły, że przyjęte losowo z 50% prawdopodobieństwem założenie było trafione. Wprowadzenie tego pojęcia, jeszcze przed opracowaniem spektroskopowych metod określania konfiguracji bezwzględnej, miało na celu określanie konfiguracji innych związków przez korelację do odpowiedniego izomeru aldehydu glicerynowego przez reakcje chemiczne tego aldehydu z innymi związkami w taki sposób, aby nie dokonać rozerwania wiązań przy asymetrycznym atomie węgla.
Oznaczenie D lub L zapisuje się kapitalikiem i stawia, oddzielone dywizem (łącznikiem), przed nazwą związku. Rodzaj anomeru podaje się w nazwie przed nim – na przykład: α-D-glukoza.
Konfiguracja względna a skręcalność optyczna[edytuj | edytuj kod]
Początkowo przyjęto arbitralnie, że aldehyd glicerynowy skręcający płaszczyznę światła spolaryzowanego w prawo (aldehyd (+)-glicerynowy) to ten, który ma w cząsteczce grupę OH po prawej stronie w projekcji Fischera. Skręcalność optyczna nie jest jednak odpowiednikiem konfiguracji względnej, to znaczy różne związki o konfiguracji D mogą być „prawoskrętne” albo „lewoskrętne” (analogicznie izomery L).
Określanie konfiguracji D i L biocząsteczek[edytuj | edytuj kod]

Konwencja D i L jest obecnie ograniczona zazwyczaj do określania konfiguracji węglowodanów i α-aminokwasów. Istnieje także konwencja DP/LP określania konfiguracji P-chiralnych analogów nukleotydów[1].
Cukry[edytuj | edytuj kod]
Cząsteczki cukrów są najczęściej diastereoizomerami posiadającymi kilka asymetrycznych atomów węgla, a o ich konfiguracji względnej decyduje położenie grupy hydroksylowej na przedostatnim atomie węgla w łańcuchu. Określanie konfiguracji względnej formy łańcuchowej cukrów dokonuje się, przedstawiając cząsteczkę w projekcji Fischera. Cząsteczkę cukru należy ustawić tak aby grupa −CHO (u aldoz) lub ketonowa (u ketoz) znalazła się na górze, a −CH2OH na dole. Jeżeli −OH na przedostatnim atomie węgla w łańcuchu znajduje się po prawej stronie, dany cukier ma konfigurację D; jeśli grupa ta jest po lewej stronie, jest to cukier L.
Określenie konfiguracji cukrów w formach piranozowych i furanozowych najwygodniej jest dokonać, korzystając z projekcji Hawortha. Jeśli grupa −CH2OH znajduje się nad płaszczyzną pierścienia, mówimy o izomerze D; jeżeli jest skierowana w dół, jest to izomer L. Cukry w przyrodzie to najczęściej D-cukry.
Cząsteczkom posiadającym formę mezo nie nadaje się żadnego z szeregu konfiguracyjnego.

|

| |
|
(naturalny) |
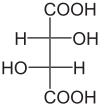
D-(-)-kwas winowy |
forma mezo kwasu winowego |
Aminokwasy[edytuj | edytuj kod]
W przypadku α-aminokwasów określenia konfiguracji względnej dokonuje się rysując cząsteczkę aminokwasu w projekcji Fischera ustawiając grupę karboksylową −COOH na górze, łańcuch boczny aminokwasu ustawia się na dole (podobnie jak grupę −CH2OH w cukrach) natomiast w poziomych ustawieniach znajdują się grupa −NH2 oraz −H. Położenie grupy aminowej determinuje szereg D lub L aminokwasu adekwatnie do grupy −OH aldehydu glicerynowego. Aminokwasy tworzące białka to L-aminokwasy. D-Aminokwasy występują znacznie rzadziej i nie są spotykane w białkach.
Zobacz też[edytuj | edytuj kod]
Przypisy[edytuj | edytuj kod]
- ↑ Michal Sobkowski, Jacek Stawinski, Adam Kraszewski, A Proposal for a New Stereochemical Notation for P -Chiral Nucleotide Analogues and Related Compounds, „Nucleosides, Nucleotides and Nucleic Acids”, 24 (9), 2005, s. 1301–1307, DOI: 10.1080/15257770500230392 [dostęp 2024-01-04] (ang.).
Bibliografia[edytuj | edytuj kod]
- R.T. Morrison, R.N. Boyd: Chemia organiczna. T. 2. Warszawa: Wydawnictwo Naukowe PWN, 1997, s. 309–334, 363. ISBN 83-01-04166-8.
Linki zewnętrzne[edytuj | edytuj kod]
- D and L Are Outmoded and Wrong, chemistry.umeche.maine.edu [zarchiwizowane 2011-02-09] (ang.).