Proteinaza K
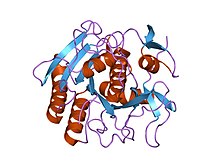
Proteinaza K, proteaza K, endopeptydaza K (EC 3.4.21.64[2]) – enzym należący do rodziny proteaz serynowych S8. Masa cząsteczki 28 900 daltonów.
Został odkryty w 1974 roku w grzybie Engyodontium album (dawniej Tritirachium album)[3]. Proteinaza K jest w stanie strawić keratynę (włosy), stąd nazwa "proteinaza K". Podstawowym miejscem ataku enzymu jest wiązanie peptydowe sąsiadujące z grupą karboksylową aminokwasów alifatycznych bądź aromatycznych z zablokowaną grupą aminową.
Proteinaza K jest powszechnie używana z uwagi na jej szerokie spektrum działania. W biologii molekularnej służy zazwyczaj do trawienia i usuwania zanieczyszczeń białkowych podczas izolacji kwasów nukleinowych. Po jej dodaniu następuje też szybka dezaktywacja nukleaz, które mogłyby zdegradować DNA lub RNA podczas procesów ich oczyszczania. Nadaje się ona dobrze do tego celu dzięki zdolności do działania w obecności denaturujących związków chemicznych takich jak Laurylosiarczan sodu (SDS) i mocznik, związków chelatujących takich jak EDTA, związków tiolowych, jak również inhibitorów trypsyny czy chymotrypsyny. Co więcej, proteinaza K zachowuje stabilność w szerokim zakresie pH 4-12, z optimum pomiędzy pH 7.5 a 12[3].
Aktywność proteinazy K w stosunku do natywnych białek jest stymulowana przez czynniki denaturujące w rodzaju SDS, mimo że aktywność enzymu mierzona w stosunku do oligopeptydów maleje. Wynika to z ułatwionego dostępu enzymu do długiego łańcucha polipeptydowego rozwiniętego na skutek denaturacji[4].
Przypisy[edytuj | edytuj kod]
- ↑ C. Betzel, T.P. Singh, M. Visanji i inni. Structure of the complex of proteinase K with a substrate analogue hexapeptide inhibitor at 2.2-A resolution. „J. Biol. Chem.”. 268 (21), s. 15854–8, lipiec 1993. PMID: 8340410.
- ↑ Enzyme entry: EC 3.4.21.64, [w:] Enzyme nomenclature database, SIB Swiss Institute of Bioinformatics (ang.).
- ↑ a b W. Ebeling i inni, Proteinase K from Tritirachium album Limber, „European Journal of Biochemistry”, 47 (1), 1974, s. 91–7, DOI: 10.1111/j.1432-1033.1974.tb03671.x, PMID: 4373242.
- ↑ H. Hilz, U. Wiegers, P. Adamietz. Stimulation of proteinase K action by denaturing agents: application to the isolation of nucleic acids and the degradation of 'masked' proteins. „Eur. J. Biochem.”. 56 (1), s. 103–8, 1975. DOI: 10.1111/j.1432-1033.1975.tb02211.x. PMID: 1236799.
Linki zewnętrzne[edytuj | edytuj kod]
- Proteinase K Worthington enzyme manual
