Mikroglej
 |
Ten artykuł od 2014-01 zawiera treści, przy których brakuje odnośników do źródeł. |
Mikroglej (ang. microglia, third element) – komórki nieneuronalne centralnego układu nerwowego, tkankowo specyficzne, rezydentne makrofagi kontrolujące homeostazę i biorące udział w odpowiedzi immunologicznej.
Historia[edytuj | edytuj kod]
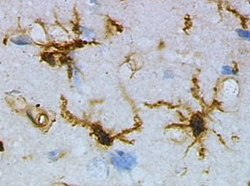
Pierwszymi poważnymi badaniami nad opisem gleju zajął się Santiago Ramon y Cajal (1852–1934) który scharakteryzował trzy podstawowe rodzaje komórek glejowych. Doniósł on o obecności komórek o kształcie gwieździstym – nieświadom tego że są to astrocyty, komórek włóknistych z licznymi wypustkami i komórek protoplazmatycznych występujących licznie w istocie szarej. Jak się okazało później jest to mikroglej. Niezależnie odkryty przez Nissla i Robertsona, dokładniejszy opis zyskał jednak dzięki uczniowi Cajala, Pío del Río-Hortedze (1882–1945). W wyniku barwienia solami srebra Hortega wyróżnił specyficzny rodzaj komórek zawierających jądro o wyraźnie wydłużonym kształcie. Scharakteryzowane przez niego komórki mikrogleju zyskały od tej pory miana komórek Hortegi. Następny „krok milowy” w badaniach nad mikroglejem należał znów do Hortegi, który opisywał rolę odkrytego mikrogleju w patologii centralnego układu nerwowego. W późniejszych latach, w wyniku zidentyfikowania komórkowo specyficznych markerów narastały kontrowersje wokół rozwoju embrionalnego jak i pochodzenia mikrogleju. Te i inne wątpliwości rozwiały zaawansowane badania w latach 80. z użyciem markerów lektynowych oraz rozwiniętych technik immunocytochemicznych.
Pochodzenie[edytuj | edytuj kod]
Na temat pochodzenia mikrogleju prowadzono już wiele debat, na podstawie których nawet obecnie trudno jednoznacznie określić rodowód tych komórek[1]. Zdania są podzielone i część badaczy stoi na stanowisku, że źródłem mikrogleju są komórki linii monocytarnej, a więc prekursorów dopatrują się w mezodermie. Dowodem popierającym mezodermalną tezę są badania prowadzone przez Ling (Ling i in. 1980) polegające na znakowaniu monocytów z krwi obwodowej noworodków koloidalnym węglem i późniejszym lokalizowaniu ich w tkance nerwowej mózgu. Niepodważalnym dowodem jest również fakt, że komórki mikrogleju posiadają na swojej powierzchni markery F4/80, Mac-1, ED1, lektyny (GSA I-B4) typowe dla monocytów i makrofagów oraz receptory na Fc,CR3 (Perry i in. 1985). Faktem potwierdzającym założenie mezodermalnej teorii jest również obecność w cytoplazmie mikrogleju elementów lysozymu, oraz takich enzymów jak niespecyficzna esteraza czy peroksydaza.
Zgodnie z mezodermalną teorią pochodzenia komórek mikrogleju monocyty infiltrują parenchymę mózgu we wczesnych okresach życia embrionalnego jako mikroglej amebowaty. Zaznaczyć trzeba że napływ mikrogleju do mózgu jest dodatnio skorelowany z rozwojem unaczynienia tkanki nerwowej co również przemawia za mezodermalnym źródłem mikrogleju (Perry i in. 1985, Miyake i in. 1984, Hurley i in. 1996). Opuszczenie naczyń krwionośnych przez te komórki jest możliwe gdyż bariera krew-mózg tworzona w tym czasie przez astrocyty nie jest jeszcze dokładnie zamknięta w tym stadium życia organizmu. Po przeniknięciu dochodzi do transformacji mikrogleju amebowatego w mikroglej spoczynkowy charakteryzujący się obkurczoną częścią cytoplazmatyczna oraz licznymi rozgałęzieniami (Boya i in. 1991, Fedoroff i in. 1995).
Jako alternatywne źródło mikrogleju podaje się neuroektodermę, z której wywodzą się glioblasty będące prekursorami astrocytów i oligodendrocytów (Fujita i in. 1975,1980). Jednym z dowodów popierających teorię ektodermalnego pochodzenia mikrogleju jest fakt, że mikroglej, jak i komórki progenitorowe 0-2A, z których mogą się rozwinąć oligodendrocyty oraz astrocyty typu drugiego, posiadają jednakowe właściwości histochemiczne. Poza tym zidentyfikowano homologiczne epitopy powierzchniowe zlokalizowane na astrocytach, jak i na mikrogleju, a rozpoznawane przez przeciwciała monoklonalne LN-1 (Dickson i in. 1989). Zgodnie z neuroektodermalną teorią o pochodzeniu mikrogleju zakłada się, że mikroglej wykształcił się jako samodzielna linia z puli komórek macierzystych neurogleju. Faktem przemawiającym za tą teorią jest to, że glioblasty ze strefy okołokomorowej wykształconej z cewki nerwowej są prekursorami komórek Hortegi. Znaczyłoby to że oligodendrocyty, astrocyty i mikroglej są grupami siostrzanymi pochodzącymi z tej samej linii multipotencjalnych komórek neuroektodermalnych (Fujita i in. 1975,1980).
Ze względu na brak jednoznacznych i niepodważalnych faktów przemawiających za jedną z opcji pochodzenia mikrogleju proponowane jest alternatywne heterogeniczne jest źródło (De Groot i in.). Według tego założenia część mikrogleju zasiedlającego tkankę nerwową jest pochodzenia mezodermalnego, a część neuroektodermalnego. Bez względu na pochodzenie mikrogleju, przyjmuje on w mózgu formy i funkcje charakterystyczne tylko dla tego rodzaju komórek gleju w dużym stopniu zależne od stanu fizjologicznego tkanki.
Funkcja mikrogleju[edytuj | edytuj kod]
Mikroglej stanowiący około 5-20% populacji komórek nieneuronalnych w mózgu występuje w warunkach normalnych w formie spoczynkowej. Główne funkcje fizjologiczne mikrogleju sprowadzają się do monitorowania mikrośrodowiska tkanki, usuwania umierających neuronów i reakcji w wyniku stwierdzenia obecności obcego antygenu (Nakajima i in. 1993). W formie nieaktywnej mikroglej posiada liczne i długie rozgałęzienia części cytoplazmatycznej komórki. Ta specyficzna struktura prawdopodobnie ułatwia potencjalną reakcję tych komórek jako specyficznego dla tkanki nerwowej elementu układu immunologicznego.
Charakterystyczna transformacja mikrogleju z formy spoczynkowej do aktywowanej została poznana i opisana przez Rio Hortege prawie wiek temu. W wyniku aktywacji dochodzi do przemian morfologicznych którym towarzyszy: zwiększenie rozmiaru ciała komórki oraz obkurczenie rozgałęzień. Na poziomie molekularnym dochodzi do ekspresji białek adhezyjnych, reorganizacji cytoszkieletu oraz ekspresja elementów kompleksu zgodności tkankowej MHC typu I jak i II (Perry i in. 1987, 1989, Aloisi i in. 2000).
Zaobserwowano, że aktywowanie mikrogleju może odgrywać rolę w ciężkich postaciach zaburzeń psychiatrycznych[2].
Mikroglej w uszkodzonej tkance nerwowej[edytuj | edytuj kod]
W wyniku uszkodzenia tkanki nerwowej dochodzi w mózgu do odpowiedzi komórkowej i chemicznej otaczających komórek które to reakcje są efektem fizycznego naruszenia integralności tkanki nerwowej, jak i zmian w lokalnym mikrośrodowisku np. zmiany homeostazy jonowej. Jednocześnie z uszkodzeniem uruchamianych jest wiele procesów mających na celu doprowadzić z jednej strony do ochrony przed czynnikami uszkadzającymi z drugiej do naprawy powstałych zniszczeń tkanki (Berkenbosch i in. 1992).
Odpowiedzi komórkowej na czynnik uszkadzający w większości przypadków towarzyszy: proliferacja i migracja komórek mikrogleju i astrocytów, produkcja cytokin prozapalnych, funkcjonalne zmiany w śródbłonku naczyń krwionośnych oraz rekrutacja z krwiobiegu komórek układu immunologicznego w obręb uszkodzonej tkanki (Dong i in. 2001, Aloisi i in. 2001). W uszkodzonych neuronach dochodzi do ekspresji wczesnych genów odpowiedzialnych za stymulację i aktywowanie astrocytów i mikrogleju (Neumann i in. 2001, Raivich i in. 1999). A poprzez przerwaną ciągłość bariery krew-mózg aktywowane zostają monocyty z krwi obwodowej które na wzór mikrogleju ulegają następnie transformacji morfologicznej (Fujita i in. 1998, Leong i in. 1992, Maxwell i in. 1990).
Aktywacja mikrogleju jaką wywołuje uszkodzenie tkanki związana jest ze wzrostem poziomu czynników o funkcji immunologicznej. W okresie tym może dojść do indukcji ekspresji szerokiej rzeszy receptorów powierzchniowych które przyspieszają odpowiedź immunologiczną. Pośród nich są receptory biorące udział w rozpoznawaniu cząsteczek związanych z patogenem, receptory komplementu (np. CR1, CR3, CR4), receptory cytokin (np. TNFRI, TNFRII, IL-1RI, IL-12R) oraz chemokin (np. CCR2, CCR3, CXCR4, CX3CR1) jak i receptory ułatwiające interakcje z układem immunologicznym jak np. z limfocytami T czy immunoglobulinami (np. Fc RI, RII, RIII) (Aloisi i in. 2001, Perry i in. 1992, Nakajima i in. 1993).
W wyniku uszkodzenia CNS napływowe monocyty oraz mikroglej zaczynają produkować również wiele związków prozapalnych takich jak cytokiny (IL-1,TNFα, IL-6, IL-12, IL-15, IL –18), chemokiny (IL-8, fraktalkina, IP-10, MIP-1α, MIP-1β, MCP-1, RANTES, MDC) oraz związki cytotoksyczne (iNOS, wolne rodniki tlenowe i azotowe) i prostanoidy (PGD2, PGE2, tromboksan B2) Aloisi i in. 2001). Rezultatem tego działania jest wzmożony napływ elementów krwiopochodnych z krwi obwodowej takich jak kolejna fala monocytów i makrofagów oraz limfocytów T i B, czy neutrofile. W pierwszej fazie odpowiedzi immunologicznej inicjowanej przez takie cytokiny jak IL-1, IL-6 czy TNF dochodzi do synergicznej reakcji monocytów, makrofagów oraz mikrogleju. Fakt ten wskazuje na współzależność tych komórek w efekcie uszkodzenia tkanki nerwowej.
Zwiększona proliferacja, migracja a przede wszystkim silna fagocytoza to cechy mikrogleju oraz makrofagów sprzyjające naprawie uszkodzonych części tkanki. Wzmożona proliferacja mikroleju w obrębie uszkodzenia jest efektem interakcji z uszkodzonymi neuronami jak również wynikiem skomplikowanych oddziaływań ze strony astrocytów oraz autostymulacji mikrogleju (Aloisi i in. 2001, Neumann i in. 2001, Dong i in. 2001). W wyniku kontaktu z uszkodzonym neuronem lub degenerującym połączeniem neuronalnym mikroglej wykazuje zdolność do transformacji w fagocyta – makrofaga mającego za cel usunięcie pozostałości z miejsca uszkodzenia tkanki nerwowej.
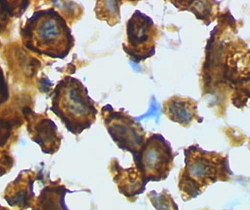
Właściwością aktywowanego mikrogleju służącą precyzyjnemu przeciwdziałaniu przyczynom oraz skutkom uszkodzenia mózgu jest zdolność tych komórek do transformacji w komórki prezentujące antygen (APC). Elementem kluczowym w pełnieniu tej funkcji przez komórkę mikrogleju jest zdolność do produkcji przez nią cząsteczki powierzchniowej CD40 oraz ekspresji elementów kompleksu zgodności tkankowej MHC typu I jak i II. Systemy oddziaływań CD40 – CD40L, MHC-II – TCR uważane są za kluczowe elementy w rozwoju odpowiedzi immunologicznej. Interakcje te mogą doprowadzić do rozwoju i różnicowania się aktywowanych limfocytów B czy też do pełnej aktywacji limfocytów T poprzez ekspresję cząsteczek stymulujących co ma miejsce w przypadku MS i EAE (Perry i in. 1987, 1989, Aloisi i in. 2000,2001).
W rezultacie odpowiedzi immunologicznej ze strony aktywowanego mikrogleju dochodzi z jednej strony do indukcji kaskady procesów naprawczych w obrębie uszkodzenie tkanki nerwowej. Z drugiej jednak strony procesowi naprawy towarzyszy wtórne uszkodzenie tkanki nerwowej a szczególnie neuronów co jest efektem nadmiernej produkcji cytokin prozapalnych (np. TNFα) produkowanych przez aktywowany mikroglej. Czynnikiem cytotoksycznym jest również produkcja wolnych rodników tlenowych jak i azotowych przez fagocyty usuwające pozostałości pierwotnego uszkodzenia.
Przypisy[edytuj | edytuj kod]
- ↑ Kazuyuki Nakajima, Shinichi Kohsaka. Functional roles of microglia in the brain. „Neurosci Res.”. 17 (3), s. 187-203, August 1993. DOI: 10.1016/0168-0102(93)90047-T. [dostęp 2017-04-30]. (ang.).
- ↑ Mondelli, Valeria, Vernon, Anthony C, Turkheimer, Federico et al. Brain microglia in psychiatric disorders. „Lancet Psychiatry.”, 2017 Apr 25. DOI: 10.1016/S2215-0366(17)30101-3. [dostęp 2017-04-30]. (ang.).
Bibliografia[edytuj | edytuj kod]
- K. Nakajima, S. Kohsaka, Functional roles of microglia in the brain, „Neuroscience Research”, 17 (3), 1993, s. 187–203, DOI: 10.1016/0168-0102(93)90047-T, ISSN 0168-0102, PMID: 8233123.
- V.H. Perry, D.A. Hume, S. Gordon, Immunohistochemical localization of macrophages and microglia in the adult and developing mouse brain, „Neuroscience”, 15 (2), 1985, s. 313–326, ISSN 0306-4522, PMID: 3895031.
- Tadahisa Kitamura, Toshihiko Miyake, Setsuya Fujita, Genesis of resting microglia in the gray matter of mouse hippocampus, „The Journal of Comparative Neurology”, 226 (3), 1984, s. 421–433, DOI: 10.1002/cne.902260310, ISSN 1096-9861, PMID: 6747031 (ang.).
- S.D. Hurley i inni, Cytokine transcripts expressed by microglia in vitro are not expressed by ameboid microglia of the developing rat central nervous system, „Glia”, 25 (3), 1999, s. 304–309, ISSN 0894-1491, PMID: 9932876 [dostęp 2017-06-04].
- J Boya i inni, A lectin histochemistry study on the development of rat microglial cells., „Journal of Anatomy”, 175, 1991, s. 229–236, ISSN 0021-8782, PMID: 2050568, PMCID: PMC1224482.
- S. Fedoroff, C. Hao, Origin of microglia and their regulation by astroglia, „Advances in Experimental Medicine and Biology”, 296, 1991, s. 135–142, ISSN 0065-2598, PMID: 1781324.
- S. Fujita, T. Kitamura, Origin of brain macrophages and the nature of the so-called microglia, „Acta Neuropathologica. Supplementum”, Suppl 6, 1975, s. 291–296, ISSN 0065-1435, PMID: 168722.
- S. Fujita, Cytogenesis and pathology of neuroglia and microglia, „Pathology, Research and Practice”, 168 (4), 1980, s. 271–278, DOI: 10.1016/S0344-0338(80)80269-X, ISSN 0344-0338, PMID: 7413517.
- D.W. Dickson, L.A. Mattiace, Astrocytes and microglia in human brain share an epitope recognized by a B-lymphocyte-specific monoclonal antibody (LN-1)., „The American Journal of Pathology”, 135 (1), 1989, s. 135–147, ISSN 0002-9440, PMID: 2476034, PMCID: PMC1880225.
- Corline J. de Groot, Christine D. Dijkstra, Taede Sminia, Discrimination between different types of neuroglial cells in rat central nervous system using combined immuno- and enzyme-histochemical methods, „Immunobiology”, 178 (3), 1988, s. 177–190, DOI: 10.1016/S0171-2985(88)80063-9, ISSN 0171-2985, PMID: 2465992.
- B. Hugh Perry, Siamon Gordon, Modulation of CD4 antigen on macrophages and microglia in rat brain, „The Journal of Experimental Medicine”, 166 (4), 1987, s. 1138–1143, DOI: 10.1084/jem.166.4.1138, ISSN 0022-1007, PMID: 2443599, PMCID: PMC2188707.
- V.H. Perry, S. Gordon, Macrophages and microglia in the nervous system, „Trends in Neurosciences”, 11 (6), 1988, s. 273–277, DOI: 10.1016/0166-2236(88)90110-5, ISSN 0166-2236, PMID: 2465626.
- F. Aloisi, The role of microglia and astrocytes in CNS immune surveillance and immunopathology, „Advances in Experimental Medicine and Biology”, 468, 1999, s. 123–133, ISSN 0065-2598, PMID: 10635024.
- F. Berkenbosch, Macrophages and astroglial interactions in repair to brain injury, „Annals of the New York Academy of Sciences”, 650, 1992, s. 186–190, DOI: 10.1111/j.1749-6632.1992.tb49119.x, ISSN 0077-8923, PMID: 1605474.
- F. Aloisi, Immune function of microglia, „Glia”, 36 (2), 2001, s. 165–179, ISSN 0894-1491, PMID: 11596125.
- H. Neumann, Control of glial immune function by neurons, „Glia”, 36 (2), 2001, s. 191–199, ISSN 0894-1491, PMID: 11596127.
- Gennadij Raivich, Like cops on the beat: the active role of resting microglia, „Trends in Neurosciences”, 28 (11), 2005, s. 571–573, DOI: 10.1016/j.tins.2005.09.001, ISSN 0166-2236, PMID: 16165228.
- T. Fujita i inni, Cellular dynamics of macrophages and microglial cells in reaction to stab wounds in rat cerebral cortex, „Acta Neurochirurgica”, 140 (3), 1998, s. 275–279, ISSN 0001-6268, PMID: 9638265.
- Seng-Kee Leong, Eng-Ang Ling, Amoeboid and ramified microglia: their interrelationship and response to brain injury, „Glia”, 6 (1), 1992, s. 39–47, DOI: 10.1002/glia.440060106, ISSN 0894-1491, PMID: 1380949.
- William L. Maxwell i inni, Thalamic nuclei after human blunt head injury, „Journal of Neuropathology and Experimental Neurology”, 65 (5), 2006, s. 478–488, DOI: 10.1097/01.jnen.0000229241.28619.75, ISSN 0022-3069, PMID: 16772871.
- V.H. Perry, P.B. Andersson, The inflammatory response in the CNS, „Neuropathology and Applied Neurobiology”, 18 (5), 1992, s. 454–459, DOI: 10.1111/j.1365-2990.1992.tb00811.x, ISSN 0305-1846, PMID: 1454134.
- Kazuyuki Nakajima i inni, Microglia-derived elastase produces a low-molecular-weight plasminogen that enhances neurite outgrowth in rat neocortical explant cultures, „Journal of Neurochemistry”, 61 (6), 1993, s. 2155–2163, DOI: 10.1111/j.1471-4159.1993.tb07454.x, ISSN 0022-3042, PMID: 8245967.
