Obrazowanie przedkliniczne
Obrazowanie przedkliniczne – pojęcie odnoszące się do obrazowania medycznego przeprowadzanego w fazie przedklinicznej badań eksperymentalnych. Może być przeprowadzane in vitro na komórkach i tkankach wyizolowanych z organizmów zwierząt lub in vivo na żywym organizmie[1]. Stosuje się również odmianę in vivo nazywaną ex vivo, która od in vivo różni się tym, że materiał biologiczny jest pozyskiwany z żywego organizmu w celu jego modyfikacji in vitro i ponownego podania z powrotem do organizmu, z którego go pozyskano. W odróżnieniu od klasycznego obrazowania diagnostycznego (diagnostyki obrazowej), obrazowanie przedkliniczne skupia się głównie na wykrywaniu zaburzeń na poziomie molekularnym, które stoją u podstaw rozwoju procesów chorobowych, a nie na widocznych końcowych efektach tych procesów[2]. Wykorzystując techniki biomedyczne, biotechnologię, nanoinżynierię oraz przetwarzanie i analizę obrazów, obrazowanie to pozwala na obserwację organów, tkanek, komórek czy molekuł w badanych obiektach pod kątem zmian powstałych na skutek oddziaływania różnych substancji lub czynników środowiskowych. Bezinwazyjne metody obrazowania in vivo, umożliwiając głębsze zrozumienie zarówno procesów chorobowych jak i zachowania substancji w organizmie, zyskały duże znaczenie zwłaszcza w badaniach nad rozwojem leków[3]. Do obrazowania całych organizmów lub ich organów zwykle wykorzystywane są: mikro-ultrasonografia (USG), obrazowanie magnetycznego rezonansu jądrowego (ang. magnetic resonance imaging, MRI) oraz tomografia komputerowa (ang. computed tomography CT), natomiast do obrazowania molekularnego stosuje się częściej emisyjną tomografię pozytonową (ang. positron emission tomography] PET), komputerową tomografię pojedynczego fotonu (ang. single photon emission computed tomography] SPECT), tomografię fotoakustyczną (ang. photoacoustic tomography] PAT) oraz techniki obrazowania optycznego: bioluminescencję i fluorescencję.
Faza przedkliniczna badań eksperymentalnych[edytuj | edytuj kod]
Badania eksperymentalne można podzielić na pięć faz[4]:
- badania podstawowe (laboratoryjne) – synteza nowych związków chemicznych,
- badania przedkliniczne – ocena działania związku poprzez próby in vivo i in vitro,
- badania kliniczne fazy I – pierwszy kontakt testowanego środka z organizmem człowieka; ocena bezpieczeństwa stosowania,
- badania kliniczne fazy II – określenie działania leku, jego dawki, wchłaniania, metabolizmu, wydalania,
- badania kliniczne fazy III – ostateczne stwierdzenie skuteczności badanej substancji,
Badanie eksperymentalne w fazie drugiej (przedklinicznej), do której zalicza się obrazowanie przedkliniczne, stanowią podstawę w badaniu właściwości leków. Jest to pierwszy etap właściwych badań nad wyodrębnioną we wcześniejszych testach substancją, mającą znaleźć później zastosowanie w medycynie. Substancja taka musi przejść próby na komórkach in vitro oraz in vivo, co wiąże się z koniecznością przeprowadzania testów na zwierzętach[4]. Badania na zwierzętach są podstawowym sposobem oceny wpływu różnych substancji na organizm człowieka i pozwalają przewidzieć skutki ich oddziaływania i/lub wyjaśnić przyczyny powstałej odpowiedzi i zachowania organizmu. Ponadto umożliwiają sprawdzenie działania np. kosmetyków, składników zawartych w badanym pokarmie czy np. wpływ środowiska na organizm itp.[1]
| gatunek | zastosowanie |
|---|---|
| myszy | badania farmakologiczne, onkologiczne, biochemiczne, mikrobiologiczne, immunologiczne |
| szczury | badania farmakologiczne, toksykologiczne, onkologiczne, fizjologiczne |
| myszoskoczki | eksperymenty neurochirurgiczne |
| nornice | badania biomedyczne |
| króliki | badania ciał gorączkotwórczych, badania działania miejscowo-drażniącego; apirogenność płynów aptecznych, immunizacja, badania ortopedyczne |
| świnki morskie | badania farmakologiczne, toksykologiczne, immunologiczne, źródło leukocytów do badań w hodowlach komórkowych |
| ryby (Danio rerio) | badania chemiczne, genetyczne, farmakologiczne |
Główne zastosowania badań na zwierzętach to:
- analiza oddziaływań na tkanki organizmów żywych różnych komórek, które odpowiadają za rozwój procesów chorobotwórczych,
- śledzenie farmaceutyków i innych substancji w trakcie ich interakcji z tkankami, między innymi:
- badanie metabolizmu leków,
- określenie dawki śmiertelnej oraz optymalnej,
- badanie reakcji na różne stężenia danej substancji,
- rozwój biofarmaceutyków, radiofarmaceutyków.
Z powodu licznych kontrowersji wokół wykorzystywania zwierząt w eksperymentach, trwają poszukiwania alternatywnych rozwiązań. Początek tego nurtu datuje się na rok 1959, kiedy to R.L. Burch oraz zoolog W.M.S. Russell opublikowali pracę "The Principles of Humane Experimental Technique", w której przedstawili trzy koncepcje dążenia do wyeliminowania badań na zwierzętach, tak zwane 3R: Replacement (zastąpienie), Reduction (ograniczenie) oraz Refinement (doskonalenie)[5].
Regulacje prawne[edytuj | edytuj kod]
Badania stosujące eksperymenty na zwierzętach podlegają ścisłym unormowaniom prawnym. Najważniejszymi dokumentami regulującymi postępowanie w badaniach klinicznych są norma ISO 10993 oraz Ustawa o doświadczeniach na zwierzętach z dnia 21.01.2005 r. Instytucje sprawujące pieczę nad badaniami klinicznymi w Polsce to[1]:
- Komisja Etyczna Badań na Zwierzętach,
- Lokalna Komisja Etyczna ds. Doświadczeń na Zwierzętach,
- Krajowa Komisja Etyczna ds. Doświadczeń na Zwierzętach,
- Ministerstwo Nauki i Szkolnictwa Wyższego.
Ministerstwo Nauki i Szkolnictwa Wyższego publikuje wykaz specjalnie przystosowanych jednostek badawczych, które spełniając wszystkie wymogi, uprawnione są do przeprowadzania eksperymentów na zwierzętach.
Wybrane jednostki uprawnione do badań eksperymentalnych w Polsce, według listy opublikowanej przez Ministerstwo Nauki i Szkolnictwa Wyższego (2010r)[6]:
- Ośrodek Diagnostyczno – Badawczy Chorób Przenoszonych Drogą Płciową w Białymstoku,
- Akademia Świętokrzyska w Kielcach Wydział Matematyczno – Przyrodniczy,
- Instytut Przemysłu Organicznego oddział w Pszczynie,
- SLW BIOLAB s. c. Weterynaryjne Laboratorium Diagnostyczne w Ostródzie,
- Instytut Biologii Doświadczalnej im. M. Nenckiego Polska Akademia Nauk w Warszawie,
- Instytut Farmakologii Polska Akademia Nauk w Krakowie,
- Instytut Medycyny Doświadczalnej i Klinicznej im. M. Mossakowskiego Polska Akademia Nauk w Warszawie,
- Państwowy Instytut Weterynaryjny – Państwowy Instytut Badawczy w Puławach,
- Narodowy Instytut Leków w Warszawie,
- Wojewódzki Inspektorat Weterynaryjny w Katowicach Zakład Higieny Weterynaryjnej.
Rynek obrazowania przedklinicznego w Polsce[edytuj | edytuj kod]
Dostępne dane wskazują, że nowy lek wprowadzony na rynek pochłania nakłady ok. 3–3,5 mld złotych (warto zauważyć, że są to nakłady ponoszone na przestrzeni kilku do kilkunastu lat), z czego aż ok. 25% przypada na badania przedkliniczne i na pierwsze etapy badań klinicznych[1]. W 2010 roku wartość rynku diagnostyki obrazowej osiągnęła 674 mln złotych (wartość rynku diagnostyki obrazowej rozumiana jest tu jako sprzedaż urządzeń diagnostycznych w danym okresie z następujących segmentów: medycyna nuklearna, rentgenodiagnostyka, rezonans magnetyczny, tomografia komputerowa i ultrasonografia). Według prognoz, sprzedaż na tym rynku miała rosnąć w tempie 16% rocznie i przekroczyć 1 mld złotych w 2012 roku. Głównie sektor publiczny przyczynia się do stabilnego rozwoju rynku. Wiele inwestycji finansowanych jest z funduszy UE (Program Operacyjny Infrastruktura i Środowisko czy Regionalne Programy Operacyjne). Dofinansowanie do zakupu aparatury do diagnostyki obrazowej można również uzyskać z funduszy krajowych. Głównym źródłem finansowania jest Narodowy Program Zwalczania Chorób Nowotworowych. Sprzęt do tradycyjnej diagnostyki (głównie USG) finansowany jest również przez Wielką Orkiestrę Świątecznej Pomocy[7].
Obrazowanie molekularne jako obrazowanie przedkliniczne[edytuj | edytuj kod]
Do obrazowania przedklinicznego wykorzystuje się metody obrazowania molekularnego. Należy ono do technik biomedycznych i biotechnologicznych pozwalających na analizę molekularnych i wewnątrzkomórkowych zjawisk występujących w organizmach żywych i prowadzących do zrozumienia procesów fizjologicznych i patologicznych. Obrazowanie molekularne jest pochodną postępu w zakresie biologii komórkowej i molekularnej oraz metod projektowania leków. Szczególnie szybki rozwój tej dziedziny nastąpił w połowie lat 90. XX wieku, dzięki rosnącemu zainteresowaniu medycyną komórkową i molekularną oraz powstaniu i upowszechnieniu biotechnologii, rozwojowi technik laserowych i optoelektronicznych oraz dostępności dużych mocy obliczeniowych komputerów wymaganych do analizy uzyskiwanych obrazów[8]. W obrazowaniu molekularnym wyróżnić można techniki wykorzystujące egzogenne środki kontrastujące lub z zastosowaniem endogennych markerów, jak np.: micro-MRI, micro-PET, micro-CT czy micro-SPECT oraz techniki optyczne, jak bioluminescencja i fluorescencja[9]. Dodatkowo istnieją jeszcze techniki niewykorzystujące markerów, jak micro-USG oraz micro-PAT. Zastosowania obrazowania molekularnego to między innymi: genetyka, karcynogeneza, badania nad genomem, testowanie terapii genowej[2].
Micro-MRI[edytuj | edytuj kod]
Obrazowanie za pomocą jądrowego rezonansu magnetycznego (magnetic resonance imaging, MRI) wykorzystuje właściwości magnetyczne jąder atomu wodoru. Jądra atomowe wodoru umieszczone w stałym zewnętrznym polu magnetycznym pochłaniają rezonansowo impulsy fal elektromagnetycznych o częstotliwości radiowej. Impulsy te wysyłane są w kierunku pacjenta przez elektromagnes. Kolejne warstwy ciała pochłaniają impulsy, wytwarzając w odpowiedzi na nie miniaturowe wirujące pola magnetyczne. Pola te z kolei generują własne impulsy zwrotne, które odbierane są przez cewki odbiorcze znajdujące się w cylindrze wokół ciała pacjenta. Bezpośrednio mierzoną wielkością są sygnały prądu zmiennego indukowane w cewkach po pewnym czasie od zadziałania każdego impulsu pobudzającego. Komputer, obliczając rozkład amplitudy sygnału w płaszczyźnie danej warstwy, tworzy mapę z wektora magnetyzacji jąder wodoru. Zróżnicowanie tkanek na obrazie końcowym uzyskiwane jest dzięki różnicom zawartości wodoru w poszczególnych komórkach, które odpowiadają za powstawanie pól o odmiennych impulsach elektromagnetycznych[10].
MRI może być przeprowadzone z wykorzystaniem urządzeń z otworami o małej średnicy (poniżej 20 centymetrów), dzięki czemu może zostać użyte do badania mniejszych obiektów, jak małe zwierzęta. Silniejsze pole magnetyczne i gradienty, które mogą zostać osiągnięte dzięki mniejszym otworom, pozwalają uzyskać mniejszy wskaźnik szumu oraz większą rozdzielczość. Grupie naukowców z Duke University udało się uzyskać za pomocą micro-MRI obrazy mózgu myszy o rozdzielczości 50x50x500μm w czasie 2-3 godzin, a obrazy serca myszy (przy problemach z poruszeniem) o rozdzielczości 120x120x1000μm w czasie 10-13 minut. Dla porównania, typowy woksel w badaniach ludzkiego mózgu za pomocą MRI ma wielkość 800x800x5000μm.[2]
MRI stosowane jest między innymi w badaniach nad zapaleniem mięśnia sercowego, ostrymi zespołami wieńcowymi, ocenie tętnic wieńcowych, stopniem niedokrwienia i żywotości mięśnia sercowego, niewydolnością serca oraz elektrokardiologii[11].
Micro-CT[edytuj | edytuj kod]

Tomografia komputerowa, TK, to rodzaj tomografii rentgenowskiej. W tomografach komputerowych lampa rentgenowska, porusza się ruchem okrężnym wokół badanego obiektu, a zmiany natężenia promieniowania po przejściu przez ciało pacjenta, rejestrowane są za pomocą detektorów umieszczonych na obwodzie układu. Następnie otrzymane dwuwymiarowe przekroje przetwarzane są w sposób elektroniczny i przeprowadzana jest rekonstrukcja do obrazu trójwymiarowego, z wykorzystaniem odwrotnej transformaty Radona. Wyróżnić można następujące systemy tomografii komputerowej: tomograf, w którym stół z pacjentem przesuwany jest skokowo, dla zobrazowania kolejnych przekrojów ciała. Kolejną odmianą tomografu jest system spiralnej tomografii, w którym następuje stała rotacja lampy i ciągłe przesuwanie stołu. Pozwala to na znaczne skrócenie czasu badania. Jeszcze innym rodzajem tomografii jest tomografia komputerowa z wielorzędowym układem detektorów. Na obwodzie układu umieszcza się tu od 4 do 16 rzędów detektorów, co pozwala w czasie jednego obrotu lampy uzyskać odpowiednio od 4 do 16 przekrojów ciała. W czasie jednego takiego badania uzyskuje się do 800 przekrojów ciała, co stanowi ogromną ilość danych, wymagających dedykowanego oprogramowania komputerowego w celu przetworzenia[10].

Dzięki zastosowaniu micro-CT, udaje się uzyskać rozdzielczość do 50μm w czasie od 15 do 20 minut w badaniach żywych organizmów in vivo. Badania ex vivo, dzięki wyeliminowaniu utrudnień związanych z ruchem, pozwoliły na osiągnięcie woksela wielkości 14x14x14μm i mniejszych[2].
Do zalet tomografii komputerowej zalicza się krótki czas badania, wysoką rozdzielczość uzyskiwanych obrazów, możliwość trójwymiarowych rekonstrukcji oraz brak dyskomfortu u badanych organizmów. Ograniczeniami tej metody są natomiast stosunkowo duża dawka promieniowania jonizującego, które przy nadmiernej ekspozycji może być niebezpieczne dla badanych obiektów oraz ryzyko wystąpienia powikłań w związku z podawaniem środków cieniujących[12].
Micro-PET[edytuj | edytuj kod]
Pozytonowa tomografia emicyjna (ang. positron emission tomography] PET) to metoda obrazowania z wykorzystaniem technik radioizotopowych w ocenie procesów metabolicznych w organizmie. Prototyp gammakamery do badania PET został stworzony już w 1973 roku przez J.S.Robertsona, natomiast w pierwszych dwóch dekadach XXI wieku stała się ona uznaną techniką diagnostyczną w praktyce klinicznej. W badaniu metodą PET pacjentowi podana zostaje substancja radioizotopowa, która w procesie rozkładu emituje pozytony (cząsteczki wielkości elektronów, ale o dodatnim ładunku elektrycznym). W wyniku zderzenia z elektronami znajdującymi się w tkankach ciała, pozytony ulegają anihilacji, tzn. zmianie materii pozytonu i elektronu na dwa kwanty promieniowania elektromagnetycznego o ściśle określonej energii (511 keV), przebiegające równolegle do siebie w dwóch przeciwległych kierunkach[10], które następnie rejestrowane są przez dwa z wielu detektorów ustawionych pod różnymi kątami wokół badanego obiektu. Impuls zostaje zarejestrowany przez układ komputerowy tylko wówczas, gdy równocześnie pobudzona zostanie para przeciwległych detektorów (zjawisko koincydencji). Fakt ten, w połączeniu ze ściśle określoną energią promieniowania, sprawia, że rejestrowane są prawie wyłącznie fale powstałe w wyniku anihilacji. Pozwala to uzyskać obrazy o wysokiej rozdzielczości (do kilku milimetrów).
Naukowcy z Uniwersytetu Kalifornijskiego w Los Angeles stworzyli system micro-PET do obrazowania małych gryzoni. Rozdzielczość uzyskana dzięki temu systemowi to 2mm. Z kolei Szpital Ogólny z Massachusetts skonstruował system PET z pojedynczym pierścieniem, który z powodzeniem uzyskuje rozdzielczość do 1mm. Trwają prace nad ulepszeniem tego sprzętu (wykorzystując specyfikę budowy myszy czy otaczanie badanych obiektów detektorami), aby uzyskać rozdzielczość mniejszą niż 1mm.[2]

Badania techniką PET znajdują szerokie zastosowanie w onkologii, badaniach mózgu czy śledzeniu metabolizmu mięśnia sercowego, schorzeń układu krążenia oraz stanów zapalnych niejasnego pochodzenia[13].
Obecnie praktycznie wszystkie dostępne skanery pozytonowej tomografii emisyjnej są urządzeniami hybrydowymi typu:
- PET-CT, PET/CT – połączenie PET z wielorzędowym tomografem komputerowym,
- PET-MRI, PET/MRI – połączenie PET z rezonansem magnetycznym[14].
Micro-SPECT[edytuj | edytuj kod]
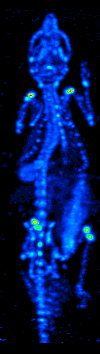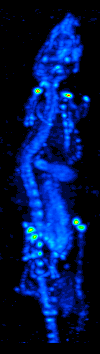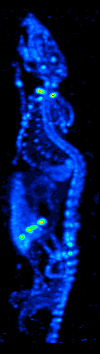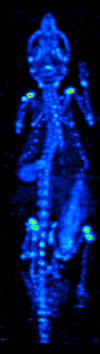
Tomografia emisyjna pojedynczego fotonu jest ważną, nieinwazyjną, szeroko dostępną metodą obrazowania, cechującą się wysoką czułością (ok. 90%) i swoistością (ok. 80%)[15]. Wykorzystuje się w niej radiofarmaceutyki. Są to związki chemiczne składające się z dwóch elementów - ze znacznika, który jest radioaktywnym izotopem oraz z nośnika zdolnego do osadzania się w tkankach i narządach i pokonywania bariery krew-mózg. Nośniki często posiadają właściwość selektywnego wiązania się z przeciwciałami komórek nowotworowych. Osadzają się w ilościach proporcjonalnych do metabolizmu. Radioizotop po wprowadzeniu do organizmu ulega rozpadowi, wydzielając promieniowanie gamma, które jest bezpośrednio rejestrowane (filtrowanie wiązek tylko pod kątem prostym) przez zewnętrzny detektor - kamerę gamma. Obraz przestrzenny uzyskuje się poprzez umieszczenie głowicy kamery gamma na mechanicznym obracanym wysięgniku, który zapewnia ruch kamery wokół badanego obszaru pacjenta.
Badanie SPECT różni się od badania PET tym, że rejestruje bezpośrednio samo promieniowanie, podczas gdy PET wykorzystuje powstałe z anihilacji pozytonów cząstki, które zderzając się z cząstkami tkanek emitują energię, która to jest dopiero rejestrowana przez detektory. PET jest metodą dokładniejszą, ale co za tym idzie, droższą.
Badania micro-SPECT, choć o wiele mniej dokładne niż micro-PET, bo charakteryzujące się rozdzielczością 1,7 mm, są jednocześnie o wile łatwiej dostępne. Ponadto, gryzonie mają większą tolerancję na podawane w badaniu radioizotopy, dzięki czemu możliwe jest podanie im znacznie większej dawki (w przeliczeniu na objętość ciała) niż u pacjentów. Większe stężenie substancji pozwala zatem na zniwelowanie słabej rozdzielczości[2].
Metody optyczne[edytuj | edytuj kod]
Zastosowanie radioizotopów może wywołać działania niepożądane na modelu zwierzęcym. Aby tego uniknąć, stosuje się metody badawcze oparte na znacznikach nieradioizotopowych[9]. Metody te pozwalają na ocenę zjawisk zachodzących w tkankach i komórkach dzięki zastosowaniu sond-znaczników, które selektywnie wiążą się z elementami struktury komórki bądź struktury tkankowej. Wykorzystanie metod obrazowania optycznego pozwala na dynamiczne monitorowanie napływu i współczynnika oczyszczania (klirensu) znaczników oraz ocenę ich farmakokinetyki. Znaczniki biooptyczne można podzielić na wykorzystujące zjawisko bioluminescencji samoistnej lub wywoływanej czynnikiem biochemicznym (np. obecnością danej molekuły) oraz oparte na zjawisku fluorescencji, czyli emisji światła pod wpływem napromieniowania światłem o nieco krótszej długości fali. W obrazowaniu optycznym wykorzystuje się techniki mikroskopowe, między innymi: fluorescencję jedno- i wielofotonową, fluorescencyjną spektroskopię korelacyjną i pomiar czasu relaksacji fluorescencyjnej[8].
Do celów obrazowania optycznego stosuje się układy wielu światłowodów transmitujących światło laserowe o długości fali wzbudzenia do badanego obiektu, np. zwierzęcia, oraz kamer CCD do detekcji promieniowania fluorescencyjnego reemitowanego z badanej tkanki bądź transmitowanego przez nią. Techniki opierające się na analizie skupisk fluoroforu są często wykorzystywane w powiązaniu z innymi technikami obrazowanymi (rentgenografia, CT, MRI). Takie badania pozwalają na uwidocznienie tych skupisk na tle struktury anatomicznej badanego zwierzęcia[8]. Rozdzielczość uzyskiwana technikami mikroskopowymi sięga 10μm.[2]
Micro-USG[edytuj | edytuj kod]
Ultrasonografia to metoda wykorzystująca ultradźwięki do obrazowania tkanek. Emiter wysyła falę ultradźwiękową o określonej częstotliwości. Fala ta odbija się od badanego ośrodka i wraca do odbiornika. Informacje o ośrodkach uzyskuje się dzięki wykorzystaniu różnic w impedancji pomiędzy poszczególnymi tkankami. W USG do uzyskania obrazów 2D lub 3D wykorzystuje się cyfrową obróbkę w połączeniu z odpowiednimi nakładkami na głowicę, między innymi: obrazowanie harmoniczne, ultrasonograficzne obrazowanie fotopowe czy ultrasonografię trójwymiarową.
Micro-USG wykorzystuje wyższe, w porównaniu z tradycyjnym USG, częstosliwości fal. W USG są to częstosliwości 3-15 MHz, podczas gdy micro-USG wykorzystuje częstotliwości 15-80 MHz. Wyższa częstotliwość oznacza krótszą falę, dzięki której można uzyskać wyższą rozdzielczość. Jednocześnie ze wzrostem częstotliwości wzrasta również tłumienie fali, co uniemożliwia badanie głęboko położonych lub dużych obiektów. Wykorzystanie częstotliwości 40-50 MHz pozwala uzyskać obraz o rozdzielczości około 40μm.[2]
Micro-PAT[edytuj | edytuj kod]
Tomografia fotoakustyczna pozwala dokładnie i głęboko zajrzeć pod wierzchnie tkanki ciała, dzięki połączeniu światła i dźwięku. Tradycyjne narzędzia tomografii nie pozwalają na penetrację tkanki głębszą niż 1mm, PAT natomiast umożliwiło pokonanie tej bariery i osiągnięcie obrazowania optycznego o wysokiej rozdzielczości i stopniu penetracji[16]. Prześwietlenie metodą fotoakustyczną, daje kombinację wysokokontrastowych obrazów, uzyskanych w wyniku absorpcji światła przez molekuły badanego organu, z przestrzenną rozdzielczością ultradźwięków. Idea tomografii nowego typu polega na zamianie absorbowanego przez tkanki światła w fale dźwiękowe, które o wiele słabiej, aniżeli światło, rozpraszają się podczas powrotu z wnętrza ciała na jego powierzchnię. Tkanka organu, który ma być zbadany, zostaje najpierw napromieniowana światłem nanosekundowego lasera. Molekuły organu absorbują to światło, po czym generują spowodowany wzrostem temperatury skok ciśnienia. Skok ten powoduje drgania tkanek, przez co powstają fale dźwiękowe, a te są odbierane przez zewnętrzny ultrasonograf, który tworzy fotograficzny obraz badanego fragmentu[17].
Metoda PAT znalazła ważne zastosowanie w diagnostyce czerniaka, z powodu możliwości bardzo dokładnego określenia granic tkanki nowotworowej[18].
Przypisy[edytuj | edytuj kod]
- ↑ a b c d J. Olszewski, A. Jabłecka, J. Piątek, W. Samborski, J. Zawadziński, "Badania eksperymentalne - przedkliniczne na zwierzętach", Nowiny Lekarskie 2011, 80, 3, 219–221
- ↑ a b c d e f g h R. Weissleder, U. Mahmood, "Molecular Imaging", Radiology 2001; 219:316–333
- ↑ J. K. Willmann, N. van Bruggen, L. M. Dinkelborg, S. S. Gambhir, "Molecular imaging in drug development", Nature Reviews Drug Discovery 7, 591-607 (July 2008)
- ↑ a b c Z. Koperwas, "Fazy przeprowadzania badań klinicznych" laboratoria.net
- ↑ N. Ranganatha, I.J. Kuppast, "A Review of Alternatives to Animal Testing Methods in Drug Develompent", International Journal of Pharmacy and Pharmaceutical Sciences, Vol 4, Suppl 5, 2012
- ↑ Wykaz jednostek doświadczalnych uprawnionych do przeprowadzania - Ministerstwo Nauki i Szkolnictwa Wyższego [online], www.nauka.gov.pl [dostęp 2017-11-19] (pol.).
- ↑ A. Stawarska,M. Stefańczyk, "W 2012 r. wartość rynku diagnostyki obrazowej przekroczy 1 mld zł", PMR Publications
- ↑ a b c T. Sołtysiński, A. Liebert, I. Zawicki, R. Maniewski, "Optyczne metody obrazowania molekularnego", Acta Bio-Optica et Informatica Medica 4/2008, vol. 14
- ↑ a b Z. Rogulski, "Obrazowanie molekularne w Centrum Nauk Biologiczno-Chemicznych Uniwersytetu Warszawskiego", Centrum Nauk Biologiczno-Chemicznych Uniwersytetu Warszawskiego, Wydział Chemii, Uniwersytet Warszawski
- ↑ a b c B. Pruszyński, "Radiologia. Diagnostyka obrazowa. Rtg, TK, USG, MR i medycyna nuklearna", Wydawnictwo Lekarskie PZWL, Warszawa 2005
- ↑ T. Rakowski, A. Dziewierz, D. Dudek, "Zastosowanie rezonansu magnetycznego i tomografii komputerowej w kardiologii", Kardiologia - co nowego?
- ↑ J. Walecki, A. Lewszuk, "Tomografia komputerowa", Wydawnictwo Lekarskie PZWL 2010
- ↑ "Definicja badania pozytonowej tomografii emisyjnej (PET-TK)" voxel.pl
- ↑ Pozytonowa tomografia emisyjna PET, Portal onkologiczny zwrotnikRAKA.pl
- ↑ S. Miernik, M. Dziuk, "Metody hybrydowe (SPECT-CT, PET-CT) w diagnostyce choroby wieńcowej i ocenie żywotności mięśnia sercowego", Choroby Serca i Naczyń 2008, tom 5, nr 2, 93–101
- ↑ Lihong V. Wang, "Prospects of photoacoustic tomography", Medical Physics 35, 5758 (2008)
- ↑ Prześwietlenie i przesłuchanie - strona 1 - Polityka.pl [online], www.polityka.pl [dostęp 2017-11-19] (pol.).
- ↑ Tomografia fotoakustyczna pomoże w leczeniu czerniaka - Badania i rozwój [online], www.rynekzdrowia.pl [dostęp 2017-11-19] (pol.).
