Przegrupowanie Hofmanna
Przegrupowanie Hofmanna, degradacja Hofmanna – reakcja chemiczna, w której pierwszorzędowe amidy ulegają przekształceniu do pierwszorzędowych amin o łańcuchu węglowym krótszym o jeden atom węgla[1][2][3]:
Nazwa reakcji pochodzi od nazwiska jej odkrywcy, Augusta Wilhelma von Hofmanna.
Mechanizm[edytuj | edytuj kod]
Mechanizm reakcji jest podobny do reakcji przegrupowania Curtiusa, z tą różnicą, że w przegrupowaniu Hofmanna izocyjaniany tworzą się z pierwszorzędowych amidów, nie zaś z azydków acylowych.
W reakcji bromu z wodorotlenkiem sodu powstaje in situ podbromin sodu (NaOBr), który przekształca pierwszorzędowy amid w odpowiedni izocyjanian jako produkt pośredni. Izocyjanian jest hydrolizowany do pierwszorzędowej aminy z wydzieleniem ditlenku węgla.
Odmiany[edytuj | edytuj kod]
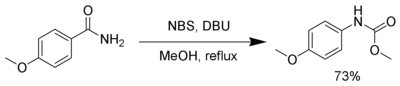
Brom jest niebezpieczny i przez to niewygodny w użyciu, można go zastąpić kilkoma substancjami. Przegrupowania Hofmanna można dokonać przy pomocy N-bromosukcynoimidu (NBS) i 1,8-diazabicyklo[5.4.0]undek-7-enu (DBU).
Produkt pośredni, izocyjanian, może zostać wyłapywany przez metanol tworząc karbaminian[4]:
W podobny sposób izocyjanian może zostać wyłapany przez tert-butanol tworząc Boc-aminę, tj. aminę podstawioną grupą tert-butoksykarbonylową.
Inną alternatywą dla bromu jest (bis(trifluoroacetoksy)jodo)benzen (CF
3COO)
2I−C
6H
5[5].
Zobacz też[edytuj | edytuj kod]
Przypisy[edytuj | edytuj kod]
- ↑ A.W. Hofmann, Ueber die Einwirkung des Broms in alkalischer Lösung auf Amide, „Berichte der Deutschen Chemischen Gesellschaft”, 14, 1881, s. 2725–2736, DOI: 10.1002/cber.188101402242 (niem.).
- ↑ Everett S. Wallis, John F. Lane, The Hofmann Reaction, „Organic Reactions”, 3, 1949, s. 267–306, DOI: 10.1002/0471264180.or003.07 (ang.).
- ↑ Takayuki Shioiri, Degradation Reactions, „Comprehensive Organic Synthesis”, 6, 1991, s. 795–828, DOI: 10.1016/B978-0-08-052349-1.00172-4 (ang.).
- ↑ Jeffrey W. Keillor, Xicai Huang, Methyl carbamate formation via modified Hofmann rearrangement reactions: methyl N-(p-methoxyphenyl)carbamate, „Organic Syntheses”, 78, 2002, s. 234, DOI: 10.15227/orgsyn.078.0234 (ang.).
- ↑ M.R. Almond i inni, Hofmann rearrangement under mildly acidic conditions using [I,I-bis(trifluoroacetoxy)]iodobenzene: cyclobutylamine hydrochloride from cyclobutanecarboxamide, „Organic Syntheses”, 66, 1988, s. 132, DOI: 10.15227/orgsyn.066.0132 (ang.).
Bibliografia[edytuj | edytuj kod]
- Jonathan Clayden i inni, Organic Chemistry, New York: Oxford University Press, 2007, s. 1073, ISBN 978-0-19-850346-0 (ang.).
- Louis F. Fieser, Mary Fieser, Advanced Organic Chemistry, New York: Reinhold Publishing Corporation, 1962, s. 499–501, LCCN 61-14594 (ang.).
- John McMurry, Chemia organiczna, t. 4, Warszawa: Wydawnictwo Naukowe PWN, 2003, s. 956–959, ISBN 83-01-14103-4.
- Robert T. Morison, Robert N. Boyd, Chemia organiczna, t. 2, Warszawa: Wydawnictwo Naukowe PWN, 1997, s. 88–94, ISBN 83-01-04166-8.