Cząsteczka
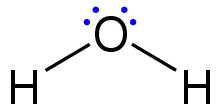


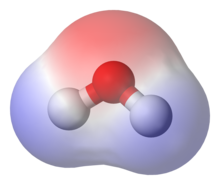
Cząsteczka, molekuła[1] – neutralna elektrycznie grupa dwóch lub więcej atomów utrzymywanych razem kowalencyjnym wiązaniem chemicznym[2][3].
Cząsteczki różnią się od innych cząstek chemicznych (np. jonów) brakiem ładunku elektrycznego – jednak w fizyce kwantowej, chemii organicznej i biochemii pojęcie cząsteczka jest zwyczajowo używane do określania jonów wieloatomowych[potrzebny przypis].
W teorii kinetycznej gazów pojęcie cząsteczka często jest używane do opisu gazowej cząstki bez względu na jej budowę. Według tej teorii gazy szlachetne składają się z cząsteczek, pomimo że składają się z pojedynczego, niezwiązanego wiązaniem chemicznym atomu[4].
Cząsteczka może się składać z atomów jednego pierwiastka, jak w przypadku tlenu (O2), lub różnych, czego przykładem jest woda (H2O). Atomy i struktury powiązane wiązaniem niekowalencyjnym (wodorowym, jonowym) ogólnie nie są uważane za pojedyncze cząsteczki.
Cząsteczki jako składniki materii są powszechne wśród substancji organicznych. Tworzą także większą część hydrosfery i atmosfery. Jednak większość znanych stałych substancji na Ziemi, włączając w to minerały tworzące skorupę, płaszcz i jądro Ziemi, zawiera wiele wiązań chemicznych, ale nie są one zbudowane z „rozpoznawalnych” cząsteczek. Do substancji zawierających struktury, dla których nie można wyróżnić pojedynczych cząsteczek, zaliczane są również kryształy jonowe (sole) i kryształy kowalencyjne (diament, kwarc, chlorek sodu). Układ powtarzających się jednostek-komórek-struktur występuje również w ciałach z wiązaniem metalicznym, co oznacza, że metale w postaci stałej także nie są zbudowane z cząsteczek. W szkłach (ciałach stałych posiadających bezpostaciową, nieuporządkowaną strukturę) atomy mogą być utrzymywane z sobą poprzez wiązania chemiczne, bez tworzenia jakiejkolwiek określonej cząsteczki oraz bez regularności powtarzających się jednostek (charakterystycznych dla kryształów).
Nauka
[edytuj | edytuj kod]Nauka o cząsteczkach jest nazywana chemią molekularną lub fizyką molekularną, w zależności od tego, czy skupia się na zagadnieniach związanych z chemią, czy fizyką. Chemia molekularna zajmuje się prawami rządzącymi oddziaływaniami między cząsteczkami, które wpływają na tworzenie lub rozpadanie się wiązań chemicznych, natomiast fizyka molekularna zajmuje się prawami rządzącymi ich strukturą i właściwościami. W rzeczywistości granica między nimi jest bardzo niewyraźna. W naukach molekularnych cząsteczka składa się ze stabilnego układu (stanu związanego) zawierającego dwa lub więcej atomów. Jony wieloatomowe są na ogół traktowane jako elektrycznie naładowane cząsteczki. Określenie cząsteczki niestabilne może odnosić się do bardzo dynamicznych układów cząsteczek, to znaczy krótkotrwałych zespołów elektronów i jąder (struktur rezonansowych), na przykład rodników, jonów cząsteczkowych, stanów przejściowych, lub układów zderzających się z sobą atomów, przykładowo kondensatu Bosego-Einsteina.
Rozmiary cząsteczek
[edytuj | edytuj kod]Większość cząsteczek jest zdecydowanie za mała, by można było je zobaczyć za pomocą metod optycznych – ale są wyjątki. makrocząsteczka DNA może osiągnąć rozmiary makroskopowe, tak jak inne cząsteczki polimerów. Guma znana z opon czy butów jest pojedynczą molekułą[5]. Cząsteczki powszechnie używane jako jednostki budulcowe syntezy organicznej mają wymiary od kilku do kilkudziesięciu Å. Niewielkie cząsteczki (poniżej 800 daltonów) mogą być obserwowane przy użyciu mikroskopii sił atomowych.
Najmniejszą cząsteczką jest dwuatomowa cząsteczka wodoru, H
2, o masie cząsteczkowej 2 Da (zawiera dwa protony i dwa elektrony), z długością wiązania 0,74 Å[6]. Z kolei w roku 2010 otrzymano największą wówczas cząsteczkę syntetyczną o zdefiniowanej strukturze, nazwaną PG5. Składa się ze sfunkcjonalizowanego łańcucha węglowodorowego, na którym zbudowano struktury dendrymeryczne. Cząsteczka ma długość ok. 1 μm i średnicę 10 nm. Zawiera ok. 17 mln atomów, a jej masa cząsteczkowa wynosi ok. 200 mln Da[7][8][9].
Spektroskopia cząsteczkowa
[edytuj | edytuj kod]Spektroskopia cząsteczkowa zajmuje się odpowiedzią cząsteczki oddziałującej z sygnałem próbkującym o znanej energii (lub częstotliwości, wg równania stałej Plancka). Cząsteczki posiadają skwantowane poziomy energetyczne, które mogą być analizowane przez wykrywanie wymiany energii cząsteczki poprzez absorbancję lub emisję[10].
Przypisy
[edytuj | edytuj kod]- ↑ molekularny, [w:] Słownik wyrazów obcych i zwrotów obcojęzycznych [zarchiwizowane z adresu 2007-06-21].
- ↑ Atoms, Molecules, and Ions, [w:] Steven S. Zumdahl, Susan A. Zumdahl, Chemistry, wyd. 8, Brooks Cole, 2010, s. 52, ISBN 0-547-12532-1 [dostęp 2021-08-25] (ang.).
- ↑ Erwin Boschmann, Molecules, [w:] J.J. Lagowski (red.), Chemistry. Foundations and applications, t. 3 K-Pl, Macmillan Reference USA, 2004, s. 114-119, ISBN 0-02-865724-1 (ang.).
- ↑ Monica Halka, Brian Nordstrom, Halogens and noble gases, 2010, s. 98, ISBN 978-0-8160-7368-9 [dostęp 2021-08-25] (ang.).
- ↑ One Big Happy Molecule [online], pslc.ws [dostęp 2019-04-08].
- ↑ Roger L. DeKock, Harry B. Gray, Chemical structure and bonding, University Science Books, 1989, s. 199, ISBN 0-935702-61-X [dostęp 2021-08-25] (ang.).
- ↑ The largest synthetic molecule [online], polychem.mat.ethz.ch [dostęp 2021-08-25] (ang.).
- ↑ Baozhong Zhang i inni, The largest synthetic structure with molecular precision: towards a molecular object, „Angewandte Chemie International Edition”, 50 (3), 2011, s. 737–740, DOI: 10.1002/anie.201005164, PMID: 21226166 [dostęp 2021-08-25] (ang.).
- ↑ Catarina Pietschmann: Giant molecule synthesized. Phys.Org, 2011-01-19. [dostęp 2013-01-24]. (ang.).
- ↑ Taras Plakhotnik, Absorption and coherent emission of single molecules, „Journal of Luminescence”, 98 (1-4), 2002, s. 57–62, DOI: 10.1016/S0022-2313(02)00252-1 (ang.).
