Wydzielanie
Wydzielanie – proces produkcji, modyfikacji i uwalniania substancji chemicznych z komórki lub gruczołu. W przeciwieństwie do wydalania, substancje te pełnią określoną funkcję, a nie są zbędnym produktem przemiany materii.
Klasyczny mechanizm wydzielania zachodzi przez struktury zwane porosomami[1].
Wydzielanie u prokariontów polega na transporcie lub translokacji cząsteczek (białek, enzymów, toksyn) z wnętrza komórki bakteryjnej na zewnątrz. Wydzielanie jest bardzo ważnym mechanizmem niezbędnym do funkcjonowania i adaptacji do warunków środowiska naturalnego.
Wydzielanie u eukariontów
[edytuj | edytuj kod]Wydzielanie może zachodzić na drodze:
Mechanizm klasyczny
[edytuj | edytuj kod]Komórki eukariotyczne, w tym ludzkie, mają bardzo rozwinięty proces wydzielania. Białka przeznaczone do wydzielenia są syntetyzowane przez rybosomy znajdujące się na powierzchni siateczki śródplazmatycznej. Zsyntetyzowane białka przemieszczane są do światła siateczki, gdzie są glikozylowane i ulegają zwijaniu. Białka nieprawidłowo sfałdowane są zazwyczaj transportowane z powrotem do cytozolu, gdzie są degradowane przez proteasomy. Pęcherzyki zawierające prawidłowo złożone białka są wprowadzane do aparatu Golgiego.
W aparacie Golgiego modyfikowana jest glikozylacja białek i następują dalsze modyfikacje potranslacyjne. Białka są następnie przenoszone do pęcherzyków transportujących, które przesuwają się wzdłuż cytoszkieletu do błony komórkowej. Kolejne zmiany mogą wystąpić w pęcherzykach wydzielniczych (tam proinsulina jest przekształcana w insulinę).
W końcu pęcherzyk ulega fuzji z błoną komórkową w miejscu zwanym porosomem, w procesie egzocytozy, wyrzucając swoją zawartość z komórki do jej środowiska[2].
Mechanizm nieklasyczny
[edytuj | edytuj kod]Istnieje wiele białek, takich jak FGF1 (aFGF), FGF2 (bFGF), interleukina 1 (IL-1) itp., które nie mają sekwencji sygnałowej. Nie korzystają one z klasycznej drogi siateczka śródplazmatyczna – aparat Golgiego. Są wydzielane różnymi nietypowymi drogami.
Zostały opisane co najmniej cztery nieklasyczne (niekonwencjonalne) metody wydzielania białek[3].
Wydzielanie w ludzkich tkankach
[edytuj | edytuj kod]Wiele typów ludzkich komórek ma zdolności wydzielnicze. Mają w tym celu dobrze rozwiniętą siateczkę śródplazmatyczną i aparat Golgiego. Wśród ludzkich tkanek produkujących wydzieliny są:
- przewód pokarmowy, wydzielający enzymy trawienne i sok żołądkowy
- płuca, wydzielające surfaktant
- gruczoły łojowe, wydzielające łój do natłuszczania skóry i włosów
- gruczoły tarczkowe, których wydzielina nawilża i chroni oko.
Wydzielanie u bakterii Gram-ujemnych
[edytuj | edytuj kod]Wydzielanie nie występuje tylko u eukariontów, ale jest także obecne u prokariontów i archeonów. Transportery ABC występują u wszystkich tych taksonów. Bakterie Gram-ujemne posiadają jednak dwie błony komórkowe, czyniąc mechanizmy wydzielania bardziej skomplikowanymi. Istnieje co najmniej sześć wyspecjalizowanych systemów wydzielniczych. Wiele z wydzielanych przez nie białek jest szczególnie ważnych w patogenezie bakterii.

System sekrecji typu I (T1SS/TOSS)
[edytuj | edytuj kod]Jest podobny do transportera ABC, ale posiada dodatkowe białka, które razem z białkiem ABC tworzą kanał przechodzący przez wewnętrzną i zewnętrzną błonę bakterii. T1SS wydziela różnorodne cząsteczki od jonów i białek różnych rozmiarów (20 – 900 kDa) po cząsteczki niebiałkowe (np. cykliczne β-glukany, polisacharydy).

System sekrecji typu II (T2SS)
[edytuj | edytuj kod]Białka wydzielane przez T2SS są transportowane do przestrzeni międzybłonowej przez system Sec lub Tat, skąd przechodzą przez zewnętrzną błonę dzięki polimerowemu (12–14 merów) kompleksowi białek. Od 10 do 15 innych białek błonowych wchodzi w skład T2SS, jednak ich funkcje nie zostały dotąd poznane.
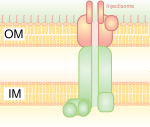
System sekrecji typu III (T3SS/TTSS)
[edytuj | edytuj kod]T3SS jest homologiczny do aparatu bazalnego znajdującego się u podstawy wici. Jest jak molekularna strzykawka, przez którą bakterie (np. pewne gatunki Salmonella, Shigella, Yersinia, Vibrio) mogą „wstrzykiwać” białka do komórek eukariotycznych. T3SS został po raz pierwszy odkryty u pałeczki dżumy, dzięki czemu udowodniono, że toksyny mogą być wprowadzane z cytoplazmy bakterii prosto do cytoplazmy komórki gospodarzowej, zamiast wydzielane do środowiska zewnętrznego, jak wcześniej sądzono[4].
System sekrecji typu IV (T4SS/TFSS)
[edytuj | edytuj kod]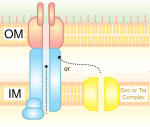
T4SS jest homologiczny do bakteryjnych pilusów koniugacyjnych. Jest głównym mechanizmem, dzięki któremu bakterie wydzielają i pochłaniają cząsteczki DNA lub białek. Precyzyjne działanie jego mechanizmu pozostaje nieznane. Został odkryty u Agrobacterium tumefaciens, która używa T4SS do wprowadzania plazmidu Ti do roślinnej komórki-gospodarza, co powoduje chorobę zwaną guzowatością korzeni. Helicobacter pylori używa T4SS do wprowadzania CagA do komórek nabłonkowych jelita, co jest wiązane z tworzeniem się raka żołądka[5]. Bordetella pertussis, bakteria powodująca krztusiec, wydziela toksyny przez T4SS. Legionella pneumophila, powodująca chorobę legionistów, korzysta ze zmodyfikowanego T4SS (T4BSS) do wprowadzania toksyn do komórek eukariotycznego gospodarza[6].
System sekrecji typu V (T5SS)
[edytuj | edytuj kod]
Również nazywany systemem autotransporterowym, T5SS wykorzystuje system Sec do przekroczenia wewnętrznej błony komórkowej. Białka przekraczające tę błonę mają zdolność fałdowania w ten sposób, że część ich łańcucha wystaje poza komórkę. Często wystająca część jest odcinana, co pozwala jej znaleźć się na zewnątrz komórki.
System sekrecji typu VI (T6SS)
[edytuj | edytuj kod]T6SS została odkryta w 2006 roku przez grupę Johna Mekelanosa z Harvard Medical School u Vibrio cholerae i Pseudomonas aeruginosa[7]. Wszystkie dotychczasowe odkrycia dotyczące T6SS można odnaleźć tutaj.
Wydzielanie u bakterii Gram-dodatnich
[edytuj | edytuj kod]Białka są syntetyzowane w cytoplazmie a następnie kierowane do konkretnej ścieżki transportowej prowadzącej do błony komórkowej. Podczas przechodzenia przez błonę białko jest poddawane obróbce i odpowiedniemu fałdowaniu. Gotowe białko jest zatrzymywane w środku komórki lub uwalniane na zewnątrz. Decydują o tym sekwencje sygnałowe przyłączające się do białka i kierujące je w odpowiednie miejsce.
Przypisy
[edytuj | edytuj kod]- ↑ Lee J.S., Jeremic A., Shin L., Cho W.J., Chen X., Jena B.P.. Neuronal porosome proteome: Molecular dynamics and architecture.. „J Proteomics”. 75 (13), s. 3952–62, 2012. PMID: 22659300.
- ↑ Anderson L.L.. Discovery of the 'porosome'; the universal secretory machinery in cells. „J. Cell. Mol. Med.”. 10 (1), s. 126–31, 2007. DOI: 10.1111/j.1582-4934.2006.tb00294.x. PMID: 16563225.
- ↑ Nickel W., Seedorf M.. Unconventional mechanisms of protein transport to the cell surface of eukaryotic cells. „Annu. Rev. Cell Dev. Biol.”. 24, s. 287–308, 2008.
- ↑ A.A. Salyers, D.D. Whitt: Bacterial Pathogenesis: A Molecular Approach. Wyd. 2. Washington, D.C.: ASM Press, 2002. ISBN 1-55581-171-X.
- ↑ Hatakeyama M., Higashi H.. Helicobacter pylori CagA: a new paradigm for bacterial carcinogenesis. „Cancer Science”. 96, s. 835–843, 2005. DOI: 10.1111/j.1349-7006.2005.00130.x. PMID: 16367902.
- ↑ Cascales E., Christie P.J.. The versatile Type IV secretion systems. „Nat. Rev. Microbiol.”. 1 (2), s. 137–149, 2003. DOI: 10.1038/nrmicro753. PMID: 15035043.
- ↑ Mougous J.D., Cuff M.E., Raunser S., Shen A., Zhou M., Gifford C.A., Goodman A.L., Joachimiak G., Ordoñez C.L., Lory S., Walz T., Joachimiak A., Mekalanos J.J.. A Virulence Locus of Pseudomonas aeruginosa Encodes a Protein Secretion Apparatus. „Science”. 312 (5779), s. 1526–30, 2006. DOI: 10.1126/science.1128393. PMID: 16763151. PMCID: PMC2800167.
