Równanie Clapeyrona (stan gazu doskonałego)
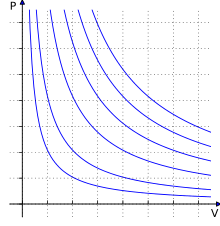
Równanie Clapeyrona, równanie stanu gazu doskonałego – równanie stanu opisujące związek pomiędzy temperaturą, ciśnieniem i objętością gazu doskonałego, a w sposób przybliżony opisujące gazy rzeczywiste. Sformułowane zostało w 1834 roku przez Benoît Clapeyrona[1]. Prawo to można wyrazić wzorem[2][3]:
gdzie[a]:
- – ciśnienie,
- – objętość,
- – objętość molowa,
- – liczba moli gazu, będąca miarą liczby jego cząsteczek;
- – temperatura (w kelwinach),
- – uniwersalna stała gazowa: gdzie: – stała Avogadra (liczba Avogadra), – stała Boltzmanna, = 8,314 J/(mol·K).
Równanie to jest wyprowadzane na podstawie założeń:
- gaz składa się z poruszających się cząsteczek;
- cząsteczki zderzają się ze sobą oraz ze ściankami naczynia, w którym się znajdują;
- nie ma oddziaływań międzycząsteczkowych w gazie, z wyjątkiem odpychania w momencie zderzeń cząsteczek;
- objętość (rozmiary) cząsteczek pomija się;
- zderzenia cząsteczek są doskonale sprężyste.

Równanie to, mimo że wyprowadzone w ramach wyidealizowanego modelu, dobrze opisuje większość substancji gazowych w obszarze ciśnień do ok. 100 atmosfer i temperatury do 300–400 °C, oraz w temperaturze trochę większej od temperatury skraplania gazu przy danym ciśnieniu.
Wyprowadzenie[edytuj | edytuj kod]
Równanie to można wyprowadzić fenomenologicznie (tj. bez odwoływania się do mikroskopowych właściwości układu). W wyniku wielu eksperymentów przeprowadzonych na gazach głównie w XVIII wieku badacze doszli do wniosku, że można w sposób satysfakcjonujący i wystarczający opisać te przemiany dla 1 mola gazu poprzez podanie 3 zmiennych np. Spośród tych trzech zmiennych tylko dwie są niezależne, wobec czego można traktować np. ciśnienie jako funkcję dwóch pozostałych zmiennych, tj. Można zatem zapisać różniczkę zupełną ciśnienia jako
Pierwszy człon opisuje proces, w którym gaz zamknięty w stałej objętości jest ogrzewany, czemu towarzyszy zmiana jego ciśnienia. Jako pierwszy taką przemianę opisał Jacques Alexandre Charles (prawo Charles’a) i podał jej równanie w postaci:
skąd wynika
Drugi człon to izotermiczne rozprężanie lub sprężanie gazu opisane przez Boyle’a i Mariotte’a (izotermiczna przemiana Boyle’a-Mariotte’a) wzorem
gdzie to stała. Z równania tego wynika, że
Otrzymane pochodne cząstkowe podstawmy do wyrażenia na
Dzieląc to równanie przez można rozdzielić zmienne
Po wycałkowaniu
Stałą całkowania można zapisać przy pomocy innej stałej
wówczas, ponieważ funkcja jest różnowartościowa, a to prowadzi do równania
Rozumowanie można uogólnić na dowolną liczbę moli gazu Równanie to stanowi fundamentalny związek między ciśnieniem, temperaturą i liczbą cząstek gazu, z którego wynikają trzy wnioski:
- moli (taka sama liczba cząstek) gazu, przy danej temperaturze i ciśnieniu panującym w naczyniu zajmuje zawsze taką samą objętość, niezależnie od budowy chemicznej tego gazu
- w danej objętości, przy danym ciśnieniu i temperaturze, znajduje się zawsze taka sama liczba moli cząsteczek gazu, niezależnie od jego budowy chemicznej
- moli gazu zamkniętych w naczyniu o określonej objętości, przy określonej temperaturze, będzie wywierało na jego ścianki takie samo ciśnienie, niezależnie od tego, jaki to jest gaz
Określenie równanie Clapeyrona nie jest stosowane powszechnie w odniesieniu do tego wzoru – w literaturze anglojęzycznej równanie to znane jest jedynie jako ideal gas law (prawo gazu doskonałego), podobnie jest w większości innych języków. W Rosji równanie to funkcjonuje pod nazwą równania Mendelejewa-Clapeyrona. Jako równanie Clapeyrona określana jest też zależność opisująca przemiany fazowe, m.in. ciecz-gaz. Pod tą nazwą często funkcjonuje też równanie Clausiusa-Clapeyrona.
Rozszerzeniami równania gazu doskonałego, uwzględniającymi objętość cząsteczek gazu oraz przyciąganie cząsteczek, są równanie van der Waalsa oraz wirialne równanie stanu.
Energia gazu[edytuj | edytuj kod]
Zgodnie z założeniami kinetycznej teorii gazów zakładaliśmy, że nie ma międzycząsteczkowych oddziaływań pomiędzy cząsteczkami gazu doskonałego. Innymi słowy, jego potencjalna energia wynosi zero. Stąd cała energia posiadana przez gaz jest energią kinetyczną:
Jest to energia kinetyczna jednego mola gazu.
| Energia gazu | Wzór matematyczny |
|---|---|
| energia związana z jednym molem gazu | |
| energia związana z jednym gramem gazu | |
| energia związana z jedną cząsteczką gazu |
Zobacz też[edytuj | edytuj kod]
- Przemiany termodynamiczne
- przemiana izobaryczna – (stałe ciśnienie )
- przemiana izotermiczna – (stała temperatura )
- przemiana izochoryczna – (stała objętość )
- przemiana adiabatyczna – (brak wymiany ciepła z otoczeniem )
- przemiana politropowa – ( gdzie – wykładnik politropy)
Uwagi[edytuj | edytuj kod]
- ↑ Zgodnie z zasadą obowiązującą w termodynamice chemicznej wielkie litery powinny być stosowane do oznaczania wielkości molowych (stąd – objętość molowa), a litery małe do innych wielkości (stąd – objętość).
Przypisy[edytuj | edytuj kod]
- ↑ Clapeyrona równanie, [w:] Encyklopedia PWN [dostęp 2021-10-08].
- ↑ Encyklopedia techniki. Chemia. Warszawa: WNT, 1965.
- ↑ Antoni Basiński, Bielański Adam, Kazimierz Gumiński i inni: Chemia fizyczna. Wyd. 3. Warszawa: Państwowe Wydawnictwo Naukowe, 1966, s. 297.
Linki zewnętrzne[edytuj | edytuj kod]
- applet Java obrazujący działanie przemian gazu doskonałego. walter-fendt.de. [zarchiwizowane z tego adresu (2007-10-23)].












































