Guanina
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||
| Wzór sumaryczny |
C5H5N5O | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
151,13 g/mol | ||||||||||||||||||||||
| Wygląd |
bezpostaciowy, biały lub prawie biały proszek[1] | ||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||
| DrugBank | |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||
Guanina – organiczny związek chemiczny z grupy puryn, jedna z pięciu zasad azotowych, wchodzących w skład podstawowych nukleotydów kwasów nukleinowych (DNA i RNA). W kwasach nukleinowych tworzy komplementarną parę z cytozyną (C).
Guanina to biała substancja krystaliczna nierozpuszczalna w wodzie. Formuje ona kryształy molekularne. Nazwa „guanina” pochodzi z wyodrębnienia tego związku z odchodów (guana) ptaków.
Historia[edytuj | edytuj kod]
Pierwszy raz związek został wyodrębniony w 1844 roku z odchodów morskich ptaków, nazywanych guanem[7]. Ponad 50 lat później Emil Fischer ustalił strukturę guanozyny, a następnie wykazał, że kwas moczowy może zostać łatwo przekształcony do guanozyny.
Właściwości[edytuj | edytuj kod]
Guanina, podobnie jak adenina i cytozyna, występuje zarówno w RNA, jak i DNA, podczas gdy tymina występuje głównie w DNA, a uracyl głównie w RNA. Ma ona dwie formy tautomeryczne – ketonową i enolową. Forma ketonowa jest dominująca, udział formy enolowej w populacji cząsteczek guaniny jest minimalny. W kwasach nukleinowych guanina poprzez trzy wiązania wodorowe formuje parę z cytozyną. W cząsteczce cytozyny grupa aminowa działa jako donor wodoru natomiast grupa karbonylowa przy węglu C2 i azot w pozycji 3 stanowią akceptory wodorów. Guanina posiada karbonylową grupę akceptorową przy węglu C6 oraz dwie grupy donorowe.
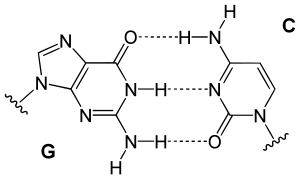
W środowisku silnych kwasów guanina rozkłada się do glicyny, amoniaku oraz tlenku węgla. Guanina jest bardziej podatna na utlenianie niż adenina. Wysoka temperatura topnienia (powyżej 350 °C) wynika z silnych oddziaływań międzycząsteczkowych pomiędzy grupami funkcyjnymi zawierającymi azot i tlen. Obecność tych oddziaływań tłumaczy także słabą rozpuszczalność w czystej wodzie. Dodatek kwasu lub zasady niszczy interakcje między cząsteczkami guaniny, zwiększając jej rozpuszczalność.
Przypisy[edytuj | edytuj kod]
- ↑ Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4.
- ↑ CRC Handbook of Chemistry and Physics, William M. Haynes (red.), wyd. 97, Boca Raton: CRC Press, 2016, s. 3-286, ISBN 978-1-4987-5429-3 (ang.).
- ↑ a b Guanine, [w:] ChemIDplus, United States National Library of Medicine [dostęp 2012-09-10] (ang.).
- ↑ a b Guanine, [w:] DrugBank, University of Alberta, DB02377 (ang.).
- ↑ Podręczny słownik chemiczny, Romuald Hassa (red.), Janusz Mrzigod (red.), Janusz Nowakowski (red.), Katowice: Videograf II, 2004, s. 155, ISBN 83-7183-240-0.
- ↑ Guanina (nr 51020) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2018-07-10]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ George H. Hitchings, Elvira A. Falco, The Identification of Guanine in Extracts of Girella Nigricans: The Specificity of Guanase, „Proceedings of the National Academy of Sciences of the United States of America”, 30 (10), 1944, s. 294–297, DOI: 10.1073/pnas.30.10.294, PMID: 16578130, PMCID: PMC1078714 [dostęp 2023-10-02] (ang.).


