Oksydaza ksantynowa

Czerwony: związany FAD, pomarańczowy: centrum żelazowo-siarkowe, żółty: molibdenopteryna z atomami molibdenu, niebieski: salicylan
Oksydaza ksantynowa – enzym (EC 1.17.3.2) z klasy oksydoreduktaz[2] katalizujący przekształcenie hipoksantyny w ksantynę oraz ksantyny w kwas moczowy. Enzym ten odgrywa kluczową rolę w metabolizmie puryn[3][4].
Oksydaza ksantynowa jest definiowana jako enzym o aktywności oksydazy (EC 1.17.3.2)[5]. To samo białko kodowane przez gen XDH może wykazywać aktywność dehydrogenazy ksantynowej (EC 1.17.1.4)[6]. Większość białka w wątrobie występuje w formie o aktywności dehydrogenazy ksantynowej, jednak może być ono przemienione w oksydazę ksantynową poprzez odwracalne utlenienie grup sulfhydrylowych (−SH) lub nieodwracalne modyfikacje proteolityczne[7][8].
Katalizowane reakcje[edytuj | edytuj kod]
Przy udziale oksydazy ksantynowej katalizowane są następujące reakcje:
Oksydaza ksantynowa może również katalizować przemiany niektórych puryn, pteryn oraz aldehydów, np. efektywnie katalizuje przemianę 1-metyloksantyny (metabolitu kofeiny) do kwasu 1-metylomoczowego; natomiast wobec 3-metyloksantyny wykazuje niewielką aktywność katalityczną[9].
W niektórych okolicznościach może umożliwić wytworzenie jonu nadtlenkowego[6]:
- RH + H2O + 2O2 ⇌ ROH + 2O2− + 2H+.
- Struktury puryny i jej pochodnych tlenowych
-
puryna (nie zawiera atomów tlenu)
-
hipoksantyna (zawiera jeden atom tlenu)
-
ksantyna (zawiera dwa atomy tlenu)
-
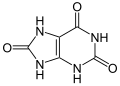
kwas moczowy (zawiera trzy atomy tlenu)
Inne reakcje[edytuj | edytuj kod]

Ponieważ oksydaza ksantynowa jest enzymem wytwarzającym nadtlenki o ogólnej niskiej swoistości[10], więc może łączyć z innymi związkami oraz enzymami i tworzyć reaktywne utleniacze, a także utleniać substraty.
Początkowo sugerowano, że bydlęca oksydaza ksantynowa (z mleka) posiada miejsce wiążące do redukcji cytochromu c. Jednak teraz wiadomo, że za mechanizm redukcyjny cytochromu c odpowiada produkt uboczny działania oksydazy ksantynowej anionorodnik ponadtlenkowy (O2–•), konkurencyjnie hamowany przez anhydrazę węglanową[11].
Kolejną reakcją katalizowaną przez oksydazę ksantynową jest rozkład S-nitrozotioli, RSNO (reaktywnej formy azotu) do tlenku azotu (NO), który reaguje z anionorodnikiem ponadtlenkowym tworząc w warunkach tlenowych nadtlenoazotyn (ONOO-)[12].
W wyniku utleniania aldehydu octowego w obecności katalazy i wodorowęglanu, oksydaza ksantynowa wytwarza anionorodnik węglanowy (CO3-•) będący silnym utleniaczem jednoelektronowym. Sugeruje się, że anionorodnik węglanowy jest wytwarzany w jednym z centrów redoks enzymu przy udziale nadtlenowęglanu[10].
Struktura[edytuj | edytuj kod]
Jest to duże białko o masie cząsteczkowej 270 kDa zawierające dwie grupy flawinowe (związane jako FAD), 2 atomy molibdenu i 8 atomów żelaza w jednostce enzymatycznej. Atomy molibdenu są zawarte w kofaktorach - molibdenopterynach, które stanowią centrum aktywne enzymu. Atomy żelaza są częścią centrum żelazowo-siarkowego ferrodoksyny [2Fe-2S] i biorą udział w reakcjach przeniesienia elektronów.
Mechanizm katalityczny[edytuj | edytuj kod]
Miejsce aktywne oksydazy ksantynowej jest zbudowane z molibdenopteryny (zawierającej atom molibdenu); jest regulowane przez terminalny atom tlenu, atomy siarki oraz terminalny jon wodorotlenowy[13]. W reakcji wytworzenia kwasu moczowego z ksantyny atom tlenu jest przenoszony z molibdenu na ksantynę (w reakcji tej biorą udział kofaktory)[14]. Przekształcenie do formy wyjściowej centrum aktywnego molibdenopteryny wymaga udziału wody. Jak w przypadku innych oksydoreduktaz zawierających molibden, atom tlenu włączany do substratu przez oksydazę ksantynową pochodzi raczej z wody niż z cząsteczki tlenu.
Znaczenie kliniczne[edytuj | edytuj kod]
Oksydaza ksantynowa jest enzymem wytwarzającym nadtlenki. Stwierdzono wzrost jej aktywności w surowicy krwi oraz w płucach podczas infekcji wirusem grypy typu A, co prowadzi do szkodliwego wzrostu stężenia nadtlenków[15].
Podczas ciężkiego uszkodzenia wątroby dochodzi do uwolnienia oksydazy ksantynowej do krwiobiegu, w związku z tym badanie oznaczające stężenie oksydazy ksantynowej może pozwolić na ocenę stanu wątroby[16].
W związku z tym, że oksydaza ksantynowa należy do enzymów szlaku metabolicznego, w wyniku działania którego wytwarzany jest kwas moczowy, jej inhibitor, allopurynol, jest lekiem stosowanym w leczeniu dny moczanowej - schorzenia w któremu towarzyszy hiperurykemia. Ponieważ oksydaza ksantynowa jest zaangażowana również w metabolizm 6-merkaptopuryny, należy zachować szczególną ostrożność przy jednoczesnym stosowaniu allopurynolu oraz 6-merkaptopuryny (lub jej proleku, azatiopryny).
Ksantynuria jest rzadką chorobą genetyczną, w której brak oksydazy ksantynowej prowadzi do wysokiego stężenia ksantyny we krwi, czego następstwem mogą być problemy zdrowotne takie jak niewydolność nerek. Nie ma swoistego leczenia tej choroby. Lekarze zalecają chorym unikanie produktów z wysoką zawartością puryn w diecie oraz przyjmowanie dużej ilości płynów. Za ksantynurię typu I odpowiadają bezpośrednio mutacje w genie XDH, który wpływa na aktywność oksydazy ksantynowej. Ksantynuria typu II może być wynikiem niewydolnego mechanizmu, który odpowiada za "wstawianie" atomu siarki w miejsca aktywne oksydazy ksantynowej i oksydazy aldehydowej (pokrewnego enzymu wykazującego podobną aktywność (np. przy konwersji allopurynolu do oksypurynolu)[17].
Sugeruje się, że inhibicja oksydazy ksantynowej może być dobrym mechanizmem pozwalającym na poprawę stanu zdrowia układu krwionośnego[18]. U pacjentów z przewlekłą obturacyjną chorobą płuc (POChP), którzy stosują allopurynol w celu zahamowania oksydazy ksantynowej obserwuje się spadek poziomu stresu oksydacyjnego, oksydacji glutationu oraz peroksydacji lipidów[19]. Stres oksydacyjny może być spowodowany przez wolne rodniki hydroksylowe i nadtlenek wodoru, które są produktami ubocznymi aktywności oksydazy ksantynowej[20].
Podwyższone stężenie kwasu moczowego w surowicy może być wskaźnikiem stanu zdrowia układu krwionośnego. Wykazano, że jest ono silnym czynnikiem predykcyjnym śmiertelności i konieczności przeszczepu serca[18]. Źródła tej zależności nie są jasne[21]. Typowymi przyczynami wysokiego stężenia kwasu moczowego w surowicy jest stan wzmożonego podziału komórek oraz przyjmowanie alkoholu[20].
Potwierdzono, że reaktywne formy azotu, takie jak nadtlenoazotyn (ONOO-), które mogą być wytwarzane przy współudziale oksydazy ksantynowej, reagują z DNA i białkami, powodując uszkodzenia komórek lub nawet wykazując toksyczność. Wykazano, że szlaki sygnałowe reaktywnych form azotu i reaktywnych form tlenu odgrywają kluczową rolę w funkcjonowaniu mięśnia sercowego oraz naczyń krwionośnych. Wyjaśnia to potrzebę badań oksydazy ksantynowej w ocenie stanu zdrowia układu krwionośnego[22].
Stwierdzono obecność zarówno oksydazy ksantynowej, jak i oksydoreduktazy ksantynowej w nabłonku oraz śródbłonku rogówki. Sugeruje się, że mogą być one zaangażowane w uszkodzenia oksydacyjne oka[23].
Inhibitory[edytuj | edytuj kod]
Inhibitorami oksydazy ksantynowej są allopurynol[24], oksypurynol[25] i kwas fitowy[26]. Wykazano, że oksydaza ksantynowa jest hamowana również przez flawonoidy[27], na tej podstawie swoje zastosowanie znalazły liście bugenwilli okazałej (Bougainvillea spectabilis Wild) (z rodzaju bugenwilli) (o wartości połowy maksymalnego stężenia hamującego (IC50) równej 7,23 μM), tradycyjnie stosowane w medycynie ludowej[28].
Przypisy[edytuj | edytuj kod]
- ↑ Enroth C, Eger BT, Okamoto K, Nishino T, Nishino T, Pai EF. Crystal structures of bovine milk xanthine dehydrogenase and xanthine oxidase: structure-based mechanism of conversion. „Proc. Natl. Acad. Sci. U.S.A.”. 97 (20), s. 10723–8, wrzesień 2000. DOI: 10.1073/pnas.97.20.10723. PMID: 11005854. PMCID: PMC27090.
- ↑ Ardan T, Kovaceva J, Cejková J. Comparative histochemical and immunohistochemical study on xanthine oxidoreductase/xanthine oxidase in mammalian corneal epithelium. „Acta Histochem”. 106 (1), s. 69–75, 2004. DOI: 10.1016/j.acthis.2003.08.001. PMID: 15032331.
- ↑ Hille R. Molybdenum-containing hydroxylases. „Arch. Biochem. Biophys.”. 433 (1), s. 107–116, 2005. DOI: 10.1016/j.abb.2004.08.012. PMID: 15581570.
- ↑ Harrison R. Structure and function of xanthine oxidoreductase: where are we now?. „Free Radic. Biol. Med.”. 33 (6), s. 774–97, 2002. DOI: 10.1016/S0891-5849(02)00956-5. PMID: 12208366.
- ↑ KEGG record for EC 1.17.3.2.
- ↑ a b KEGG record for EC 1.17.1.4.
- ↑ Entrez Gene: XDH xanthine dehydrogenase.
- ↑ *607633 Xanthine dehydrogenase; XDH.
- ↑ D. J. Birkett i wsp.. 1-Methylxanthine derived from caffeine as a pharmacodynamic probe of oxypurinol effect. „Br J Clin Pharmacol”. 43 (2), s. 197–200, 1997. PMID: 9131954. PMCID: PMC2042732.
- ↑ a b MG. Bonini, S. Miyamoto, P. Di Mascio, O. Augusto. Production of the carbonate radical anion during xanthine oxidase turnover in the presence of bicarbonate. „J Biol Chem”. 279 (50), s. 51836-51843, 2004. DOI: 10.1074/jbc.M406929200. PMID: 15448145.
- ↑ JM. McCord, I. Fridovich. The reduction of cytochrome c by milk xanthine oxidase. „J Biol Chem”. 243 (21), s. 5753-5760, 1968. PMID: 4972775.
- ↑ M. Trujillo. Xanthine Oxidase-mediated Decomposition of S-Nitrosothiols. „Journal of Biological Chemistry”. 273 (14), s. 7828–7834, 1998. DOI: 10.1074/jbc.273.14.7828.
- ↑ Hille R.. Structure and Function of Xanthine Oxidoreductase. „European Journal of Inorganic Chemistry”. 2006 (10), s. 1905–2095, 2006. DOI: 10.1002/ejic.200600087.
- ↑ Metz S, Thiel W.. A Combined QM/MM Study on the Reductive Half-Reaction of Xanthine Oxidase: Substrate Orientation and Mechanism. „Journal of the American Chemical Society”. 131 (41), s. 14885–14902, 2009. DOI: 10.1021/ja9045394. PMID: 19788181.
- ↑ Hemila, H. Vitamin C and the common cold. „British Journal of Nutrition”. 67 (1), s. 3-16, 1992. DOI: 10.1079/BJN19920004.
- ↑ MG. Battelli, S. Musiani, M. Valgimigli, L. Gramantieri i inni. Serum xanthine oxidase in human liver disease. „Am J Gastroenterol”. 96 (4), s. 1194-1199, 2001. DOI: 10.1111/j.1572-0241.2001.03700.x. PMID: 11316169.
- ↑ OMIM: Xanthinuria type II.
- ↑ a b Dawson J, Walters M. Uric acid and xanthine oxidase: future therapeutic targets in the prevention of cardiovascular disease?. „British Journal of Clinical Pharmacology”. 62 (6), s. 633, 2006. DOI: 10.1111/j.1365-2125.2006.02785.x. PMID: 21894646. PMCID: PMC1885190.
- ↑ LM Heunks, Viña, J; van Herwaarden, CL; Folgering, HT; Gimeno, A; Dekhuijzen, PN. Xanthine oxidase is involved in exercise-induced oxidative stress in chronic obstructive pulmonary disease. „The American journal of physiology”. 277 (6), s. R1697-R1704, 1999. PMID: 10600916.
- ↑ a b Peter Higgins, Dawson, Jesse; Walters, Matthew. The Potential for Xanthine Oxidase Inhibition in the Prevention and Treatment of Cardiovascular and Cerebrovascular Disease. „Cardiovascular Psychiatry and Neurology”. 2009, s. 1–9, 2009. DOI: 10.1155/2009/282059.
- ↑ J Dawson, Quinn, T; Walters, M. Uric acid reduction: a new paradigm in the management of cardiovascular risk?. „Current medicinal chemistry”. 14 (17), s. 1879–86, 2007. DOI: 10.2174/092986707781058797. PMID: 17627523.
- ↑ J. M. Zimmet, Hare, J. M.. Nitroso-Redox Interactions in the Cardiovascular System. „Circulation”. 114 (14), s. 1531–1544, 3 października 2006. DOI: 10.1161/CIRCULATIONAHA.105.605519.
- ↑ Cejková J, Ardan T, Filipec M, Midelfart A. Xanthine oxidoreductase and xanthine oxidase in human cornea. „Histol. Histopathol.”. 17 (3), s. 755–760, 2002. PMID: 12168784. [zarchiwizowane z adresu].
- ↑ Pacher P, Nivorozhkin A, Szabó C. Therapeutic effects of xanthine oxidase inhibitors: renaissance half a century after the discovery of allopurynol. „Pharmacol. Rev.”. 58 (1), s. 87–114, 2006. DOI: 10.1124/pr.58.1.6. PMID: 16507884. PMCID: PMC2233605.
- ↑ Spector T. Oxypurinol as an inhibitor of xanthine oxidase-catalyzed production of superoxide radical. „Biochem. Pharmacol.”. 37 (2), s. 349–52, 1988. DOI: 10.1016/0006-2952(88)90739-3. PMID: 2829916.
- ↑ S. Muraoka, T. Miura. Inhibition of xanthine oxidase by phytic acid and its antioxidative action. „Life Sci”. 74 (13), s. 1691-700, 2004. DOI: 10.1016/j.lfs.2003.09.040. PMID: 14738912.
- ↑ Paul Cos, Ying, Li; Calomme, Mario; Hu, Jia P.; Cimanga, Kanyanga; Van Poel, Bart; Pieters, Luc; Vlietinck, Arnold J.; Berghe, Dirk Vanden. Structure−Activity Relationship and Classification of Flavonoids as Inhibitors of Xanthine Oxidase and Superoxide Scavengers. „Journal of Natural Products”. 61 (1), s. 71–76, 1998. DOI: 10.1021/np970237h.
- ↑ WS Chang, Lee, YJ; Lu, FJ; Chiang, HC. Inhibitory effects of flavonoids on xanthine oxidase. „Anticancer research”. 13 (6A), s. 2165–2170, 1993. PMID: 8297130.