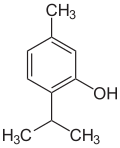
Tymol
| |||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
C10H14O | ||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
150,22 g/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd |
bezbarwne, krystaliczne ciało stałe | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||||||||||||
Tymol (2-izopropylo-5-metylofenol) – organiczny związek chemiczny z grupy terpenoidów i fenoli. Jest obok swojego izomeru karwakrolu składnikiem olejków eterycznych występujących w macierzance (tymianku), lebiodce (oregano) i cząbrze. Tworzy bezbarwne kryształy o charakterystycznym silnym zapachu macierzanki.
Historia[edytuj | edytuj kod]
W starożytnym Egipcie tymol i karwakrol były używane ze względu na ich właściwości bakterio- i grzybobójcze stosowane przy mumifikacji.
Tymol w postaci krystalicznej został odkryty w roku 1719 przez Caspara Neumanna, a w roku 1842 opisany na podstawie analizy elementarnej przez M. Lallemanda, który w sposób prawidłowy przedstawił stosunek węgla, wodoru i tlenu w tymolu. Analiza krystalograficzna z dokładnym określeniem pozycji atomów została wykonana dopiero w roku 1980[8].
Właściwości[edytuj | edytuj kod]
Ciśnienie pary nasyconej wynosi 2,5 hPa przy 25 °C.
Tymol jako derywat fenolu ma właściwości typowe dla fenolu. Jest trudno wchłaniany z przewodu pokarmowego, dlatego stosowany był jako środek przeciw robaczycy, a także do odkażania błon śluzowych. Jest silną trucizną komórkową. Uszkadza wątrobę, nerki, serce i ośrodkowy układ nerwowy.
Otrzymywanie[edytuj | edytuj kod]
Jedną z metod otrzymywania jest reakcja m-krezolu i propenu. Proces został opracowany w roku 1927 przez Karla Schoellkopfa z firmy Rheinische Kampfer Fabrik. Reakcję prowadzi się w obecności katalizatorów kwasowych w temperaturze 170–230 °C[9].
Zastosowanie[edytuj | edytuj kod]
Tymol jest stosowany jako środek dezynfekujący. W pszczelarstwie znajduje zastosowanie do zwalczania warrozy.
Zastosowania medyczne[edytuj | edytuj kod]
Dawniej tymol stosowany był jako środek przeciwpasożytniczy[10]. Współczesne badania na myszach wskazują, że tymol może być skutecznym środkiem w bąblowicy, samodzielnie lub w połączeniu z albendazolem, prowadząc do istotnej redukcji protoskoleksu w cystach tasiemca. Po analizie poziomów enzymów ALP GOT oraz GPT po leczeniu wykazano, że tymol nie działał toksycznie na komórki myszy[11].
Tymol i jego pochodne badane są także jako środki przeciw kandydozie jamy ustnej[12].
Olejki eteryczne zawierające duże stężenia tymolu (m.in. Thymbra capitata, Thymus zigis) badano pod kątem potencjalnej skuteczności przeciw giardozie. Olejki w stężeniu 71–257 µg/ml w ciągu godziny zabijały prawie 50% badanej populacji lamblii. Nie stwierdzono ich cytotoksyczności dla komórek ssaków[13].
Przypisy[edytuj | edytuj kod]
- ↑ a b c d e Haynes 2014 ↓, s. 3-514.
- ↑ a b Thymol, [w:] DrugBank, University of Alberta, DB02513 (ang.).
- ↑ a b Tymol, [w:] ChemIDplus, United States National Library of Medicine [dostęp 2016-08-14] (ang.).
- ↑ a b c Haynes 2014 ↓, s. 6-73.
- ↑ a b Tymol, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2016-08-14] (ang.).
- ↑ a b c Thymol (nr T0501) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2016-08-14]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Tymol (nr T0501) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2016-08-14]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Thozet, A., Perrin, M. Structure of 2-isopropyl-5-methylphenol (thymol). „Acta Cryst. B”. 36 (6), s. 1444–1447, 1980. DOI: 10.1107/S0567740880006243.
- ↑ Karl Schoellkopf: Verfahren zur Herstellung O- oder C-propylierter (isopropylierter) Kresole. Patent DE586150. Rheinische Kampfer Fabrik, 1927. [dostęp 2015-08-09].
- ↑ Tymol – thymolum « Medycyna dawna i współczesna. rozanski.li. [dostęp 2015-08-09].
- ↑ C.M. Albani, P.E. Pensel, N. Elissondo, G. Gambino i inni. In vivo activity of albendazole in combination with thymol against Echinococcus multilocularis. „Vet Parasitol”. [w druku], 2015. DOI: 10.1016/j.vetpar.2015.06.030. PMID: 26190130.
- ↑ G.S. Labib, H. Aldawsari. Innovation of natural essential oil-loaded Orabase for local treatment of oral candidiasis. „Drug Des Devel Ther”. 9, s. 3349–3359, 2015. DOI: 10.2147/DDDT.S85356. PMID: 26170621.}
- ↑ S. Pérez G., M. A. Ramos-López, E. Sánchez-Miranda, M. C. Fresán-Orozco, J. Pérez-Ramos. Antiprotozoa activity of some essential oils. „Journal of Medicinal Plants Research”. 6 (15), s. 2901–2908, 2012. DOI: 10.5897/JMPR11.1572.
Bibliografia[edytuj | edytuj kod]
- CRC Handbook of Chemistry and Physics, William M. Haynes (red.), wyd. 95, Boca Raton: CRC Press, 2014, ISBN 978-1-4822-0867-2 (ang.).