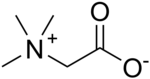
N,N,N-Trimetyloglicyna
| |||||||||||||||
| |||||||||||||||
| Ogólne informacje | |||||||||||||||
| Wzór sumaryczny |
C5H11NO2 | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
117,15 g/mol | ||||||||||||||
| Wygląd |
ciało stałe o słodkim smaku z metalicznym posmakiem, chlorowodorek betainy ma kwaśny smak | ||||||||||||||
| Identyfikacja | |||||||||||||||
| Numer CAS | |||||||||||||||
| PubChem | |||||||||||||||
| DrugBank | |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Podobne związki | |||||||||||||||
| Podobne związki | |||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||
N,N,N-Trimetyloglicyna, TMG, betaina, (CH
3)
3N+
CH
2CO−
2 – organiczny związek chemiczny z grupy betain, pochodna aminokwasu glicyny. Wykryta została po raz pierwszy w burakach cukrowych Beta vulgaris w XIX w. (stąd nazwa betaina). Z czasem określenie betainy rozszerzyło swoje znaczenie na całą klasę związków tego typu[3], a samą trimetyloglicynę wyróżnia się nazwą betaina glicynowa. Jest produktem ubocznym przemysłu cukrowniczego. Izoluje się ją za pomocą krystalizacji w formie chlorowodorku.
Struktura i reakcje[edytuj | edytuj kod]
Trimetyloglicyna jest czwartorzędową solą amoniową występującą jako jon obojnaczy (zwitterjon)[3], czyli związek posiadający jednocześnie fragment anionowy oraz kationowy, w szerokim zakresie pH. Mocne kwasy (np. HCl, HNO
3, H
2SO
4, HBF
4) przekształcają TMG w odpowiednie sole, np. reakcja z HCl daje chlorowodorek betainy[4]:
- (CH
3)
3N+
CH
2CO−
2 + HCl → [(CH
3)
3N+
CH
2COOH]Cl−
Stała dysocjacji formy sprotonowanej (CH
3)
3N+
CH
2COOH, wynosi 0,02 (pKa = 1,68)[1].
Otrzymywanie[edytuj | edytuj kod]
Betainę otrzymuje się z produktów spożywczych w formie właściwej betainy lub pokrewnego związku, choliny ([HOCH
2CH
2N+
(CH
3)
3]X−
). Szczególnie wysoką zawartość betainy bądź choliny mają pszenica, szpinak, buraki cukrowe, a także skorupiaki.
Fizjologia[edytuj | edytuj kod]
Betaina ma trzy poznane funkcje fizjologiczne u ssaków:
- Jest organicznym osmolitem akumulującym się w komórkach nerkowych dla zbalansowania hipertoniczności zewnątrzkomórkowej.
- Działa jako szaperon stabilizujący strukturę białek w warunkach denaturujących.
- Służy jako donor grup metylowych podczas syntezy metioniny z homocysteiny, sama przekształcając się przy tym w dimetyloglicynę[5].
Cholina jest przekształcana w betainę w wątrobie i nerkach w dwuetapowym procesie enzymatycznym. W pierwszym etapie reszta alkoholowa choliny utleniana jest do aldehydu przez mitochondrialną oksydazę cholinową (dehydrogenazę cholinową, EC 1.1.99.1). Aldehyd betainowy utleniany jest następnie do betainy w mitochondriach lub cytoplazmie przez dehydrogenazę aldehydu betainowego (EC 1.1.1.8).
Zastosowania[edytuj | edytuj kod]
Medycyna[edytuj | edytuj kod]
Betaina stosowana jest w leczeniu wysokiego poziomu homocysteiny (hiperhomocysteinemii)[6]. Chlorowodorek betainy stosowany jest jako środek wspomagający trawienie, szczególnie skuteczny u osób z niedostatecznym wytwarzaniem kwasu solnego w żołądku.
Hodowla zwierząt[edytuj | edytuj kod]
W kombinacji z lizyną zużywana jest w ilościach tonowych jako dodatek do paszy zwierząt rzeźnych, przyspieszający przyrost masy mięśni. W hodowlach łososi stosowana jest jako środek obniżający ciśnienie osmotyczne komórek podczas przenoszenia zwierząt z wody słodkiej do słonej.
Biologia molekularna[edytuj | edytuj kod]
Betaina stosowana jest jako związek wspomagający w reakcji łańcuchowej polimerazy (PCR) i innych reakcjach opartych o polimeryzację DNA, np. sekwencjonowanie DNA. Jest to związek izostabilizujący, wyrównujący temperatury topnienia DNA wynikające z różnej trwałości par GC i AT[7].
Suplementacja sportowa[edytuj | edytuj kod]
Betaina jest wykorzystywana jako suplement zapobiegający odwodnieniu podczas długich treningów. Stosuje się ją w sportach wytrzymałościowych i siłowych, jako komponent odżywek przedtreningowych[8][niewiarygodne źródło?].
Przypisy[edytuj | edytuj kod]
- ↑ a b Edwin Chrystiuk i inni, Rate and equilibrium studies of the reaction of oxyanions with 2-phenyloxazol-5(4H)-one, „Journal of the Chemical Society, Perkin Transactions 2” (1), 1986, s. 163, DOI: 10.1039/p29860000163 (ang.).
- ↑ a b Betaine, karta charakterystyki produktu Sigma-Aldrich, Merck, 27 kwietnia 2022, numer katalogowy: 61962 [dostęp 2022-12-14]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ a b betaines, [w:] A.D. McNaught, A. Wilkinson, Compendium of Chemical Terminology (Gold Book), S.J. Chalk (akt.), International Union of Pure and Applied Chemistry, wyd. 2, Oxford: Blackwell Scientific Publications, 1997, DOI: 10.1351/goldbook.B00637, ISBN 0-9678550-9-8 (ang.).
- ↑ Cinzia Chiappe, Sunita Rajamani, Felicia D’Andrea, A dramatic effect of the ionic liquid structure in esterification reactions in protic ionic media, „Green Chemistry”, 15 (1), 2013, s. 137–143, DOI: 10.1039/C2GC35941C (ang.).
- ↑ J.A. Muntz, The inability of choline to transfer a methyl group directly to homocysteine for methionine formation, „Journal of Biological Chemistry”, 182 (2), 1950, s. 489–499, DOI: 10.1016/S0021-9258(18)56483-8 (ang.).
- ↑ Pål I. Holm i inni, Betaine and folate status as cooperative determinants of plasma homocysteine in humans, „Arteriosclerosis, Thrombosis, and Vascular Biology”, 25 (2), 2005, s. 379–385, DOI: 10.1161/01.ATV.0000151283.33976.e6, PMID: 15550695 (ang.).
- ↑ W.A. Rees i inni, Betaine can eliminate the base pair composition dependence of DNA melting, „Biochemistry”, 32 (1), 1993, s. 137–144, DOI: 10.1021/bi00052a019, PMID: 8418834 (ang.).
- ↑ Betaina – co to jest, co daje i jak ją stosować? [online], e-figura.pl, 30 maja 2022 [dostęp 2022-06-02].
Linki zewnętrzne[edytuj | edytuj kod]
- Juliette C. Howe, Juhi R. Williams, Joanne M. Holden, USDA Database for the Choline Content of Common Foods, U.S. Department of Agriculture, 2004 [zarchiwizowane z adresu 2009-01-31] (ang.).