Zespół Lescha-Nyhana
| |
| Klasyfikacje | |
| ICD-10 | |
|---|---|
Zespół Lescha-Nyhana[a] (LNS z ang. Lesch-Nyhan syndrome) – dziedziczne zaburzenie spowodowane całkowitym lub prawie całkowitym niedoborem fosforybozylotransferazy hipoksantynowo-guaninowej (HGPRT, z ang. hypoxanthine-guanine phosphoribosyl transferase). Częściowy spadek aktywności enzymu (nie mniej niż 8% normalnej aktywności HGPRT) nie powoduje objawów neurologicznych i określany jest jako zespół Kelleya-Seegmillera[1][2]; jego jedynym objawem jest kamica nerkowa.
Historia[edytuj | edytuj kod]
Schorzenie zostało po raz pierwszy opisane w 1964 roku przez studenta medycyny Michaela Lescha i lekarza pediatrę Williama Nyhana u dwóch braci w wieku 4 i 8 lat, prezentujących charakterystyczne objawy neurologiczne i hiperurykemię[3]. Prawdopodobnie zespół Lescha-Nyhana był opisany już wcześniej, w 1959 roku, przez niemieckich lekarzy Wernera Catela i J. Schmidta[4]. Przypadek opisany przez Niemców 18-miesięcznego dziecka z hiperurykemią, hiperurykozurią i encefalopatią nie został przez nich opisany jako nowa jednostka chorobowa. Metaboliczną przyczynę zespołu wyjaśnił zespół Jarvisa Edwina Seegmillera w 1967 roku[5].
Epidemiologia[edytuj | edytuj kod]
Zespół Lescha-Nyhana występuje rzadko, dotykając około jedną osobę na 380 tys. żywych urodzeń[6].
Etiologia[edytuj | edytuj kod]
Choroba jest związana z mutacją w genie HPRT1 na chromosomie X w locus Xq26-q27.2 kodującym białko fosforybozylotransferazy hipoksantynowo-guaninowej (EC 2.4.2.8). Kobiety są bezobjawowymi nosicielkami mutacji: na drugiej kopii chromosomu X mają prawidłową kopię genu HPRT, co chroni je przed rozwinięciem się choroby, chociaż mogą mieć zwiększone ryzyko hiperurykemii. Chorują mężczyźni posiadający tylko jeden chromosom X ze zmutowaną kopią genu. 50% męskiego potomstwa kobiet będących heterozygotami względem zmutowanego genu HGPRT otrzymuje tę kopię genu i rozwija objawy zespołu. Choroba nie pozwala dotkniętym mężczyznom mieć potomstwa; jednak w przypadku poronnych postaci schorzenia wszystkie córki chorego z LNS są nosicielkami mutacji i żaden syn nie posiada kopii uszkodzonego genu. Około 50% mutacji powstaje de novo. Częstość mutacji de novo wzrasta w z wiekiem matki, jak w wielu innych sprzężonych z chromosomem X chorobach genetycznych[7].
Patofizjologia[edytuj | edytuj kod]
Do syntezy DNA (podczas podziałów komórkowych) potrzebne są nukleotydy, cząsteczki budujące DNA. Puryny (adenina i guanina) oraz pirymidyny (tymina i cytozyna) są związane z deoksyrybozą i resztą kwasu ortofosforowego i w razie potrzeby włączane do DNA (zobacz: Replikacja DNA). Zwykle nukleotydy są syntetyzowane de novo z aminokwasów i innych prekursorów. Oprócz tego mała ich część jest wytwarzana z produktów rozpadu nukleotydów (nukleozydów oraz zasad purynowych i pirymidynowych) za pośrednictwem ścieżek metabolicznych noszących nazwę reakcji rezerwowych (reakcje reutylizacji, reakcje Salvage, szlaki oszczędzające). Jedną z nich jest szlak zależny od HGPRT (na rysunku HPRT), która katalizuje fosforybozylację guaniny oraz hipoksantyny do odpowiednich nukleotydów (IMP i GMP). Jej brak skutkuje gromadzeniem się w komórkach pirofosforanu fosforybozylu (PRPP), co przy niskim stężeniu IMP i GMP nasila biosyntezę puryn de novo[8][9].

Objawy i przebieg[edytuj | edytuj kod]
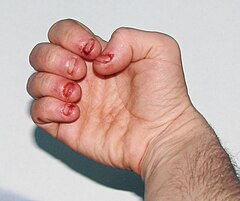
LNS daje objawy od chwili urodzenia. Pacjenci mają poważne psychiczne i fizyczne problemy przez całe życie. Zespół Lescha-Nyhana charakteryzuje się trzema głównymi cechami: zaburzeniem czynności neurologicznych, funkcji poznawczych (kognitywnych) oraz dewiacją zachowań, a także nadprodukcją kwasu moczowego (hiperurykemia). Niektórzy mogą być także dotknięci anemią (makrocytarną). W zasadzie wszyscy pacjenci to mężczyźni, którzy mają opóźniony wzrost i dojrzewanie, a ich jądra są pomniejszone lub atroficzne. Kobiety posiadające kopię zmutowanego genu mają zwiększone ryzyko dnawego zapalenia stawów, ale niemal nigdy nie są dotknięte schorzeniem. Brak HGPRT powoduje zwiększenie stężenia kwasu moczowego we wszystkich płynach ciała i prowadzi do takich problemów, jak dna moczanowa, słaba kontrola mięśniowa, umiarkowane opóźnienie umysłowe, które pojawiają się w pierwszym roku życia[10]. Uderzającą cechą zespołu Lescha-Nyhana są zachowania związane z samookaleczeniem, charakteryzujące się gryzieniem warg i palców, które pojawiają się w drugim roku życia. Nawyk ten jest tak silny, że używaną do niedawna metodą zapobiegania samookaleczaniu się była ekstrakcja zębów[11]. Nienormalnie wysoki poziom kwasu moczowego może powodować wytrącanie się kryształów moczanu sodu w stawach, nerkach, ośrodkowym układzie nerwowym oraz innych tkankach ciała, prowadząc do wystąpienia ostrych ataków dny z obrzmieniem stawów i poważnych problemów z nerkami. Wśród objawów neurologicznych występują: grymasy na twarzy, mimowolne skręcania oraz powtarzanie ruchów rąk i nóg, które przypominają te występujące w pląsawicy Huntingtona. Bezpośrednia przyczyna nieprawidłowości neurologicznych pozostaje nieznana. Niedobór HGPRT sprawia, że organizm słabo wykorzystuje witaminę B12 i u niektórych chłopców może się rozwinąć anemia megaloblastyczna[12].
Objawy ze strony układu moczowego[edytuj | edytuj kod]
Jednym z pierwszych objawów choroby jest pojawienie się przypominających piasek kryształków kwasu moczowego w pieluszce dotkniętego zespołem niemowlęcia. Nadmierna produkcja kwasu moczowego może prowadzić do powstania kryształów kwasu moczowego (potocznie kamieni) w nerkach, moczowodach lub pęcherzu moczowym. Takie kryształy odłożone później w stawach mogą dawać objawy dnawego zapalenia stawów, takie jak obrzmienie i bolesność dotykowa.

Nadprodukcja kwasu moczowego jest obecna od momentu narodzin, ale może nie być rozpoznana przy pomocy zwykłych klinicznych metod diagnostycznych. Stężenie kwasu moczowego w surowicy jest często w normie, jako że nadmiar puryn jest szybko eliminowany z moczem. Kryształy najczęściej pojawiają się w postaci pomarańczowego, ziarnistego materiału lub łączą się w liczne małe kamienie albo wyraźnie widoczne, duże kamienie, które trudno usuwają się w czasie oddawania moczu. Kamienie są zazwyczaj przyczyną hematurii (pojawienia się krwi w moczu) oraz wzrostu ryzyka zakażeń układu moczowego. U niektórych mogą wystąpić uszkodzenia nerek z powodu kamicy nerkowej. Kamienie mogą być główną cechą w chorobie, ale do momentu ich wykrycia może czasem minąć kilka miesięcy lub nawet lat.
Objawy neurologiczne[edytuj | edytuj kod]
Przez krótki czas po urodzeniu osoby z zespołem Lescha-Nyhana nie prezentują żadnych objawów chorobowych. Pierwsze najczęstsze objawy jakie się pojawiają, to obniżone napięcie mięśniowe (hypotonia) oraz opóźnienie rozwoju, które ujawniają się pomiędzy 3 i 6 miesiącem życia. Osoby dotknięte chorobą później siadają, a większość nigdy nie raczkuje i nie chodzi. Brak mowy jest także powszechną cechą powiązaną z zespołem Lescha-Nyhana.
Drażliwość jest najczęściej zauważana wraz z pierwszymi objawami upośledzenia układu nerwowego. W czasie kilku pierwszych lat życia zajęcie układu pozapiramidowego powoduje rozwinięcie się nienormalnych, mimowolnych skurczów mięśni, takich jak utrata kontroli motorycznej (dystonia), ruchy skręcające (choreoatetoza) oraz łukowate wygięcie się kręgosłupa (opistotonus). Objawy zajęcia układu piramidowego to spastyczność, wygórowanie odruchów (hyperrefleksja) oraz objaw Babińskiego. W aspekcie neurologicznym, zespół Lescha-Nyhana przypomina atetotyczne mózgowe porażenie dziecięce. W wyniku tego, większość pacjentów ma wstępnie zdiagnozowane mózgowe porażenie dziecięce. Niemoc motoryczna jest tak poważna, że większość osób nigdy nie będzie chodzić i do końca życia porusza się na wózku inwalidzkim.
Rozpoznanie[edytuj | edytuj kod]
Leczenie[edytuj | edytuj kod]
Objawy spowodowane gromadzeniem się kwasu moczowego (zapalenie stawów, objawy nerkowe) dobrze odpowiadają na leczenie za pomocą takich leków jak allopurinol, który obniża poziom kwasu moczowego w krwi. Upośledzenie umysłowe i zachowania związane z samookaleczaniem nie odpowiadają na leczenie. Wyleczenie nie jest możliwe, ale wielu pacjentów przeżywa do dorosłości. Kamienie nerkowe można leczyć za pomocą litotrypsji, która polega na rozbiciu kamieni przy użyciu lasera lub fal ultradźwiękowych. Nie ma standardu w leczeniu objawów neurologicznych zespołu Lescha-Nyhana. Poprawę mogą dać: karbidopa lub lewodopa, diazepam, fenobarbital lub haloperidol[13].
Niezbędne jest kontrolowanie nadprodukcji kwasy moczowego, aby obniżyć ryzyko nefropatii, kamicy nerkowej oraz dnawego zapalenia stawów. Allopurinol jest wykorzystywany do zatrzymania przekształcania oksypuryn do kwasu moczowego oraz aby zapobiec powstawaniu guzków dnawych (wykształacających się przy przewlekłej dnie), kamieni nerkowych oraz nefropatii nerkowej. Allopurinol jest przyjmowany doustnie w typowych dawkach 3–20 mg/kg masy ciała na dzień. Następnie ustala się dawkę allopurinolu tak, aby przywrócić poziom kwasu moczowego do stężenia prawidłowego (<3 mg/dL). Większość osób dotkniętych chorobą może być leczona allopurinolem przez całe życie.
Żadne lekarstwo nie jest skuteczne w kontrolowaniu pozapiramidowych ruchowych objawów choroby, jednakże spastyczność można zmniejszyć poprzez przyjmowanie baklofenu lub benzodiazepin. Baklofen to środek zwiotczający mięśnie o działaniu ośrodkowym, który pobudza receptory GABAβ, zlokalizowane pre- i postsynaptycznie[14], natomiast benzodiazepiny wywierają działanie uspokajające, przeciwlękowe oraz miorelaksacyjne[15].
Żadna metoda leczenia neurobehawioralnych aspektów choroby nie jest skuteczna. Nawet u dzieci leczonych od urodzenia allopurinolem rozwijają się problemy behawioralne i neurologiczne, pomimo tego, że poziom kwasu moczowego w surowicy nigdy nie był zbyt wysoki. Zachowania autoagresywne i inne niekorzystne zachowania można leczyć łącząc metody farmakologiczne, fizykalne i behawioralne.
Rokowanie[edytuj | edytuj kod]
Rokowanie dla osób z zespołem Lescha-Nyhana jest niekorzystne. Śmierć następuje zazwyczaj z powodu niewydolności nerek w pierwszej lub drugiej dekadzie życia[16].
Uwagi[edytuj | edytuj kod]
- ↑ Spotykana jest też nieprawidłowa nazwa zespół Lesch-Nyhana.
Przypisy[edytuj | edytuj kod]
- ↑ Lesch-Nyhan syndrome; LNS w bazie Online Mendelian Inheritance in Man (ang.)
- ↑ HA Jinnah, T Friedmann: Lesch-Nyhan disease and its variants. Scriver, CR, Beaudet, AL, Sly, WS, Valle, D (red.). New York: McGraw-Hill, 2001. ISBN 0-07-913035-6.
- ↑ Lesch M, Nyhan Wl, A familial disorder of uric acid metabolism and central nervous system function, „The American Journal of Medicine”, 36, 1964, DOI: 10.1016/0002-9343(64)90104-4, PMID: 14142409 (ang.).
- ↑ W. Catel, J. Schmidt, Über familiäre gichtische Diathese in Verbindung mit zerebralen und renalen Symptomen bei einem Kleinkind 1, „DMW - Deutsche Medizinische Wochenschrift”, 84 (48), 1959, s. 2145–2147, DOI: 10.1055/s-0028-1114586 [dostęp 2022-07-15] (niem.).
- ↑ J.E. Seegmiller, F.M. Rosenbloom, W.N. Kelley, Enzyme defect associated with a sex-linked human neurological disorder and excessive purine synthesis, „Science”, 155 (3770), 1967, s. 1682–1684, DOI: 10.1126/science.155.3770.1682, PMID: = en 6020292język = en [dostęp 2022-07-15].
- ↑ Genetics Home Reference
- ↑ U. Francke i inni, The occurrence of new mutants in the X-linked recessive Lesch-Nyhan disease, „American Journal of Human Genetics”, 28 (2), 1976, s. 123–137, PMID: 1266847, PMCID: PMC1684918 [dostęp 2022-07-15] (ang.).
- ↑ Robert K. Murray, Daryl K. Granner, Victor W. Rodwell: Biochemia Harpera. Wyd. VI uaktualnione. Warszawa: PZWL, 2015, s. 363-365, 370. ISBN 978-83-200-4554-3.
- ↑ Edward Bańkowski: Biochemia. Podręcznik dla studentów uczelni medycznych. Wyd. II. Wrocław: Elsever Urban & Partner, 2009, s. 310, 314. ISBN 978-83-7609-041-2.
- ↑ Boby Varkey Maramattom, Self-mutilation in the Lesch-Nyhan syndrome, „Neurology”, 65 (11), 2005, E25, DOI: 10.1212/01.wnl.0000184611.55051.f3, PMID: 16344506 [dostęp 2022-07-15] (ang.).
- ↑ L.T. Anderson, M. Ernst, Self-injury in Lesch-Nyhan disease, „Journal of Autism and Developmental Disorders”, 24 (1), 1994, s. 67–81, DOI: 10.1007/BF02172213, PMID: 8188575 [dostęp 2022-07-15] (ang.).
- ↑ S.P. van der Zee, E.D. Schretlen, L.A. Monnens, Megaloblastic anaemia in the Lesch-Nyhan syndrome, „The Lancet”, 1 (7557), 1968, s. 1427, DOI: 10.1016/s0140-6736(68)92002-3, PMID: 4173010 [dostęp 2022-07-15] (ang.).
- ↑ NIH/NINDS Lesch-Nyhan Information Page.. ninds.nih.gov. [zarchiwizowane z tego adresu (2007-06-08)]. NIH/NINDS (13 lutego 2007). Data dostępu 12 kwietnia 2007
- ↑ Baklofen, [w:] Indeks Leków MP, opis substancji, Medycyna Praktyczna [dostęp 2022-07-15].
- ↑ Przemysław Bieńkowski i inni, Bezpieczne stosowanie benzodiazepin w podstawowej opiece zdrowotnej – rekomendacje dla lekarzy rodzinnych, „Lekarz POZ”, 5 (3), 2019, s. 177-193 [dostęp 2022-07-15].
- ↑ Strona informacyjna NIH/NINDS. [dostęp 2007-06-11]. [zarchiwizowane z tego adresu (2007-06-08)].
Bibliografia[edytuj | edytuj kod]
- Rosa J Torres, Juan G Puig, Hypoxanthine-guanine phosophoribosyltransferase (HPRT) deficiency: Lesch-Nyhan syndrome, „Orphanet Journal of Rare Diseases”, 2 (1), 2007, s. 48, DOI: 10.1186/1750-1172-2-48, PMID: 18067674, PMCID: PMC2234399 [dostęp 2022-07-15] (ang.).
Linki zewnętrzne[edytuj | edytuj kod]
- William L. Nyhan, J. Patrick O'Neill, Hyder A. Jinnah, James C. Harris: Lesch-Nyhan Syndrome. [w:] GeneReviews [on-line]. University of Washington, Seattle, 2000 (aktualizacja 2014). [dostęp 2017-02-09].
- H.A. Jinnah: Lesch-Nyhan Disease. Medscape, 2015-12-14 (data aktualizacji). [dostęp 2017-02-09]. (ang. • niem. • hiszp. • fr. • port.)
- Lesch-Nyhan syndrome or disease w bazie Who Named It (ang.)
