Ogólny plan budowy kończyn


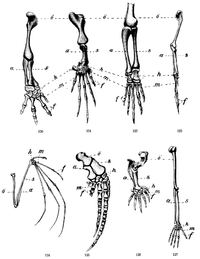
Brązowy – kość ramienna. czerwony – kość łokciowa, beżowy – kość promieniowa, żółty – nadgarstek, ciemnobrązowy – śródręcze i paliczki
Ogólny plan budowy kończyn kręgowców – zasady przekazywania dziedzicznej informacji o charakterystycznych dla wszystkich gatunków kręgowców oraz dla poszczególnych osobników cechach kończyn oraz o przebiegu procesu ich budowy w okresie ontogenezy. Kończyny embrionów zwierząt należących do różnych gatunków, lecz pochodzących od wspólnego przodka – skrzydła ptaków lub nietoperzy, płetwy ryb albo kończyny gadów lub ssaków – powstają w okresie embriogenezy według wspólnego „ogólnego planu budowy” zakodowanego w DNA i powielanego w procesie replikacji. Charakterystyczny dla gatunku żyjącego w określonym środowisku zestaw genów jest efektem procesów filogenezy, a zestaw genów osobnika – efektem rekombinacji w czasie zapłodnienia. Mimo wielkiego zróżnicowania w ramach kladu kończyny różnych zwierząt zachowują podobieństwo do budowy kończyn wspólnego przodka, dostrzegalne wyraźnie w okresie embriogenezy.
Kończyny wszystkich kręgowców – piersiowe (przednie, górne) i miedniczne (tylne, dolne) – mają jednakowy ogólny plan budowy (zob. homologia). Są zbudowane z trzech segmentów:
- stylopodium – jedna kość „ramienna” lub „udowa”[a]
- zeugopodium – dwie kości „przedramienia” (kości promieniowa i łokciowa) lub „podudzia” (kości piszczelowa i strzałkowa)[b]
- autopodium – grupa drobniejszych kostek „ręki” lub „stopy”[c].
Elementy historii badań[edytuj | edytuj kod]
Ręka człowieka (nadgarstek, śródręcze, palce) współdziałająca z przedramieniem, ramieniem i barkiem jest bardzo złożoną unerwioną konstrukcją zbudowaną między innymi z kości, mięśni, chrząstek. Umożliwia wykonywanie wielu różnorodnych czynności, zarówno bardzo precyzyjnych, jak i wymagających użycia siły. Budziła zainteresowanie artystów (np. Leonardo da Vinci). Charles Bell – szkocki anatom, chirurg, fizjolog i teolog – uznawał ją za dowód stworzenia – doskonałe dzieło Stwórcy. Wyraża to tytuł wydanej w roku 1834 książki The Hand, Its Mechanism and Vital Endowments as Deyincing Design[1] (Ręka, jej mechanizm i funkcje życiowe jako oznaka Stworzenia)[2].
Przełomowe porównania budowy kończyn różnych kręgowców z budową kończyn człowieka przeprowadził Richard Owen, autor wydanej w roku 1849 książki On the Nature of Limbs[3][4]. W przeciwieństwie do swoich poprzedników opisywał on przede wszystkim podobieństwa między osobnikami należącymi do różnych gatunków a nie różnice między nimi. Doprowadziło go to do zdefiniowania pojęcia homologii. Myśl Owena rozwinął w drugiej połowie XIX w. Karl Gegenbaur (1826-1903) – biolog ewolucyjny (zwolennik teorii ewolucji Karola Darwina), jeden z twórców anatomii porównawczej zwierząt, autor książki Elements Of Comparative Anatomy (1878)[5]. W tym samym okresie problemami ewolucji zajmował się również Ernst Haeckel (1834–1919), autor książki pt. Generelle Morphologie der Organismen (1866), w której znalazło się po raz pierwszy fundamentalne pojęcie filogenezy (zob. też filogenetyka)[6]
w kończynach różnych kręgowców:
A – kościec kończyn dolnych człowieka (kończyny miedniczne),
B – mięśnie barku, ramienia i przedramienia człowieka (szkice Leonarda da Vinci),
C – przykłady kośćców kończyn piersiowych człowieka i innych kręgowców (rys. Wilhelm Leche, 1909): 120 – płaz ogoniasty, 121 – żółw, 122 – krokodyl, 123 – ptak, 124 – nietoperz, 125 – waleń, 126 – kret, 127 – człowiek
W XX wieku nastąpił szybki rozwój nauki, dzięki któremu stały się dostępne nowe techniki badawcze, takie jak: datowanie izotopowe, spektrometria mas, sekwencjonowanie DNA, sekwencjonowanie białka. Umożliwiło to przyspieszenie postępu nauk biologicznych, w tym szybki rozwój wielu specjalistycznych dyscyplin naukowych (np. biochemia, biologia molekularna, genetyka i genomika, embriologia, ekologia ewolucyjna). Badania historii świata zwierząt – w tym przebiegu ewolucji kończyn kręgowców – są współcześnie kontynuowane na wyższym poziomie. Stało się możliwe połączenie informacji pochodzących z badań paleozoologicznych z informacjami o przeszłości gatunków zawartymi w DNA zwierząt współczesnych.
Filogeneza[edytuj | edytuj kod]
Wśród organizmów pochodzących od wspólnego przodka ewolucja doprowadziła do zróżnicowania budowy ciała, w tym kończyn przedstawicieli poszczególnych gatunków, wskutek przystosowań do zróżnicowanych i zmieniających się warunków życia. Zgodnie z neodarwinowską zasadą doboru naturalnego wzrost dostosowania (fitness) polega na stopniowych zmianach DNA (zob. gradualizm). Warunkiem reprodukcyjnego sukcesu organizmów wyposażonych w określony zestaw genów (określających m.in. przebieg wzrostu kończyn w czasie rozwoju osobniczego) jest większa rozrodczość i mniejsza śmiertelność. Często decydująca jest „śmiertelność ekologiczna” (rzeczywista, realizowana), określana z uwzględnieniem nie tylko biologicznych cech gatunku (śmiertelność biologiczna, potencjalna), ale również oporu środowiska[7][8][9].
Jednym z przykładów filogenetycznych przemian budowy i funkcji kończyn jest proces, który doprowadził do powstania gatunku Tiktaalik roseae („forma przejściowa” między rybami i płazami). Przypuszcza się, że przekształcenie płetw piersiowych gatunku dużych ryb mięśniopłetwych sprawiło, że stał się on lepiej dostosowany do środowiska życia. Do tego przekształcenia doszło w późnym dewonie (ok. 350 mln lat temu), w słodkiej wodzie rzek znajdujących się wówczas w rejonie współczesnej arktycznej Kanady. Płetwy „płazoryby”, której skamieniałości odkrył zespół Neila Shubina, mogły się zginać w połowie (płetwa miała rodzaj „barku”, „łokcia” i „nadgarstka”), dzięki czemu zwierzę mogło pełzać po przybrzeżnym mule (według Shubina mogło również wykonywać „pompki” w płytkiej przybrzeżnej wodzie). Prawdopodobnie ułatwiało to ucieczkę przed atakującymi wielkimi wodnymi drapieżnikami, co przyczyniło się do zmniejszenia śmiertelności[10][11].
Analogiczne filogenetyczne przekształcenia kończyn płazów, gadów i ssaków lub skrzydeł ptaków prawdopodobnie wielokrotnie wywierały podobny wpływ na fitness innych powstających gatunków kręgowców[12].

Ontogeneza[edytuj | edytuj kod]

W DNA różnych gatunków, ulegającym zmianom w czasie ich ewolucyjnego przystosowywania się do środowiska (zbioru określonych abiotycznych i biotycznych czynników ekologicznych), zostają zarejestrowane plany budowy ciała zwierząt oraz programy ich realizacji – w tym plan budowy kończyn w czasie rozwoju osobniczego (ontogenezy). We wczesnym etapie tego rozwoju (embriogeneza) istnieje duże wzajemne podobieństwo zarodków różnych gatunków (podobieństwo do wspólnego przodka, Ernst Haeckel)[13], co leżało u podstaw historycznej już teorii rekapitulacji[14].
W najwcześniejszym okresie życia zwierząt rozmnażających się płciowo powstaje zygota – komórka będąca wynikiem połączenia się dwóch haploidalnych gamet (zob. gametogeneza): męskiej (plemnik) i żeńskiej (komórka jajowa). Ta pojedyncza komórka zawiera unikalny DNA, decydujący o przebiegu dalszego rozwoju, jednak morfologicznie nie różni się od innych komórek eukariotycznych. Bardzo podobna jest również budowa zarodków i płodów kręgowców wytwarzających błony płodowe (owodniowce, w tym zauropsydy takie jak współczesne gady czy ptaki, a także ssaki), oraz przebieg różnicowania się tkanek i powstawania narządów. W przypadku zarodka ludzkiego przez 8–9 tygodni obserwuje się na przykład wzrost ogona[15], przez 6–7 tygodni serce przypomina serca ryb i płazów, a zaczątki palców ręki są połączone błoną pławną.
Kierunek ułożenia wypustek kończyn dolnych w ludzkim zarodku nie sugeruje przyszłej pionowej postawy ciała, a staw łokciowy i kolanowy rozwierają się w tym samym kierunku (rotacja kończyn w odpowiednich stawach następuje w późniejszym okresie embriogenezy)[12][d].


Genetyczny program budowy i rozwój kończyn[edytuj | edytuj kod]

Paleozoologiczne badania skamieniałości, np. sfosylizowanych fragmentów szkieletów lub tropów dawnych zwierząt, połączone z analizą stratygraficzną, dostarczają tylko wyrywkowych informacji o przebiegu ewolucji kończyn kręgowców. Źródłem bardziej kompletnej wiedzy stały się w ostatnich dziesięcioleciach badania genetyczne. Powstający w zygocie chromosomowy DNA jest kombinacją genów[16] rodziców (analogicznie utworzył się ich DNA oraz DNA ich przodków). Kolejność nukleotydów w łańcuchu decyduje o fenotypie nowego organizmu (zob. genotyp i plastyczność fenotypowa). Z jednej z dwóch nici DNA, nazywanej nicią kodującą lub „sensowną” (+)[e], poprzez zastosowanie kodu genetycznego odczytywana jest zapisana w DNA informacja – geny ulegają ekspresji, powstają określone białka (kolejność kodonów określa sekwencję aminokwasów w łańcuchu polipeptydowym białek)[17].
Pierwsza komórka nowego organizmu (zygota) ulega mitotycznemu podziałowi. Tworzą się blastomery[18]. Następnie powstaje morula i blastula, czyli kulista grupa 16 jednakowych komórek, utworzonych wskutek czterech kolejnych podziałów[19] (u niektórych organizmów, w tym u człowieka, ma ona formę blastocysty[18]). Nie zawiera ona żadnych dostrzegalnych dowodów realizacji genetycznego „planu budowy ciała”[19].
Dalszy wzrost objętości zarodkowej tkanki łącznej (mezenchyma) i gastrulacja przebiega u różnych gatunków w sposób zróżnicowany. W powstających gastrulach zwierząt z grupy trójwarstwowców wyodrębniają się trzy warstwy komórek – listki zarodkowe (ektoderma, entoderma i mezoderma). Każda z warstw pełni określoną funkcję w procesach zróżnicowania się tkanek (np. tkanka kostna, chrzęstna, mięśniowa) oraz powstawania narządów, m.in. kończyn o różnym stopniu złożoności, ale zbudowanych zgodnie z „ogólnym planem budowy” w przestrzeni trójwymiarowej (uwzględniającym pojęcia góra-dół, prawo-lewo)[19].
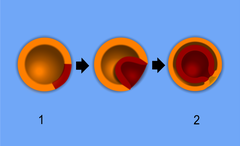
A. grupa komórek o jednakowych funkcjach – przemiana moruli (1) w blastulę (2),
B. Gastrulacja – przemiana blastuli (1) w gastrulę z wyodrębnionymi listkami (2)
(trzy warstwy o zróżnicowanych funkcjach)
Możliwość budowy różnych tkanek, pomimo że wszystkie komórki zarodka zawierają taki sam łańcuch DNA, jest związana z różnym przebiegiem procesów ekspresji poszczególnych genów. W komórkach eukariotycznych regulacja ekspresji jest związana z tworzeniem kompleksów, które zmieniają szybkość procesów transkrypcji[20] (zob. czynnik transkrypcyjny, ogólne czynniki transkrypcyjne, kompleks preinicjacyjny, promotor genu, białko wiążące DNA, enhancer). W efekcie takich procesów tylko ok. 15% genów DNA komórek eukariotycznych ulega ekspresji (również wewnątrz pojedynczych aktywnych genów występują eksony i introny; zob. gen podzielony[21]). Łańcuchy DNA zawierają również nie ulegające ekspresji pseudogeny, fragmenty genów oraz obszary pozagenowe o nie poznanym pochodzeniu i funkcji (70–80% genomu człowieka)[22].
Rodzaj genów uaktywnianych w poszczególnych komórkach, a więc rodzaj powstających białek, zależy od chemicznego składu otoczenia łańcucha DNA[17]. Badania mechanizmu regulacji ekspresji genów uczestniczących w budowie kończyn mają wieloletnią historię i wciąż trwają w licznych ośrodkach naukowych. Dotyczą procesów w różnej skali, np. zarówno mechanizmu różnicowania tkankowego w czasie ontogenezy, jak zjawisk ewolucyjnego przekształcenia płetw wymarłych gatunków w kończyny czworonożnych zwierząt lądowych (Tetrapoda)[23][24][25].

W rozwoju zarodkowym człowieka w 4. tygodniu po stronie brzuszno-bocznej pojawiają się niewielkie wypukłości – zawiązki przyszłych kończyn (pączki kończynowe). Jego rdzeń tworzy gęsta mezenchyma z listka ściennego mezodermy bocznej, otoczona czapeczką epidermalną (szczytowa listewka epidermalna, grzebień szczytowy, ang. Apical Ectodermal Ridge – AER). Dla rozwoju kończyny kluczową rolę odgrywa oddziaływanie pomiędzy mezenchymą rdzenia a AER. W warunkach naturalnych mezencyma obficie się dzieli, dzięki czemu pączki wydłużają się, a na ich obwodzie powstają płytka ręki pierwotna i płytka stopowa. Promienie palczaste pojawiają się około 7 tygodnia, następnie zaś tworzą się okrężne przewężenia, dzięki którym kończyny podzielą się na 3 części (patrz wyżej)[26].
Neil Shubin przełomowe znaczenie przypisuje eksperymentom wykonanym w latach 50. i 60. XX w. przez Edgara Zwillinga[27] i Johna Saundersa[28]. Stosując technikę mikrochirurgiczną, naukowcy wykazali, że proces wzrostu kończyn zarodka kurzego można kontrolować, usuwając lub przemieszczając niewielkie fragmenty cienkiej warstwy komórek pokrywających ich zawiązki[f]. Efekty zależały od momentu, w którym zabiegi były wykonywane, np. AER w bardzo wczesnym okresie embriogenezy prowadzi do całkowitego zahamowania rozwoju kończyny, a pisklęta, którym tkankę usunięto później, miały tylko kość ramienną lub tylko ramię i przedramię.
W kolejnych latach stwierdzono (Mary Gasseling z laboratorium Saundersa[29]), że przemieszczenia pewnych fragmentów tkanki na przeciwną stronę zawiązka kończyny powodowało rozwój dwóch kończyn o układzie zwierciadlanym. Fragment tkanki, której przemieszczanie powodowało takie efekty, nazwano „strefą aktywności polaryzującej” ZPA (ang. Zone of Polarizing Activity) wydzielają białko Sonic hedgehog (SHH), które rozprzestrzenia się i aktywuje ekspresję określonych genów w sąsiednich komórkach[30]. Stwierdzono również, że za wymienione efekty odpowiada dyfuzja białka SHH do określonych miejsc powierzchni zawiązka (wstawianie przegrody z folii powodowało zahamowanie wzrostu kończyny za przegrodą).
Wkrótce odkryto w zarodkach inne „centra sygnalizacyjne” wytwarzające inne białkowe substancje sygnałowe o działaniu analogicznym do SHH (zob. czynniki wzrostu fibroblastów (FGF), szereg białek szlaku sygnalizacyjnego Wnt). Cząsteczki te stymulują lub hamują transkrypcję DNA w komórkach docelowych. Są odpowiedzialne nie tylko za budowę kończyn wielu różnych kręgowców, lecz również odgrywają decydującą rolę w budowie np. serca, nerek i innych narządów kręgowców lub w budowie ciał owadów (realizacja „ogólnego planu budowy” ich ciał)[31][24].
W zawiązkach kończyn czynne są trzy centra sygnalizacyjne[31][24]:
- oś P-D, bliższo-dalsza („proksymalno-dystalna”) – kierunek wzrostu od ramienia do czubków palców (regulowany przez białka wydzielane z AER),
- oś A-P, przednio-tylna („anterioralno-posterialna”) – kierunek od kciuka do małego palca (regulowany przez centrum ZPA),
- oś D-V, grzbietowo-brzuszna („dorsalno-wentralna”) – kierunek od grzbietu dłoni do strony wewnętrznej.
W układaniu planu budowy kończyn uczestniczą białka zakodowane w genach rodziny hox[24].
Model reakcji-dyfuzji w rozwoju kończyny[edytuj | edytuj kod]
Po raz pierwszy w 1979 roku zaproponowano model reakcji-dyfuzji Turinga dla wyjaśnienia zjawisk zachodzących w trakcie rozwoju osi proksymalno-dystalnej kończyny[32]. Poprawność hipotezy została potwierdzona eksperymentalnie w 2007 roku i została ona powszechnie przyjęta[33]. Poprzedni akceptowany model strefy postępu (ang. progress zone, PZ), zakładający, że różnicowanie zachodzi na zasadzie czasu przebywania komórek w niewielkim paśmie komórek mezenchymatycznych pod dystalną warstwą ektodermy, okazał się niespójny z danymi doświadczalnymi. Komórki pozostające dłużej w strefie PZ miałyby przechodzić więcej podziałów mitotycznych i tworzyłyby bardziej dystalne struktury. Ponieważ jednak zarodki kury domowej zmutowane pod kątem wyłączenia ekspresji białek Fgf8 i Fgf4 wytwarzały względnie normalne struktury dystalne, z pominięciem proksymalnych, model nie jest poprawny[34]. Ponadto badania ze znakowaniem poszczególnych komórek wczesnej PZ wykazały, że ich komórki potomne pozostają w danym segmencie kończyny i prawdopodobnie przechodzą znacznie wcześniejszą specyfikację[35].
Model reakcji-dyfuzji opisuje zachowanie układu chemicznego, w którym jeden związek stanowi własny aktywator oraz aktywator swojego inhibitora, przy założeniu, że inhibitor dyfunduje wolniej. Innymi słowy: związek A, o większej prędkości dyfuzji, przechodzi autokatalizę, ale jednocześnie aktywuje związek B, dyfundujący wolniej, który jest inhibitorem związku A. Model matematyczny opracowany przez Alana Turinga wskazuje na powstanie swoistych fal stojących stężenia rozłożonych w przestrzeni.
Kluczowe w rozwoju osi proksymalno-dystalnej są białka z rodziny TGF-β (głównie białka morfogenetyczne kości, aktywina) oraz białka macierzy pozakomórkowej (białka ECM) i białka adhezji komórkowej, które inicjują formowanie węzłów chrzęstnienia. W strefie apikalnej białka Fgf8 i Fgf4 syntetyzowane przez AER hamują działanie TGF-β, przez co nie dochodzi tam do chrzęstnienia (brak TGF-β oznacza brak syntezy białek ECM i białek adhezji komórkowej). W strefie reakcji-dyfuzji zachodzi interakcja TGF-β ze swoistym białkiem receptorowym (jako receptory zidentyfikowano dotąd Notch, Noggin, białka FGF, galektynę-8), które wiąże czynniki TGF-β i hamuje ich działanie, jednak jednocześnie TGF-β stymulują własną syntezę na zasadzie pętli sprzężenia dodatniego oraz syntezę receptora. TGF-β dyfunduje wolniej niż jego inhibitor, przez co okresowo pojawiają się fale stojące stężeń w określonych obszarach zawiązka[36]
W ostatniej fazie rozmiar danej strefy decyduje o wyjściu ze stadium reakcji-dyfuzji i utworzenie tzw. strefy zamrożonej (ang. frozen zone), gdzie komórki agregują w tkankę chrzęstną. Większa prędkość dyfuzji inhibitora ostatecznie powoduje przewagę TGF-β w węźle chrzęstnienia, a co za tym idzie zwiększoną produkcję białek macierzy pozakomórkowej i białek adhezji, które, znajdując się już daleko od AER, nie podlegają pośredniej inhibicji ze strony Fgf8 i Fgf4[37]. Wydaje się jednak, że strefa zamrożona jeszcze wcześniej przestaje być hamowana przez inhibitory TGF-β, kiedy upakowanie komórek przekroczy określoną wartość progową[36].
Rola modelu reakcji-dyfuzji w formowaniu osi brzuszno-grzbietowej[edytuj | edytuj kod]
Dyfuzja TGF-β oraz jego receptora jest ograniczona, przez co wzrost zawiązka kończyny pozwala na organizację skupisk reakcji-dyfuzji. Przy wczesnym, małym zawiązku istnieje tylko jedno skupisko, a w fazie formowania się zeugopodium (łydki lub przedramiona) już dwa, dzięki czemu później powstaną dwie kości długie[36].
Obecnie uważa się, że model reakcji-dyfuzji stanowi główny system decydujący zarówno o formowaniu kości w osi proksymalno-dystalnej, jak i brzuszno-grzbietowej. Geny Hox oraz ekspresja białka Sonic hedgehog (Shh) funkcjonują najprawdopodobniej jako elementy regulatorowe[38].
Inhibicja chrzęstnienia w strefie apikalnej zawiązka kończyny[edytuj | edytuj kod]
Sonic hedgehog produkowane w ZPA aktywuje białko Gremlin-1, które z kolei hamuje białka morfogenetyczne kości (BMP). Działanie BMP sprowadza się do wstrzymywania ekspresji Fgf8, a co za tym idzie także ekspresji Fgf10. Coraz niższe stężenie Fgf8 powoduje coraz słabszą inhibicję produkcji białek ECM i białek adhezji komórkowej, a małe stężenie Fgf10 hamuje procesy mitotyczne w mezenchymie zawiązka. Zatem dzięki sekrecji Sonic hedgehog przez komórki ZPA strefa apikalna jest utrzymywana w stanie niepozwalającym na chrzęstnienie mezenchymy, a komórki dalej dzielą się mitotycznie, co umożliwia odpowiedni wzrost zawiązka[39].
Zatrzymanie wzrostu w osi proksymalno-dystalnej[edytuj | edytuj kod]
Gremlin-1 jest aktywny, gdy stężenie FGF pozostaje na niskim poziomie. Przez brak inhibicji ze strony BMP stężenie FGF rośnie, a białko Gremlin-1 staje się nieaktywne, co z kolei uwalnia BMP i powoduje spadek stężenia FGF oraz Wnt7a. Z kolejnymi podziałami komórkowymi zaczynają przeważać komórki nieposiadające receptora dla Sonic hedgehog, a co za tym idzie, niezdolne do syntezy Gremlin-1. Ostatecznie owe niekompetentne komórki znacznie utrudnią dyfuzję Sonic hedgehog i Gremlin-1 do takiego stopnia, że BMP staną się dominującą frakcją, hamując m.in. Fgf10 syntetyzowany przez AER, co spowoduje zahamowanie podziałów mitotycznych i zainicjowanie procesu chrzęstnienia[39].
Wady rozwojowe[edytuj | edytuj kod]
Błędy zdarzające się w planach budowy kończyn (zob. aberracje chromosomowe, mutacje pojedynczych genów) są przyczyną wielu wrodzonych wad rozwojowych. Etiologii 60% tych wad dotychczas nie wyjaśniono. W powstawaniu wad o poznanej etiologii istotną rolę odgrywają przeważnie czynniki genetyczne (85%). Są to m.in.[40][41]:
- polidaktylia – obecność dodatkowego palca lub palców,
- syndaktylia – zrośnięcia dwóch lub więcej palców dłoni i (lub) stopy,
- ektrodaktylia – całkowity lub częściowy brak palców stopy i (lub) dłoni,
- oligodaktylia – zmniejszona liczba palców (zob. zespół Robertsa),
- artrogrypoza,
- wady poprzeczne kończyn,
- dysplazje kostne.
Całkowity brak kończyn określa się mianem amelii bądź ectromelia, brak częściowy – meromelii. Istnieją też określenia takie, jak hemimelia (kończyna połowicza), peromelia (strzałkowatość kończyny), fokomelia (bezpośrednie połączenie dłoni lub stóp z tułowiem)[42]. Niektóre z wad są wiązane z oddziaływaniem pasożytów, na co wskazują wyniki badań rzekotki królewskiej, płaza z rodziny rzekotkowatych[43].
-
Polidaktylia ręki
-
Zahamowanie apoptozy prowadzące do syndaktylii
-
Polidaktylia kości stopy
-
Rzekotka królewska z dodatkową parą kończyn[43]
Uwagi[edytuj | edytuj kod]
- ↑ Segment nasadowy – wymienione kości kończyn człowieka lub ich odpowiedniki w kończynach piersiowych i miednicznych innych kręgowców.
- ↑ Segment przejściowy – wymienione kości kończyn człowieka lub analogiczne kości kończyn piersiowych i miednicznych innych kręgowców.
- ↑ Segment obwodowy – kostki nadgarstka, śródręcza i palców oraz stępu, śródstopia i palców stopy człowieka lub różna liczba analogicznych kostek w autopodium kończyn piersiowych i miednicznych innych kręgowców
- ↑ Niniejszy artykuł nie obejmuje zagadnień mieszczących się w dziedzinie antropologii filozoficznej, w tym np. procesu progresywnej personalizacji.
- ↑ W zależności od genu obie nici DNA mogą pełnić zamiennie funkcję nici sensownej i antysensownej
- ↑ Zobacz też – podobne strefy wzrostu w roślinach (merystem wierzchołkowy), np. radykuły korzeni, merystem wierzchołkowy pędu pędu.
Zobacz też[edytuj | edytuj kod]
- głęboka homologia
- polidaktylia bazalnych czworonogów
- Sydney Brenner
- Howard Robert Horvitz
- John Sulston
Przypisy[edytuj | edytuj kod]
- ↑ Charles Bell (1774-1842): The hand; its mechanism and vital endowments, as evincing design. London: W. Pickering, 1834.
- ↑ Shubin 2009 ↓, s. 31.
- ↑ Richard Owen: On the nature of limbs. London: John Van Voorst, 1849.
- ↑ Shubin 2009 ↓, s. 31–33.
- ↑ Carl Gegenbaur: Elements Of Comparative Anatomy. Macmillan And Company, 1878.
- ↑ Ernst Heinrich Philipp August Haeckel: Generelle morphologie der organismen. Allgemeine grundzüge der organischen formen-wissenschaft, mechanisch begründet durch die von Charles Darwin reformirte descendenztheorie. Berlin: Georg Reimer, 1866.
- ↑ Charles J. Krebs (tłum. Anna Kozakiewicz, Michał Kozakiewicz, Jakub Szacki): Ekologia. Eksperymentalna analiza rozmieszczenia i liczebności. Wyd. 4. Warszawa: Wydawnictwo Naukowe PWN, 2011, s. 152, 159, 167,–. ISBN 978-83-01-16552-9.
- ↑ Ekologia > Podstawowe pojęcia ekologiczne; Właściwości populacji; Stosunki w biocenozie. pl.static.z-dn.net. [dostęp 2014-08-20]. [zarchiwizowane z tego adresu (2016-03-04)]. (pol.).
- ↑ Jerzy Dzik: Dzieje życia na Ziemi. Warszawa: Wydawnictwo Naukowe PWN, 2011, s. 85. ISBN 978-83-01-16678-6.
- ↑ Shubin 2009 ↓, s. 26, 39–41.
- ↑ Neil Shubin, Cliff Tabin, Sean Carroll. Fossils, genes and the evolution of animal limbs. „Nature”. 388, s. 639–648, 14 sierpnia 1997. Macmillan Publishers Ltd. (ang.).
- ↑ a b Shubin 2009 ↓, s. 42.
- ↑ a b Michael K. Richardson, Gerhard Keuck. Haeckel's ABC of evolution and development. „Biol. Rev.”. 77 (2), s. 495-528, 2002. Cambridge Philosophical Society. DOI: 10.1017/S1464793102005948. [zarchiwizowane z adresu]. (ang.).
- ↑ Gerhard Medicus. The Inapplicability of the Biogenetic Rule to Behavioral Development. „Human Development”. 35 (1), s. 1-8, 1992. ISSN 0018-716X. (ang.).
- ↑ T.E. Herman, M.J. Siegel. Human tail–caudal appendage: tethered cord. „Journal of Perinatology”, s. 518–519, 2008. Nature Publishing Group (NPG). DOI: 10.1038/jp.2008.39. ISSN 0743-8346. (ang.).
- ↑ Winter, Hickey i Fletcher 2009 ↓, s. 7–11.
- ↑ a b Winter, Hickey i Fletcher 2009 ↓, s. 65–71.
- ↑ a b Hieronim Bartel: Embriologia. Wyd. IV. Warszawa: Wydawnictwo Lekarskie PZWL, 2007.
- ↑ a b c Shubin 2009 ↓, s. 86-91.
- ↑ Winter, Hickey i Fletcher 2009 ↓, s. 15–23.
- ↑ Winter, Hickey i Fletcher 2009 ↓, s. 10–11.
- ↑ Winter, Hickey i Fletcher 2009 ↓, s. 97.
- ↑ Chris T. Amemiya, Jessica Alföldi, Lee AP, Fan S, Philippe H, [...], Kerstin Lindblad-Toh,. The African coelacanth genome provides insights into tetrapod evolution. „Nature”. 496 (7445), s. 311-316, 2013 Apr 18. Nature Publishing Group (npg). DOI: 10.1038/nature12027. PMCID: PMC3633110. (ang.).
- ↑ a b c d Przemko Tylzanowski. Gra w rękę (Sleight of Hand). „Postępy biologii komórki”. 32 (4), s. 647–660, 2005. Katedra i Zakład Histologii i Embriologii Uniwersytetu Medycznego w Poznaniu. (pol.).
- ↑ Shubin 2003 ↓, s. 43–100.
- ↑ Hieronim Bartel: Embriologia. Wyd. IV. Warszawa: Wydawnictwo Lekarskie PZWL, 2007, s. 509.
- ↑ Saunders JW Jr.. Edgar Zwilling; an appreciation. „Dev Biol.”. 26 (1), s. 165-169, 1971 Sep. PMID: 4939251. (ang.).
- ↑ John W. Saunders, Jr.. [w:] Biogram [on-line]. www.sdbonline.org. [dostęp 2014-08-24]. (ang.).
- ↑ Saunders JW [au]. [w:] National Institutes of Health PubMed [on-line]. US National Library of Medicine. [dostęp 2014-08-24]. (ang.).
- ↑ Philip W. Ingham & Marysia Placzek. Orchestrating ontogenesis: variations on a theme by sonic hedgehog : Fig 4. Control of identity and growth by SHH in the developing vertebrate limb. „Nature Reviews Genetics”, s. 841-850, November 2006. DOI: 10.1038/nrg1969. (ang.).
- ↑ a b Shubin 2003 ↓, s. 47–49.
- ↑ S.A. Newman, H.L. Frisch, Dynamics of skeletal pattern formation in developing chick limb, „Science”, 4407, 1979, s. 662–668, DOI: 10.1126/science.462174, ISSN 0036-8075, PMID: 462174 [dostęp 2016-03-25] (ang.).
- ↑ Stuart A. Newman, Ramray Bhat, Activator-inhibitor dynamics of vertebrate limb pattern formation, „Birth Defects Research. Part C, Embryo Today: Reviews”, 4, 2007, s. 305–319, DOI: 10.1002/bdrc.20112, ISSN 1542-9768, PMID: 18228262 [dostęp 2016-03-25].
- ↑ Xin Sun, Francesca V. Mariani, Gail R. Martin, Functions of FGF signalling from the apical ectodermal ridge in limb development, „Nature”, 6897, 2002, s. 501–508, DOI: 10.1038/nature00902, ISSN 0028-0836 [dostęp 2016-03-25] (ang.).
- ↑ Andrew T. Dudley, María A. Ros, Clifford J. Tabin, A re-examination of proximodistal patterning during vertebrate limb development, „Nature”, 6897, 2002, s. 539–544, DOI: 10.1038/nature00945, ISSN 0028-0836 [dostęp 2016-03-25] (ang.).
- ↑ a b c Scott F. Gilbert, Developmental Biology, wyd. 10, 2013, s. 499-501, ISBN 978-0-87893-978-7.
- ↑ Scott F. Gilbert, Developmental Biology, wyd. 9, 2010, s. 697-698, ISBN 978-0878933846 (ang.).
- ↑ Jianfeng Zhu i inni, Bare Bones Pattern Formation: A Core Regulatory Network in Varying Geometries Reproduces Major Features of Vertebrate Limb Development and Evolution, „PLoS ONE”, 5, 2010, DOI: 10.1371/journal.pone.0010892, ISSN 1932-6203, PMID: 20531940, PMCID: PMC2878345 [dostęp 2016-03-25].
- ↑ a b Scott F. Gilbert, Developmental Biology, wyd. 10, 2013, s. 509-510, ISBN 978-0-87893-978-7.
- ↑ Aleksander Jamsheer. Genetyczne podłoże izolowanych wrodzonych wad dłoni. „Medycyna Wieku Rozwojowego”, s. 729-737, 3 grudnia 2008. (pol.).
- ↑ Dr med. Anna Materna-Kiryluk: Wrodzone wady rozwojowe twarzoczaszki i kończyn. [w:] Katedra i Zakład Genetyki Medycznej UM w Poznaniu, Materiały dydaktyczne [on-line]. kgm.ump.edu.pl. [dostęp 2014-08-25]. [zarchiwizowane z tego adresu (2014-08-26)]. (pol.).
- ↑ Hieronim Bartel: Embriologia. Wyd. IV. Warszawa: Wydawnictwo Lekarskie PZWL, 2007, s. 512-513.
- ↑ a b Brett A. Goodman, Pieter T. J. Johnson. Disease and the Extended Phenotype: Parasites Control Host Performance and Survival through Induced Changes in Body Plan. „PLOS (Public Library of Science)”, 2011-05-25. Internet Systems Consortium. DOI: 10.1371/journal.pone.0020193.
Bibliografia[edytuj | edytuj kod]
- Neil Shubin: Nasza wewnętrzna menażeria. Warszawa: Prószyński i S-ka, 2009, seria: Na ścieżkach nauki. ISBN 978-83-7648-098-5.
- P.C. Winter, G.I. Hickey, H.L. Fletcher: Krótkie wykłady : Genetyka. Warszawa: Wydawnictwo Naukowe PWN, 2003, seria: Na ścieżkach nauki. ISBN 83-01-13213-2.
Linki zewnętrzne[edytuj | edytuj kod]
- Limb Development na www.youtube.com
- Biologia rozwoju zwierząt D/Wykład 13. wiki.biol.uw.edu.pl. [zarchiwizowane z tego adresu (2014-08-26)]. w: Serwisy internetowe Uniwersytetu Warszawskiego > wiki Wydziału Biologii
- Randy L. Johnson and Clifford J. Tabin, Molecular Models for Vertebrate Limb Development (Review), Cell, Vol. 90, 979–990, September 19, 1997
- Homology in vertebrate limbs. truthinscience.org.uk. [zarchiwizowane z tego adresu (2015-10-18)]. na: Truth in Science (www.truthinscience.org.uk)
- MI Coates, MJ Cohn Fins, limbs, and tails: outgrowths and axial patterning in vertebrate evolution, BioEssays 20:371–381, 1998, John Wiley & Sons, Inc.
- Ilya Ruvinsky1, Jeremy J. Gibson-Brown, Genetic and developmental bases of serial homology in vertebrate limb evolution, Development 127, 5233-5244 (2000)
- Pownall ME, Isaacs HV., San Rafael (CA): Morgan & Claypool Life Sciences; 2010 FGF Signalling in Vertebrate Development Limb Development by Morgan & Claypool Life Sciences
- Origin of limbs in the evolutionary lineage of vertebrates, Universidad de Barcelona, ScienceDaily, 21 June 2012 <www.sciencedaily.com/releases/2012/06/120621125441.htm>
- K. D. Crow, C. D. Smith, J.-F. Cheng, G. P. Wagner, C. T. Amemiya. An independent genome duplication inferred from Hox paralogs in the American paddlefish-a representative basal ray-finned fish and important comparative reference. Genome Biology and Evolution, 2012; DOI: 10.1093/gbe/evs067
- Paddlefish's doubled genome may question theories on limb evolution, August 7, 2012
- Limb Development Duke University School of Medicine
- Gail R. Martin, The roles of FGFs in the early development of vertebrate limbs, Genes & Development, Cold Spring Harbor Laboratory Press
- Michael Bamshad, W Scott Watkins, Mary E Dixon, Trung Le, Amy D Roeder, Bridget E Kramer, John C Carey, Lynn B Jorde, Reconstructing the History of Human Limb Development: Lessons from Birth Defects, Pediatric Research (1999) 45, 291–299; doi:10.1203/00006450-199903000-00001










![Rzekotka królewska z dodatkową parą kończyn[43]](http://upload.wikimedia.org/wikipedia/commons/thumb/a/a8/P._regilla_with_parasite-induced_limb_malformation.png/120px-P._regilla_with_parasite-induced_limb_malformation.png)