Zapalenie kości i szpiku
| Osteomyelitis | |
 Zapalenie kości piszczelowej u małego dziecka | |
| Klasyfikacje | |
| ICD-10 | |
|---|---|
| DiseasesDB | |
| MedlinePlus | |
| MeSH | |
Zapalenie kości i szpiku (łac. osteomyelitis) – zróżnicowana grupa chorób spowodowanych rozwojem reakcji zapalnej w zakresie tkanki kostnej. Samo zapalenie oznacza zaburzenie równowagi fizykochemicznej komórek i tkanek o charakterze swoistym lub nieswoistym. W przypadku osteomyelitis dotyczy ono kości oraz szpiku kostnego. Znane jest od starożytności i pozostaje jedną z najtrudniejszych do wyleczenia chorób zakaźnych. Charakterystycznymi elementami obrazu jest postępująca degradacja kości i przebiegający podokostnowo proces wtórnego kostnienia. Drobnoustroje mogą dotrzeć do kości przez ciągłość z przyległych tkanek, wniknąć drogą krwionośną, albo zostać przeniesione w konsekwencji urazu lub zabiegu chirurgicznego.
Najczęściej izolowanym patogenem pozostaje gronkowiec złocisty (Staphylococcus aureus), bakteria posiadająca na swej powierzchni adhezyny, które ułatwiają przyleganie do białek i proteoglikanów macierzy kostnej. Leczenie polega na wdrożeniu antybiotykoterapii oraz (często) chirurgicznym opracowaniu rany.
Klasyfikacja[edytuj | edytuj kod]
Istnieją dwa sposoby klasyfikacji zakażeń. Schemat Cierny'ego i Madera uwzględnia lokalizację ogniska chorobowego oraz wydolność immunologiczną organizmu pacjenta. Dzięki temu pomaga w doborze odpowiedniego leczenia oraz ustaleniu prognozy. Lew and Waldvogel oceniają osteomyelitis pod względem czasu trwania, sposobu zakażenia oraz obecności objawów niewydolności naczyniowej. Koncentrują się tym samym na opisie etiologicznym, nie czyniąc sugestii co do metod terapeutycznych.
Zgodnie z klasyfikacją fizjologiczno-anatomiczną zaproponowaną przez Ciernego i Madera wyróżnia się cztery typy (pod względem anatomicznym) zapalenia kości i szpiku:
- typ I - wewnątrzszpikowy (jak w zapaleniu krwiopochodnym lub zakażeniu gwoździa śródszpikowego);
- typ II –powierzchowny (jak w ranach drążących);
- typ III – ograniczony (z pojedynczym martwakiem korowym)
- typ IV – rozlany (z zajęciem całego segmentu kości i kilkoma martwakami).
Ze względu na wiek osób dotkniętych chorobą rozróżnia się zapalenie kości i szpiku:
- niemowlęce (do 2 roku życia);
- dziecięce (do okresu pokwitania – dominująca liczba przypadków zachorowań);
- dorosły (każdy powyżej niemowlęcego i dziecięcego).
Z kolei przebieg choroby może mieć trojaki charakter:
- ostry
- podostry
- przewlekły
Patogeneza[edytuj | edytuj kod]
Szansę na zdobycie wiedzy o warunkach rozwoju choroby dają wyłącznie badania modeli eksperymentalnych. Wynika z nich, że zdrowa kość jest w dużym stopniu odporna na zakażenie. W warunkach prawidłowych kości nie mają bowiem kontaktu ze środowiskiem zewnętrznym. Dopiero wszczepienie znacznej ilości patogenów oraz wytworzenie lokalnego ogniska martwicy (wskutek urazu, operacji lub przez obecność ciała obcego) prowadzi do rozwoju choroby. Bakterie w rodzaju S. aureus, pochłonięte przez osteoblasty, mogą długo pozostawać przy życiu. Drobnoustroje przedostają się wtedy z krwią i limfą bądź przez rany pourazowe czy pooperacyjne do wnętrza organizmu. Zapalenie wywołane czynnikami wewnątrzpochodnymi może dotyczyć kilku kości, natomiast zewnątrzpochodne zazwyczaj ogranicza się do jednej kości. Krwiopochodne zapalenie kości zdarza się w przypadkach zakażeń ogólnych, ale ogniska zapalenia w kości mogą być tak małe, że nie dają wyraźnych objawów. Do powstania zapalenia przyczynia się także zmniejszona odporność ustroju i miejscowe zaburzenia w ukrwieniu. Zapalenie rozwija się w miejscach zwolnionego przepływu krwi przez naczynia włosowate. Miejscami tymi są przynasady u dzieci i nasady u dorosłych.
Wynikiem toczącego się procesu zapalnego jest zbieranie ropy, która zaczyna rozprzestrzeniać się siecią kanałów naczyniowych. Wzrost ciśnienia wywieranego na kość upośledza jej perfuzję i prowadzi do martwicy niedokrwiennej wskutek zaburzeń w odżywianiu. Resztki zniszczonej, oddzielającej się tkanki tworzą tzw. martwaki kostne (łac. sequestra). Zwykle ciągłość okostnej nie zostaje naruszona, a stopniowy nacisk, wywierany przez gromadzącą się ropę, sprzyja zewnętrznemu odkładaniu odczynowej masy kostnej (łac. involucrum). Stąd zapalenie kości i szpiku może prowadzić do resorpcji kości bądź jej stwardnienia. W przebiegu ostrego zapalenia przeważa naciek granulocytarny; po przejściu w stan przewlekły stopniowo jest on wypierany przez makrofagi i limfocyty. Widoczne staje się też postępujące włóknienie.
W 85% przypadkach zmiany chorobowe w ostrym zapaleniu kości (pierwotnie występujące zazwyczaj jako zapalenie szpiku) dotyczą kości długich, głównie kości udowych, piszczelowych, ramiennych i promieniowych. U małych dzieci zdarza się również zapalenie kilku kości.
Tabela 1. Najczęściej spotykane drobnoustroje chorobotwórcze
| Grupa wiekowa | Najczęsze patogeny |
|---|---|
| Noworodki | S. aureus, Enterobacter spp., Streptococcus spp. grupy A i B |
| Dzieci i młodzież | S. aureus, Enterobacter spp., Streptococcus spp. grupy A, Haemophilus influenzae |
| Dorośli | S. aureus, sporadycznie Enterobacter lub Streptococcus spp.; również Mycobacterium tuberculosis |
| Chorzy na anemię sierpowatokrwinkową | Salmonella spp., S. aureus |
Rozpoznanie[edytuj | edytuj kod]

Zakażenie kości i szpiku u osób dorosłych manifestuje się w sposób mało specyficzny jako przewlekły proces zapalny. Na stan patologiczny wskazuje bolesność zajętego miejsca, zwykle bez objawów układowych (gorączki, dreszczy czy potów). Nad kością może wytworzyć się przetoka skórna (w przypadku przewlekłego zapalenia kości i szpiku). Ból może być też sprzężony z obrzękiem, zaczerwieniem i ociepleniem zainfekowanego miejsca oraz ogólne złe samopoczucie. Z kolei u małych dzieci – jeszcze niemówiących – ból przy zapaleniu kości i szpiku mogą być manifestowane niechęć do poruszania chorą kończyną, unikanie chodzenia, utykanie, a także płacz przy dotykaniu i poruszaniu dotkniętą zmianami chorobowymi kończyną.
Rozpoznanie wstępne stawia się w oparciu o badania kliniczne. Potwierdzenie wymaga wykonania zdjęć radiologicznych oraz przeprowadzenia testów laboratoryjnych, z założeniem hodowli mikrobiologicznej włącznie. Zwykle podwyższone są wskaźniki stanu zapalnego (OB, CRP); rzadziej zachodzą zmiany w układzie leukocytarnym. Rutynowa fotografia RTG jest mało czuła, ale za to łatwa do realizacji. Metody medycyny nuklearnej używa się ze zmiennym szczęściem; powszechnie stosowanymi markerami pozostają białe krwinki wyznakowane związkami Tc-99, Ga-67 i In-111. Za najbardziej wartościowe uważa się badania obrazowe: tomografię komputerową, rezonans magnetyczny oraz pozytonową tomografię emisyjną.
Aby antybiotykoterapia przyniosła zamierzony efekt, należy wpierw zidentyfikować drobnoustrój chorobotwórczy. Materiał do analizy pobiera się drogą aspiracji igłowej albo zwykłej biopsji wycinającej; wymaz z przetoki może mieć również pewną wartość.
Leczenie[edytuj | edytuj kod]

Antybiotyk wprowadza się po pobraniu materiału do hodowli mikrobiologicznej. W większości wypadków równie istotnym elementem leczenia jest chirurgiczne opracowanie rany. Zwykle stosuje się środki bakteriobójcze, aplikowane w dużych dawkach drogą pozajelitową. Po opanowaniu procesu ostrego można przejść na środki przyjmowane doustnie. Pomimo wdrożenia skutecznego leczenia nawroty występują często, niekiedy aż w 20% przypadków.
Do najpowszechniej stosowanych leków należą β-laktamy i wankomycyna. Dobrym rozwiązaniem w wypadku infekcji gronkowcem jest użycie cefalosporyn albo penicylin penicylinazoopornych. Cechuje je niska toksyczność i spektrum działania obejmujące większość możliwych patogenów. Wankomycyna jest potrzebna do walki ze szczepami MRSA oraz enterokokami opornymi na ampicylinę.
Linezolid jest kolejnym, alternatywnym środkiem terapeutycznym. Ten lek przeciwbakteryjny z grupy oksazolidynonów wykazuje dobrą aktywność przeciwko rodzajom Staphylococcus, Streptococcus i szczepom VRA Enterococcus. Niestety, jego przewlekłe stosowanie wiąże się z ryzykiem poważnych działań niepożądanych: pancytopenią, neuropatią obwodową oraz zapaleniem nerwu wzrokowego. Z powyższych względów (oraz wysokiej ceny preparatu) wykorzystuje się go wyłącznie w wyjątkowych sytuacjach.
W przyszłości dużą rolę odegrać może odegrać daptomycyna, niedawno wprowadzona do użytku. Wykazuje skuteczność przeciwko organizmom Gram-(+). Przeprowadzone badania kliniczne wykazały korzyści z terapii łączonej, w której jednym ze składników była ryfampina – prawdopodobnie dzięki łatwości przenikania do wnętrza biofilmu kolonii bakteryjnych. Fluorochinolony mogą działać niekorzystnie na proces zrastania się złamanych kości, więc stosuje się je z dużą ostrożnością. Do leczenia zakażeń beztlenowcami (m.in. z rodzaju Bacteroides) nadaje się też metronidazol. Bardziej kontrowersyjna wydaje się kwestia doboru regimentu przy kontynuacji leczenia MRSA w warunkach ambulatoryjnych; używane są do tego, wybierane raczej arbitralnie, ko-trimoksazol, klindamycyna oraz pochodne tetracykliny.
Z powodu znacznych odczuć bólowych u pacjentów ze zdiagnozowanym zapaleniem kości i szpiku w leczeniu zachowawczym stosuje się również środki przeciwbólowe z grupy niesteroidowych leków przeciwzapalnych (NLPZ).
Optymalny czas prowadzenia farmakoterapii nie jest znany z powodu braku prospektywnych badań klinicznych z udziałem wystarczająco dużej liczby pacjentów. Wielu specjalistów prowadzi ją przez okres 4–6 tygodni, gdyż tyle trwa przywrócenie ukrwienia w opracowanej chirurgicznie ranie. Po wypisaniu ze szpitala przyjmowanie lekarstw drogą pozajelitową jest możliwe dzięki zastosowaniu wkłucia centralnego typu PICC (ang. peripherally inserted central catheter).
Dodatkowe możliwości terapeutyczne[edytuj | edytuj kod]
Terapia hiperbaryczna bywa stosowana jako środek wspomagający u pacjentów cierpiących na przewlekłe lub nawracające formy zapalenia kości. Istnieje przypuszczenie, że zwiększenie ciśnienia parcjalnego tlenu nasila aktywność fagocytarną granulocytów i przyśpiesza proces gojenia. W stosunku do organizmów beztlenowych wywierany jest bezpośredni efekt bakteriobójczy. Zebrane dowody potwierdzają szybsze tempo gojenia się wrzodów i zmniejszone ryzyko amputacji kończyny u tych chorych.
Do odkażania ran, szczególnie przed upowszechnieniem się chemioterapeutyków, wykorzystywano larwy muchy-plujki (tzw. "biochirurgia"). Potrafią one skutecznie oczyścić miejsce z martwych tkanek, a wydzielane przez nie substancje (m.in. alantoina) również przyśpieszają proces gojenia.
Zakażenia przenoszone przez ciągłość[edytuj | edytuj kod]
Rozległa kategoria zakażeń kości, spowodowanych ranami głębokimi: ukłuciami, ugryzieniami, złamaniami otwartymi. Zaliczają się do niej również powikłania pooperacyjne, np. po wstawieniu endoprotezy albo zabiegach dentystycznych. Immunosupresja i niewydolność naczyniowa zwiększają ryzyko takich komplikacji oraz znacznie utrudniają proces leczniczy.
Złamania otwarte[edytuj | edytuj kod]
W zależności od okoliczności zdarzenia i podjętych środków zaradczych, osteomyelitis bywa komplikacją złamań typu otwartego w 3–25% przypadków. Zwykle poszkodowanymi są młodzi mężczyźni poniżej 20. roku życia, którzy doświadczają urazu kości podudzia (piszczeli lub strzałki). Jeżeli nie zostanie wprowadzone odpowiednie leczenie, infekcja prowadzi do braku zrostu (ang. nonunion), przewlekłego zapalenia, a nawet amputacji.
Drobnoustrojami odpowiedzialnymi za zakażenie mogą być zarówno bakterie wchodzące w skład flory fizjologicznej skóry człowieka, organizmy żyjące w glebie, albo też patogeny odpowiedzialne za zakażenia szpitalne. Przeważają gronkowce i pałeczki Gram-(-); Mycoplasma spp. mogą powodować infekcje mostka po operacjach kardiochirurgicznych, Pseudomonas aeruginosa – infekcje kości stopy w wyniku przebicia podeszwy obuwia, Pasteurella multocida zaś – po ugryzieniu przez kotowate.
Do typowego postępowania należy: dokładne oczyszczenie zranionego miejsca, aplikację (zwykle i.v.) środków przeciwbakteryjnych, unieruchomienie/repozycję złamanej kości oraz zszycie naruszonych tkanek miękkich. Trwa dyskusja nad najbezpieczniejszym sposobem przeprowadzenia procedury ortopedycznej. Lokalne zmiany związane z poniesionym urazem powodują, że wykrywanie szerzącej się patologii za pomocą badań obrazowych jest trudne i niepewne. Po ukończeniu terapii antybiotykowej, w wypadku nawrotów zakażenia, miejsce złamania zostaje ponownie otworzone chirurgicznie, wszelkie ciała obce wraz ze zmianami usunięte, a po zabiegu ponownie wprowadza się antybiotykoterapię celowaną. Komplikacje zwykle nie grożą trwałym upośledzeniem funkcji kończyny.
Przewlekłe zapalenie kości[edytuj | edytuj kod]
Zakładając wczesne wprowadzenie odpowiedniej terapii, mniej niż 5% przypadków ostrego krwiopochodnego zakażenia kości staje się procesem przewlekłym. Ryzyko jest wyższe, jeżeli infekcja rozwinęła się przechodząc z sąsiednich struktur. Proces może zostać zauważony dopiero po latach od momentu zakończenia leczenia szpitalnego.
Główną przyczyną tak późnego wykrycia zmian (oprócz złego stanu opieki medycznej) jest brak objawów układowych infekcji, takich jak gorączka lub dreszcze. Z powodu upływu znacznej ilości czasu proces bywa miejscowo zaawansowany, a zmiany wtórne (sequestra, involucra, miejscowe przetoki) – dobrze wykształcone. Rzadziej dochodzi do złamań patologicznych, rozwoju raka kolczystokomórkowego skóry lub amyloidozy.
Zakażenia krwiopochodne[edytuj | edytuj kod]
Hematogenne infekcje kości, które mogą rozwinąć się w dowolnym miejscu ciała, są stosunkowo rzadkie. Choroba dotyka najczęściej dzieci przed okresem dojrzewania, osoby starsze, narkomanów stosujących zastrzyki dożylne oraz osoby z założonym wkłuciem centralnym. Zwykle zakażenie dotyczy kości długich; patomorfologia zmian zależy od wieku pacjenta. U dorosłych częściej zdarza się zakażenie krążków międzykręgowych, które zostanie omówione osobno.
Osteomyelitis u dzieci rozwija się w części przynasadowej kości (łac. metaphysis), czyli w miejscu, w którym chrząstka nasadowa (łac. cartilago epiphysialis) oddziela trzon kości od nasady. Intensywny proces wzrostu kości na długość, jaki się tutaj odbywa, wymaga stworzenia sieci naczyń kapilarnych, które dostarczałyby niezbędnych substancji odżywczych. Nawet drobny uraz może skutkować wytworzeniem krwiaka lub zatoru, który doprowadzi do ogniskowej martwicy. Naprawa szkód postępuje wolniej z uwagi na niedobór komórek fagocytarnych, które mogłyby na miejscu usunąć martwą tkankę. Takie warunki sprzyjają zasiedleniu przez drobnoustroje chorobotwórcze. Zarastanie chrząstek po ukończeniu dojrzewania pozbawia bakterie dogodnego miejsca inwazji; z tej przyczyny w późniejszym wieku choroba obejmuje albo trzon kości (łac. diaphysis) albo krążki międzykręgowe (łac. disci intervertebrale) kręgosłupa.
Zakażenia kręgosłupa[edytuj | edytuj kod]
Zakażenie kręgosłupa następuje zwykle drogą krwiopochodną i przybiera wiele form: zapalenia kości (łac. osteomyelitis vertebrae), zapalenia krążka międzykręgowego (łac. spondylodiskitis), ropnia nadtwardówkowego (łac. abscessus epiduralis), którym to mogą towarzyszyć podobne ropnie mięśni lędźwiowych i innych tkanek miękkich. Pierwotnym ogniskiem zakażenia bywa skóra wraz z tkanką łączną, układ moczowo-płciowy, płuca, zmienione zapalnie wsierdzie, miejsca po wkłuciach dożylnych, wreszcie ropnie w korzeniach zębów. Zakażeń jatrogennych w trakcie operacji można w dużym stopniu uniknąć stosując antybiotykoterapię prewencyjną.
Ból pleców i miejscowa tkliwość jest najbardziej typowym objawem choroby. Rzadziej rozwija się gorączka lub deficyty neurologiczne spowodowane uciskiem na rdzeń. Podniesione OB, dodatnie posiewy krwi oraz zmiany wykrywalne w badaniach komputerowych (MRI, Ga-67) potwierdzają podejrzenia. Interwencja chirurgiczna nie jest konieczna, jeżeli nie zachodzi ryzyko uszkodzenia rdzenia kręgowego. Również nie zaleca się usunięcia już założonego sprzętu ortopedycznego.
Zakażenia mykobakteriami[edytuj | edytuj kod]
Gruźlica rozwija się poza obszarem płuc w 20% wypadków. Zakażenia układu mięśniowo-szkieletowego dotyczą 1–5 procent chorych. Osteomyelitis, wynikający z rozsiewu prątków drogą krwionośną (albo siecią naczyń limfatycznych), rozprzestrzenia się w odcinku piersiowym kręgosłupa albo przestrzeniach okołostawowych. Taki rodzaj choroby może sugerować zebrany wywiad epidemiologiczny, pozytywny wynik testu tuberkulinowego, obciążające zdjęcia RTG klatki piersiowej oraz trudności w hodowli mikrobiologicznej.
Gruźlica kręgosłupa (in. choroba Potta, szczególnie jeżeli ropnie uciskają rdzeń kręgowy) występuje najczęściej. Diagnozę opóźnia brak objawów układowych. Ból pleców i ich sztywność mogą być jedynymi oznakami choroby; później rozwija się skrzywienie kręgosłupa. Rozpoznanie stawia się po wykryciu uszkodzeń kostnych oraz ropni w badaniach obrazowych, poprzez posiew prątków.
Spotyka się również zakażenia prątkami niegruźliczymi, szczególnie u pacjentów z upośledzoną odpornością bądź po przebytych operacjach. Do rodzajów mykobakterii, które mogą być odpowiedzialne za rozwój zapalenia, zalicza się: M. avium-intracellulare, M. kansasii, M. marinum, M. fortuitum, M. chelonae, M. xenopi. Notowano przypadki rozsianych zakażeń prątkami M. bovis szczepu Calmette-Guérin po odbytym szczepieniu BCG. Takie nieprzewidziane komplikacje każą podejrzewać obecność któregoś z rzadkich, dziedzicznych zespołów niedoboru odporności komórkowej.
Terapia lekami przeciwprątkowymi zazwyczaj kończy się sukcesem. W trudniejszych wypadkach dodatkowo miejsce zakażenia opracowuje się w sposób chirurgiczny. Reżim terapeutyczny nie różni się od tego stosowanego w klasycznych przypadkach mykobakterioz.
Zmiany kostne w przebiegu kiły[edytuj | edytuj kod]
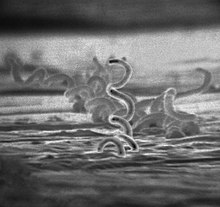
Zakażenia kostne mogą powodować krętki kiły (Treponema pallidum) oraz malinicy (in. frambezji, Treponema pertenue). Pomimo wzrostu liczby notowanych przypadków kiły do zmian kostnych dochodzi rzadko, ponieważ normalnie choroba jest wykrywana już we wczesnym etapie. Obecność krętków w materiale badawczym można potwierdzić barwiąc preparaty mikroskopowe specjalnymi metodami.
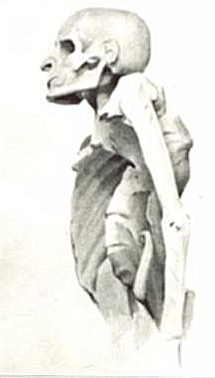
W kile wrodzonej krętki zajmują tkankę kostną od piątego miesiąca ciąży, zaburzając proces kostnienia na podłożu chrzęstnym (oddzielenie nasad od trzonów kości – łac. epiphyseolysis). Zniekształcenie struktury kości ma również miejsce w kile trzeciorzędowej (według Stachury także drugorzędowej), kilka lat po pierwotnym zakażeniu. Najbardziej charakterystycznymi zmianami morfologicznymi są: ogniska martwicze – kilaki (łac. gummata), podudzia szablaste (ang. saber shin) oraz deformacje kości twarzy.
Inne rodzaje zakażeń kości[edytuj | edytuj kod]
Chorzy na cukrzycę[edytuj | edytuj kod]
Według aktualnych statystyk 15% cukrzyków doświadczy w swoim życiu owrzodzeń stóp (tzw. stopa cukrzycowa) a 6% będzie wymagało z tego powodu hospitalizacji. Tego typu zmiany stanowią sprzyjające podłoże do rozwoju zakażeń tkanek położonych głębiej, włączając w to kości. Pierwszym symptomem bywa narastająca opuchlizna palców, ostre zapalenie tkanki łącznej (łac. cellulitis acuta) i zmiany osteolityczne na zdjęciach RTG. Leczenie jest bardzo trudne; stosuje się antybiotyki o możliwie szerokim spektrum działania.
Osoby poddawane hemodializie[edytuj | edytuj kod]
Długotrwała hemodializa również zwiększa ryzyko nabycia osteomyelitis drogą krwionośną. Najczęstszym patogenem jest S. aureus, często przejawiający oporność na oksacylinę.
Osoby chore na anemię sierpowatokrwinkową[edytuj | edytuj kod]
Pacjenci są obciążeni zwiększonym ryzykiem zakażeń kości długich, ostrego zakażenia drogą krwionośną, septycznego zakażenia stawów. Oprócz S. aureus często notuje się przypadki infekcji bakteriami Salmonella spp. W większości wypadków chorują dzieci. Do niepokojących objawów należą: ból kości, gorączka, dreszcze i leukocytoza.
Osoby stosujące narkotyki dożylne[edytuj | edytuj kod]
Wykonywanie zastrzyków sprzyja rozprzestrzenianiu się rozmaitych patogenów drogą krwionośną; stan zapalny może też objąć miejsca iniekcji. Zakażenia zlokalizowane są często w nietypowych miejscach, a drobnoustrojami za nie odpowiedzialnymi mogą być: S. aureus, Pseudomonas spp., Candida spp. i M. tuberculosis. Charakterystyczne są infekcje pałeczkami Eikenella corrodens, będącymi częścią normalnej mikroflory: dochodzi do nie poprzez zwilżanie śliną sprzętu lub skóry przed ukłuciem (ang. needle licker osteomyelitis). Pod uwagę była brana również Burkholderia cepacia.
SAPHO: Syndrome and Chronic Recurrent Multifocal Osteomyelitis[edytuj | edytuj kod]
Przewlekłe, wieloogniskowe zapalenie kości i szpiku (SAPHO, od łac. Synovitis, Acne, Pustulosis, Hyperostosis et Osteitis) to nawracająca choroba o nieokreślonej przyczynie. Obejmuje najczęściej kości ściany klatki piersiowej, miednicy i kręgosłupa. Jednocześnie współwystępuje przeciętnie około pięć zmian. Badania histopatologiczne są nierozstrzygające, hodowla nie prowadzi do izolacji hipotetycznego patogenu. Antybiotyki wydają się być nieskuteczne; w leczeniu próbowano stosować m.in. NLPZ, pamidronian, kortykosterydy, sulfadiazynę, metotreksat i INF-γ.
Ropień Brodiego[edytuj | edytuj kod]
Ropień Brodiego jest dobrze otorbioną zmianą ropną zlokalizowaną zwykle w okolicy przynasadowej kości piszczelowej, udowej lub kościach stawu skokowego. Powoduje podostry stan zapalny, z gorączką, bólami kończyny i wyczuwalnym uniesieniem okostnej. Przy przejściu w stan przewlekły (manifestującego się m.in. postępującym kostnieniem ściany) jedyną utrzymującą się dolegliwością pozostaje tępy ból.
Choroba Garré'go[edytuj | edytuj kod]
Stwardniające zapalenie kości szczęki lub żuchwy, w przebiegu którego wytwarza się duża ilości masy kostnej.
Grzybicze zapalenie kości i szpiku[edytuj | edytuj kod]
Osteomyelitis będąca wynikiem infekcji grzybami jest rzadko spotykana. Wśród opisywanych przypadków przeważają blastomykozy oraz rozsiane formy kokcydiomykozy i sporotrychozy. Wykrywano sporadycznie obecność grzybów rodzaju: Cryptococcus, Candidia i Aspergillus. Zanieczyszczenie ran pourazowych sprzyja zalęgnięciu się pleśni Pseudallescheria boydii, Scedosporium prolificans i Fusarium spp.
Niepowodzenie w identyfikacji patogenu[edytuj | edytuj kod]
W pewnych okolicznościach materiały pobrane do hodowli mogą nie wykazać obecności drobnoustrojów chorobotwórczych. Jeżeli badanie kliniczne, rezultaty badań radiologicznych oraz analiza histopatologiczna przemawia za zapaleniem, przyczynami mogą być: ropień Brodiego, zawały kości w przebiegu choroby Gauchera oraz anemia sierpowatokrwinkowa. Należy rozważyć użycie podłoży specjalnych, przeznaczonych dla mykobakterii i grzybów. Przy braku trywialnych rozwiązań problemu można uciec się do wysokospecjalistycznych analiz molekularnych (PCR z zastosowaniem bakteryjnego 16S rRNA)
Zobacz też[edytuj | edytuj kod]
- Choroby związane z osteomyelitis:
- Inne nienowotworowe patologie kości:
- Leki stosowane w przebiegu zapalenia kości i szpiku:
- antybiotyki beta-laktamowe
- wankomycyna
- penicyliny
- linezolid
- niesteroidowe leki przeciwzapalne
- tetracykliny
- klindamycyna
- ko-trimoksazol
Bibliografia[edytuj | edytuj kod]
- 103. Osteomyelitis. W: Mandell, Gerald L, Bennett, John E: Mandell, Douglas, and Bennett's principles and practice of infectious diseases 7ed. Philadelphia: Elsevier Inc., 2010. ISBN 978-0-4430-6839-3.
- Budowa ogólna kości. W: Adam Bochenek, Michał Reicher: Anatomia Człowieka. T. I. Warszawa: PZWL, 1990. ISBN 83-200-1628-2.
- 120. Osteomyelitis. W: Anthony S. Fauci, Dennis L. Kasper, Eugene Braunwald: Harrison's Principles of Internal Medicine 17ed.. New York: McGraw-Hill, 2008. ISBN 0-07-164114-9.
- T. Gaździk, Podstawy ortopedii i traumatologii narządu ruchu, Wydawnictwo Lekarskie PZWL, Warszawa 2001, ISBN 83-200-3317-9
- Wolfgang Rüdiger Hepp, Hans Ulrich Debrunner, Diagnostyka w ortopedii, Tadeusz Szymon Gaździk (red.), Rafał Rokicki (tłum.), Warszawa: Wydawnictwo Lekarskie PZWL, 2008, ISBN 978-83-200-3416-5, OCLC 833278125.
- Nimesulid (opis profesjonalny) [w:] Medycyna Praktyczna. [dostęp 2014-02-14].
