Estry
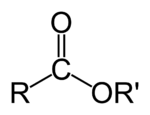
Estry (od niem. Essigäther – octan etylu, Essig – ocet i Äther – eter[1]) – grupa organicznych związków chemicznych będących produktami kondensacji kwasów i alkoholi lub fenoli. Komponentami kwasowymi mogą być zarówno kwasy karboksylowe, jak i kwasy nieorganiczne.
Bezpośrednia reakcja między kwasem karboksylowym i alkoholem nazywa się estryfikacją. Reakcja ta jest odwracalna, zachodzi w środowisku kwaśnym.
- R1
COOH + R2
OH ⇄ R1
COOR2
+ H
2O
Równowagę tej reakcji można przesunąć w prawo (w kierunku tworzenia estru) przez usuwanie jednego z produktów, wody lub estru, ze środowiska reakcji, np. przez destylację lub zastosowanie dodatkowego reagenta konsumującego wodę.
Estry niższych kwasów karboksylowych i alkoholi alifatycznych o krótkich łańcuchach węglowych są cieczami słabo mieszającymi się z wodą, o intensywnym i dość przyjemnym zapachu. Są one jednak w większych dawkach toksyczne, a niektóre są też rakotwórcze. Estry te są stosowane jako rozpuszczalniki organiczne o średniej polarności.
Estry kwasów karboksylowych z długimi grupami alkilowymi, czyli zawierające wyższe kwasy tłuszczowe lub wyższe alkohole alifatyczne, są głównymi składnikami wosku naturalnego. Z kolei estry wyższych kwasów tłuszczowych i gliceryny to tłuszcze.

W organizmach żywych poza licznymi estrami kwasów karboksylowych, powszechnie występują estry kwasu fosforowego, np. nukleotydy i kwasy nukleinowe (DNA, RNA). Estry kwasu azotowego są często nietrwałe i mogą mieć właściwości wybuchowe, np. nitroceluloza i nitrogliceryna.
Otrzymywanie[edytuj | edytuj kod]
Estry powstają np. w reakcji alkoholi z kwasami, chlorkami kwasowymi, bezwodnikami kwasowymi i innymi pochodnymi kwasów. Estry można też otrzymać z innych estrów w reakcji transestryfikacji, tj. wymiany reszty alkoholowej estru wyjściowego.
Właściwości fizyczne[edytuj | edytuj kod]
Estry niższych kwasów karboksylowych i alkoholi są cieczami trudno rozpuszczalnymi w wodzie, o intensywnym i dość przyjemnym zapachu, toksyczne w większych dawkach. W miarę wzrostu długości łańcucha zmienia się ich stan skupienia od cieczy, przez gęste oleiste płyny, do ciał stałych. Estry wyższych kwasów są bezwonne i nierozpuszczalne w wodzie. Estry kwasów tłuszczowych i gliceryny to tłuszcze. Temperatury topnienia i wrzenia estrów są niższe niż odpowiednich kwasów karboksylowych. Przyczyną tej różnicy jest fakt, że cząsteczki estrów nie zawierają grupy −OH i nie mogą tworzyć wiązań wodorowych między sobą. W wodzie rozpuszczają się jedynie estry o niskich masach molowych (dzięki tworzeniu wiązań wodorowych między –COO– a cząsteczkami wody). Są dobrymi rozpuszczalnikami dla związków organicznych.
Właściwości chemiczne[edytuj | edytuj kod]
Estry w wodzie ulegają hydrolizie (dla estrów kwasów karboksylowych reakcja ta bywa nazywana zmydlaniem) z różną szybkością, zależną od budowy estru. Reakcja ta może być katalizowana zarówno przez kwasy, jak i zasady.
Zapach estrów[edytuj | edytuj kod]
Wiele estrów kwasów karboksylowych wykazuje intensywny, przyjemny zapach. Najliczniejszą grupą tego rodzaju estrów są pochodne kwasu octowego i kwasu masłowego:
-
Maślan butylu (zapach ananasa)
-
Octan izoamylu (zapach bananów)
-
Octan oktylu (zapach pomarańczy)
-
Octan benzylu (zapach jaśminu)
Lista zapachów wybranych estrów[edytuj | edytuj kod]
| Ta sekcja od 2019-04 wymaga zweryfikowania podanych informacji. |



