Aminokwasy
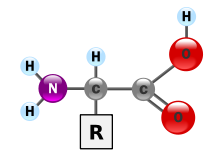
Aminokwasy (aa, AA[1], z ang. amino acids), kwasy aminowe – grupa organicznych związków chemicznych zawierających zasadową grupę aminową oraz kwasową grupę karboksylową −COOH, lub w ujęciu ogólniejszym, dowolną grupę kwasową[2].
Przykładem aminokwasu zawierającego grupę sulfonową –SO3H jest tauryna (kwas 2-aminoetanosulfonowy), natomiast zawierającego grupę fosfonową −C−PO3H2 jest ciliatyna[3] (kwas 2-aminoetanofosfonowy).
Grupa aminowa może być pierwszorzędowa (–NH2), drugorzędowa (–NHR), trzeciorzędowa (–NR2) lub czwartorzędowa amoniowa (–NH3+). Aminokwasy z czwartorzędową grupą amoniową to związki z grupy betain[4], a ich przedstawicielem jest N,N,N-trimetyloglicyna (betaina), (CH3)3N+CH2COO−.

Ponieważ aminokwasy zawierają zarówno grupę kwasową, jak i zasadową, zachodzi w nich wewnątrzcząsteczkowa reakcja kwas–zasada i związki te istnieją głównie w formie jonów obojnaczych. Jony obojnacze aminokwasów są rodzajem soli wewnętrznych (amfolitami), dlatego mają wiele właściwości typowych dla soli: są substancjami krystalicznymi o wysokich temperaturach topnienia, wykazują duże momenty dipolowe, są rozpuszczalne w wodzie, ale nierozpuszczalne w węglowodorach[5].
Kryteria podziału aminokwasów
Aminokwasy karboksylowe można podzielić na[4]:
- naturalne
- białkowe
- pierwszorzędowe (standardowe, kodowane) – 20 (21 włączając selenocysteinę) aminokwasów, które stanowią substraty w rybosomalnej syntezie białka
- drugorzędowe – powstające w wyniku postrybosomalnej modyfikacji (np. 4-hydroksyprolina)
- trzeciorzędowe – powstające w procesie postrybosomalnej modyfikacji w wyniku reakcji prowadzących do utworzenia niepeptydowych wiązań kowalencyjnych pomiędzy resztami aminokwasów wchodzących w skład białka np. cystyna
- niebiałkowe (np. kwas γ-aminomasłowy (GABA))
- białkowe
- syntetyczne (np. β-metylofenyloalanina)
Biorąc pod uwagę chemiczną budowę, aminokwasy karboksylowe można podzielić wedle:
- położenia grupy aminowej względem karboksylowej[4]: α, β, γ, δ i ε-aminokwasy; litera grecka określa położenie grupy aminowej przy danym atomie węgla w łańcuchu głównym kwasu karboksylowego. W α-aminokwasach obie te grupy funkcyjne znajdują się przy tym samym atomie węgla (α).
- polarności łańcucha bocznego, w przypadku standardowych aminokwasów[6]:
- z niepolarnym łańcuchem bocznym (glicyna, alanina, walina, leucyna, izoleucyna, metionina, prolina, fenyloalanina, tryptofan)
- z polarnym łańcuchem bocznym, ale nie posiadające formalnego ładunku (seryna, treonina, asparagina, glutamina, tyrozyna, cysteina)
- z polarnym łańcuchem bocznym posiadające ładunek formalny w fizjologicznym zakresie pH:
- z ładunkiem dodatnim (lizyna, arginina, histydyna)
- z ładunkiem ujemnym (kwas asparaginowy, kwas glutaminowy)
Aminokwasy naturalne

Znanych jest ponad 300 aminokwasów występujących naturalnie. W skład białek wszystkich organizmów żywych wchodzi głównie 20 aminokwasów, będących α-aminokwasami zawierającymi asymetryczny atom węgla o konfiguracji L (poza achiralną glicyną), a także niewielkie ilości wielu innych, w większości będących pochodnymi aminokwasów podstawowych. Łańcuch boczny (R) może zawierać takie elementy strukturalne, jak pierścień aromatyczny, łańcuch alifatyczny, siarkę (grupę tiolową lub tioeterową), grupę wodorotlenową, dodatkową grupę aminową bądź karboksylową. Są podstawowymi jednostkami budulcowymi peptydów i białek. Zazwyczaj są rozpuszczalne w wodzie i w warunkach fizjologicznego pH występują w formie jonowej.
Rodzaj reszt aminokwasowych i ich kolejność w łańcuchu polipeptydowym (sekwencja) zależy od kodu genetycznego zapisanego w DNA. Kolejne reszty aminokwasowe w łańcuchu polipeptydowym połączone są ze sobą za pomocą wiązań peptydowych.
Zobacz też
Przypisy
- ↑ Robert Kincaid Murray, Daryl K. Granner, Victor W. Rodwell: Biochemia Harpera ilustrowana. Wyd. VI uaktualnione. Warszawa: Wydawnictwo Lekarskie PZWL, 2008, s. 335, 384 i in. ISBN 978-83-200-3573-5.
- ↑ Przemysław Mastalerz, Chemia Organiczna, PWN Warszawa 1986, s. 966.
- ↑ Paulina Majewska, Biotransformacje hydroksyfosfinianów z asymetrycznym atomem fosforu, praca doktorska, s. 6, Politechnika Wrocławska, Wrocław 2006.
- ↑ a b c Aleksander Kołodziejczyk, Naturalne związki organiczne, PWN Warszawa 2003, s. 11, ISBN 978-83-01-143169.
- ↑ John McMurry, Chemia Organiczna, PWN, Warszawa 2007, s. 986, ISBN 978-83-01-14404-3.
- ↑ Donald Voet: Bichemistry. Wiley, 2004, s. 69. ISBN 0-471-39223-5.
