Dwutlenek węgla w atmosferze Ziemi: Różnice pomiędzy wersjami
| [wersja przejrzana] | [wersja przejrzana] |
| Linia 86: | Linia 86: | ||
Prowadzone są badania nad organizmami fotosyntezującymi w oceanach, zaobserwowano że fotosyntezę ograniczają niedobory niektórych pierwiastków niezbędnych do rozwoju [[fitoplankton]]u, takich jak [[azot]], [[fosfor]] i [[żelazo]]. Próby [[Zasiewanie żelazem|nawożenia żelazem]] wód oceanicznych przynosiły zwiększony wzrost fitoplanktonu i wiązania węgla w ich organizmach. |
Prowadzone są badania nad organizmami fotosyntezującymi w oceanach, zaobserwowano że fotosyntezę ograniczają niedobory niektórych pierwiastków niezbędnych do rozwoju [[fitoplankton]]u, takich jak [[azot]], [[fosfor]] i [[żelazo]]. Próby [[Zasiewanie żelazem|nawożenia żelazem]] wód oceanicznych przynosiły zwiększony wzrost fitoplanktonu i wiązania węgla w ich organizmach. |
||
== Wpływ zwiększenia stężenia {{chem2|CO2}} na rośliny == |
|||
Badania prowadzone w szklarniach wykazały, że podwojenie stężenia {{chem2|CO2}} stymuluje wzrost różnych gatunków roślin średnio o 37%. Przy czym wpływ zwiększenia stężenia {{chem2|CO2}} różnił się znacznie w zależności od gatunku, niektóre wykazywały znacznie większe przyrosty, a niektóre nawet mniejsze. Na przykład podwojenie {{chem|CO2}} spowodowało, że przyrost suchej masy roślin bawełny podwoił się, ale dla kukurydzy przyrost wyniósł tylko 20%<ref>{{Cytuj | autor = Hendrik Poorter | tytuł = Interspecific variation in the growth response of plants to an elevated ambient CO2 concentration | url = http://www.science.poorter.eu/1993_poorter_vegetatio.pdf | czasopismo = Vegetatio | numer = 104/105 | data = 1993 | s = 77-97}}</ref><ref>{{Cytuj | autor = S.C. Wong | tytuł = Elevated Partial Pressure of CO2 and Plant Growth | czasopismo = Oecologia | wolumin = 44 | data = 1979 | s = 68-74 | doi = 10.1007/BF00346400 | pmid = 28310466 | język = en}}</ref>. |
|||
Oprócz badań w szklarni, pomiary terenowe i satelitarne próbują określić wpływ zwiększonego {{chem2|CO2}} w naturalnym środowisku. W eksperymentach wzbogacania dwutlenkiem węgla wolnego powietrza, rośliny uprawia się na polach, a w otaczającym je powietrzu zwiększa się stężenie {{chem2|CO2}}. W tych eksperymentach rośliny wykazują mniejsze przyrosty wzrostu niż w badaniach szklarniowych, podobnie jak w badaniach w szklarniach zauważono różne przyrosty dla różnych gatunków roślin. Przy {{chem2|CO2}} w stężeniu 475–600 ppm, zauważono średni wzrost plonu o 17%, przy czym rośliny strączkowe zazwyczaj wykazywały większą odpowiedź niż inne gatunki, a rośliny C4 ogólnie wykazywały mniej<ref>{{Cytuj | autor = Lisa Ainsworth | tytuł = What have we learned from 15 years of free-air CO2 enrichment (FACE)? A meta-analytic review of the responses of photosynthesis, canopy properties and plant production to rising CO2. | czasopismo = New Phytologist | wolumin = 165 | data = 18.11.2004 | doi = 10.1111/j.1469-8137.2004.01224.x | pmid = 15720649 | język = en}}</ref>. |
|||
Wyrażana jest hipoteza mówiąca, że zwiększenie poziomu {{chem2|CO2}} może mieć negatywny wpływ na jakość odżywczą niektórych roślin. Zwiększenie fotosyntezy zwiększy ilość węglowodanów, takich jak glukoza, przy jednoczesnym pozostawieniu lub obniżeniu ilości ważnych składników odżywczych, takich jak białko, żelazo i cynk. Uprawy, w których zauważono spadek białka, obejmują ryż, pszenicę, jęczmień i ziemniaki<ref>{{Cytuj | autor = Helena Bottemiller Evich | tytuł = The great nutrient collapse. The atmosphere is literally changing the food we eat, for the worse. And almost nobody is paying attention. | url = http://www.politico.com/agenda/story/2017/09/13/food-nutrients-carbon-dioxide-000511 | opublikowany = Politico - The Agenda | data = 13.09.2017}}</ref>. |
|||
Pomiary satelitarne i badania naziemne prowadzone w ciągu ostatnich 35 lat wykazały wzrost wskaźnika powierzchni liści dla 25% - 50% obszarów wegetacyjnych Ziemi, podczas gdy mniej niż 4% powierzchni wykazuje zmniejszenie zazielenienia (brązowienie), co dowodzi istnieniu dodatniej korelacji między stężeniem {{chem2|CO2}} w atmosferze a fotosyntezą. Symulacje z wieloma modelami globalnego ekosystemu sugerują, że efekty nawożenia {{chem2|CO2}} wyjaśniają 70% zaobserwowanego trendu zazieleniania<ref>{{Cytuj | autor = Z. Zhu, S. Piao, R. Myneni i inni | tytuł = Greening of the Earth and its drivers. | czasopismo = Nature Climate Change | numer = 6 | data = 25.04.2016 | s = 791–795 | issn = 1758-6798 | doi = 10.1038/nclimate3004}}</ref>. |
|||
== Zmiany stężenia {{Chem|CO|2}} w atmosferze == |
== Zmiany stężenia {{Chem|CO|2}} w atmosferze == |
||
Wersja z 22:23, 20 lis 2019

Dwutlenek węgla w atmosferze Ziemi – dwutlenek węgla CO
2 w atmosferze ziemskiej jest gazem śladowym, zajmując około 0,04% (400 ppm) jej objętości.
Pomimo tak małego stężenia odgrywa ważną rolę, jest integralną częścią obiegu węgla w przyrodzie, w którym węgiel jest wymieniany między atmosferą a oceanami, glebą, skałami i biosferą. Rośliny i inne fotoautotrofy wykorzystują energię słoneczną do produkcji węglowodanów z atmosferycznego dwutlenku węgla i wody poprzez fotosyntezę. Niemal wszystkie organizmy zależą od węglowodanów pochodzących przeważnie z fotosyntezy jako głównego źródła energii i związków węgla[1].
CO
2 pochłania i emituje promieniowanie podczerwone w zakresach, w których jest ono przepuszczane przez inne gazy atmosfery, w związku z czym jest gazem cieplarnianym, odgrywając znaczącą rolę we wpływie na temperaturę powierzchni Ziemi poprzez efekt cieplarniany[2].
Około 4 mld lat temu był jednym z głównych składników atmosfery tworzącej się Ziemi i utrzymywał się w znacznych ilościach aż do związania węgla przez organizmy fotosyntezujące[3]. W kolejnych okresach historii Ziemi stężenie CO
2 w jej atmosferze zmieniało się w szerokich granicach. Stężenia CO
2 w atmosferze zmieniało się, osiągając 4000 ppm (10 razy więcej niż obecne) w okresie kambryjskim około 500 milionów lat temu, a spadając do 180 ppm podczas zlodowacenia plejstocenu około dwa miliony lat temu[4].
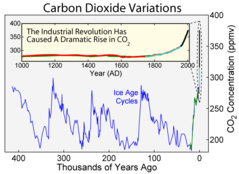
Przez dłuższy czas w neogenie stężenie wahało się wokół 280 ppm, wzrost stężenia rozpoczął od czasu rewolucji przemysłowej na początku XIX w. W związku z antropopresją stężenie CO
2 w atmosferze wzrosło o ponad 45%, z poziomu 280 ppm utrzymującego się w ciągu 10 000 lat aż do połowy XVIII wieku[4] do 415 ppm w maju 2019 r[5]. Obecne stężenie jest najwyższe od 14 milionów lat, wzrost ten przypisuje się działalności człowieka, w szczególności wylesianiu i spalaniu paliw kopalnych[6]. Wzrost CO
2 i innych gazów cieplarnianych w ziemskiej atmosferze spowodował wzrost temperatury zwany globalnym ociepleniem. Wzrost stężenia CO
2 w atmosferze zwiększa jego stężenie w wodach śródlądowych i oceanach, w tworząc kwas węglowy powoduje zakwaszanie wód[7].
Zagadnieniami ograniczania emisji CO2 zajmują się również liczne organizacje społecznościowe, np. Friends of the Earth International (w jej ramach m.in. Friends of the Earth Europe lub Peoples Climate Movement, organizujący m.in. marsze protestacyjne[8]).
Obecne stężenie

2 w zależności od pory roku i szerokości geograficznej.
Stężenie dwutlenku węgla w atmosferze w przeszłości wykazało kilka cykli zmian od około 180 części na milion podczas głębokich zlodowaceń holocenu i plejstocenu do 280 części na milion (ppm) w okresach między zlodowaceniami. Od rozpoczęcia intensywnego rozwoju przemysłu stężenie atmosferycznego CO2 wzrastało sukcesywnie do ponad 400 ppm i nadal rośnie. W kwietniu i maju 2019 r. średni miesięczny poziom CO2 w ziemskiej atmosferze przekroczył 411 ppm[9]. Stężenie 410 ppm w atmosferze odpowiada około 3200 mld ton CO2, zawierając około 870 GtC (870 mld ton węgla = 8,7·1014 kg)[a]. Globalne średnie stężenie CO2 rośnie obecnie w tempie około 2 ppm/rok i wzrost ten przyspiesza[9]. Roczna fluktuacja stężenia wynosi około 3–9 ppm, osiągając na półkuli północnej maksimum na przełomie kwietnia i maja a minimum w październiku[9]. Największe zmiany CO2 w cyklu rocznym są na półkuli północnej, im dalej na południe tym zmiany w ciągu roku są coraz mniejsze i mogą osiągać maksimum w innych miesiącach.
Globalny budżet CO2, obieg węgla
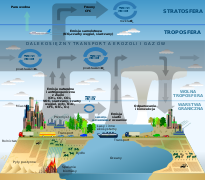
Atmosferyczny dwutlenek węgla odgrywa ważną rolę w obiegu węgla na Ziemi, w którym dwutlenek węgla jest usuwany z atmosfery za pomocą naturalnych procesów, takich jak fotosynteza, rozpuszczanie w wodzie czy osadzanie się węglanów, oraz dodawany do atmosfery naturalnych procesów, takich jak oddychanie i uwalnianie dwutlenku węgla z osadów węglanowych, oraz działalności człowieka, takich jak spalanie paliw kopalnych i zmiany w użytkowaniu ziemi. Wyróżnia się: szybki cykl węglowy i wolny cykl węglowy. Szybki cykl węglowy odnosi się do przemieszczania się węgla między środowiskiem a żywymi organizmami w biosferze, podczas gdy wolny cykl węglowy obejmuje ruch węgla między atmosferą, oceanami, glebą, skałami i wulkanizmem. Oba cykle węglowe są ze sobą ściśle powiązane, a przepływ węgla w postaci gazowego dwutlenek węgla przez atmosferę jest elementem cyklu[10].
Ilość przepływającego węgla do i z atmosfery szacuje się w zależności od rozpatrywanego przepływu. Emisje pochodzący ze spalania paliw kopalnych (EFF) określa się na podstawie statystyk wydobycia i zużycia kopalin. Emisje wynikające z użytkowania gruntów i zmiany użytkowania gruntów (ELUC), określa się na podstawie modeli uwzględniających wylesiania, użytkowanie gruntów produkcji rolnej i pod zabudowę. Pochłanianie CO
2 w oceanie (SOCEAN) i na lądzie (SLAND) są szacowane na podstawie modeli globalnych procesów z uwzględnieniem obserwacji, w tym np. satelitarnych stężenia dwutlenku węgla w atmosferze oraz zazielenienia powierzchni[1].
Opracowany przez Earth System Science Data globalny budżet węgla wskazuje, że w dziesięcioleciu 2008–2017 bilans przepływów dwutlenku węgla związane z atmosferą, w przeliczeniu na zawarty w nich węgiel wyniosły[1]:
- Emisje CO
2 ze spalania z paliw kopalnych (EFF) – 9,4 ± 0,5 GtC/rok, - Emisje wynikające z użytkowania gruntów i zmiany użytkowania gruntów (ELUC) – 1,5 ± 0,7 GtC/rok,
- Pochłanianie CO
2 przez ocean (SOCEAN) – 2,4 ± 0,5 GtC/rok - Pochłanianie CO
2 na lądach (SLAND) – 3,2 ± 0,8 GtC/rok, - Zmiana ilości dwutlenku węgla w atmosferze (GATM) – 4,7 ± 0,02 GtC/rok,
Nierównowaga budżetu węgla (BIM) jest różnicą między szacowanymi całkowitymi emisjami a szacowanymi zmianami w atmosferze, przepływami do oceanu i biosfery lądowej, jest miarą niedoskonałych danych i zrozumienia współczesnego cyklu węglowego[1].
Uwzględniając dokładności danych, powyższy bilans wykazuje niezrównoważenie równe 0,5 GtC/rok. Wskazuje to na zawyżenie emisji lub niedoszacowanie pochłaniania[1].
Budżet dla roku 2017 podaje wartości: EFF – 9,9±0,5 GtC/rok, ELUC – 1,4±0,7 GtC/rok, GATM – 4,6±0,2 GtC/rok, SOCEAN – 2,5±0,5 GtC/rok, SLAND – 3,8±0,8 GtC/rok, a BIM – 0,3 GtC/rok[1].
Porównanie roku z dziesięcioleciem wskazuje na znaczący wzrost emisji ze spalania kopalnych źródeł energii[1].
Model przepływów w atmosferze CT2017 opracowany przez NOAA umożliwia określenie źródeł emisji i pochłaniania CO2 w atmosferze. Według tego modelu emisje CO
2 ze spalania paliw kopalnych (EFF)rosły w latach 2000–2016 z 6,7 do 9,9 mld ton węgla. Emisje te koncentrują się na obszarach o dużej gęstości zaludnienia i aktywności gospodarczej w północnej strefie umiarkowanej. Drugim ważnym źródłem CO
2 są pożary, które dodają do atmosfery rocznie 1,9–2,3 mld ton węgla. Większość tych emisji pochodzi ze strefy tropikalnej i południowej[11].
Biosfery lądowe i oceany pochłaniają i emitują dwutlenek węgla do atmosfery, w sumie są one pochłaniaczami. Biosfera lądowa (SLAND) wykazuje pochłanianie netto od 2,4 do 5,1 mld ton węgla, oceany (SOCEAN) zaś od 1,6 do 3,0 mld ton węgla. Ilość węgla wiązanego przez ekosystemy lądowe zależy od przebiegu pogody w danym roku, dobre warunki do rozwoju roślin zwiększają pochłanianie, a susze na dużym obszarze zmniejszają. Model wykazuje, że tereny intensywnej działalności rolniczej są dużymi pochłaniaczami CO
2, podczas gdy strefa lasów tropikalnych jest oceniana jako źródło dwutlenku węgla w ilości 0,4–0,8 mld ton węgla. Woda oceaniczna ma mniejsze stężenie CO
2 niż równowagowe odpowiadające stężeniu CO
2 w atmosferze, przez co woda oceaniczna pochłania dwutlenek węgla. Część pochłoniętego przez wodę dwutlenku węgla zwiększa jego stężenie w wodzie, część jest pobierana przez glony, a część jest wiązane w wyniku reakcji chemicznych z minerałami. Niemal połowa węgla ze źródeł antropogenicznych jest pochłaniana przez biosferę i oceany, pozostała zwiększa stężenie dwutlenku węgla w atmosferze[11].
Z wyjątkiem spalania paliw i emisji wynikającej ze zmian użytkowania gruntów, wszystkie pozostałe ośrodki zarówno dostarczają, jak i pobierają dwutlenek węgla z atmosfery.
| Naturalne | Antropogeniczne | Łącznie | Bilans | |||||
|---|---|---|---|---|---|---|---|---|
| Źródło/Ujście | Oznaczenie | do | od | do | od | do | od | |
| Spalanie paliw | EFF | 0 | 0 | 9,4 | 0 | 9,4 | 0 | 9,4 |
| Zmiana użytkowania gruntu | ELUC | 0 | 0 | 1,5 | 0 | 1,5 | 0 | 1,5 |
| Pochłanianie przez lądy | SLAND | 120 | 120 | 0 | 3,2 | 120 | 123,2 | -3,2 |
| Pochłanianie przez oceany | SOCEAN | 90 | 90 | 0 | 2,4 | 90 | 92,4 | -2,4 |
| Razem | 210 | 210 | 10,9 | 5,6 | 220,9 | 215,6 | 5,3 | |
Łączna ilość emisji CO
2 wynosząca 221 GtC/rok, przy zawartości CO
2 w atmosferze wynoszącym 860 GtC oznacza, że cząsteczka CO
2 przebywa średnio w atmosferze niecałe 4 lata[1].
CO
2 a efekt cieplarniany

2

Naturalny efekt cieplarniany na Ziemi sprawia, że życie jest takie, jakie znamy, a dwutlenek węgla odgrywa znaczącą rolę w zapewnieniu wysokiej temperatury, jaka jest na Ziemi. Oddziaływanie obecnych w atmosferze gazów cieplarnianych na temperaturę powierzchni Ziemi polega na zmniejszeniu promieniowania elektromagnetycznego z zakresu podczerwieni, wypromieniowywanego z powierzchni Ziemi w kierunku przestrzeni kosmicznej. Powoduje to podwyższenie temperatury powierzchni i atmosfery planety do takiej, w której uzyskiwana jest równowaga między energią docierającą do globu ze Słońca przez promieniowanie słoneczne a odprowadzaną w przestrzeń kosmiczną przez promieniowanie podczerwone. [2].
Absorpcja promieniowania zachodzi wtedy, gdy energia fotonów odpowiada różnicy między dozwolonymi poziomami energetycznymi, które mogą zająć elektrony w atomach lub fragmenty cząsteczki, wzbudzane do drgań lub obrotów. Absorpcja promieniowania podczerwonego przez cząsteczki CO2 jest związana z ich wzbudzaniem do drgań zginających i rozciągających cząsteczkę. Wzbudzenie drgań zginających symetrycznych i niesymetrycznych odpowiada energii promieniowania elektromagnetycznego o długości fali około 15 μm, odpowiada mu pasmo absorpcyjne wokół tej długości fali, pasmo to leży w pobliżu maksimum emisji energii cieplnej przez powierzchnię Ziemi, do tego w zakresie 12–15 μm, leży w obszarze, w którym para wodna nie pochłania promieniowania, przez co obecność dwutlenku węgla w atmosferze zmniejsza wypromieniowywanie ciepła w przestrzeń kosmiczną[12]. Same drgania symetryczne nie mogą być wzbudzone przez pochłonięcie fotonu, ponieważ wzbudzenie ich nie powoduje zmian momentu dipolowego cząsteczki[13][14].
Chociaż para wodna jest odpowiedzialna za większość (około 36-70%) całkowitego efektu cieplarnianego Ziemi, to wielkość ta nie jest bezpośrednio związana z działalnoscią człowieka a zależy od temperatury atmosfery. Na Ziemi dwutlenek węgla jest najbardziej istotnym, bezpośrednio wpływającym antropologicznie gazem cieplarnianym. W 2017 roku wzrost wzrost stężenia CO
2 od początku rozwoju przemysłu (1750 r.) jest odpowiedzialny za 2,013 W/m² z całego 3,062 W/m² wymuszania radiacyjnego na Ziemi, to jest około 66%[15].
Dwutlenek węgla a fotosynteza

2 jest redukowany w cyklu Calvina z wytworzeniem cukrów prostych.

W ekosystemach współczesnej biosfery atmosferyczny dwutlenek węgla odgrywa kluczową rolę w cyklach biogeochemicznych. Rośliny lądowe pobierają dwutlenek węgla bezpośrednio z atmosfery, a wodne rozpuszczony w wodzie. CO
2 jest substratem fotosyntezy fotosyntezy, w wyniku której węgiel jest włączany do związków organicznych, zazwyczaj glukozy, zwiększając ilość węgla organicznego. Sumaryczny przebieg reakcji[16]:
- 6H
2 + hν (energia świetlna) → C
6H
12O
6 + 6O
2↑
Głównym procesem odwrotnym, w którym węgiel ze związków organicznych jest utleniany, a produktem reakcji jest CO
2 jest oddychanie komórkowe, prowadzące do rozwoju komórek, jak i do biodegradacji. Przykładowa reakcja pełnego utleniania glukozy[16]:
- C
6H
12O
6 + 6O
2 → 6H
2O + 6CO
2↑ + (energia)
Niemal całość ze 120 GtC pochłanianych przez lądy i większość z 90 GtC pochłanianych przez oceany jest przekształcana przez fotosyntezę z dwutlenku węgla na związki organiczne węgla. Organizmy fotosyntezujące są fotoautotrofami, syntezują związki odżywcze bezpośrednio z CO
2 i wody wykorzystując energię światła. Ogólny proces fotosyntezy jest podobny u roślin, glonów i cyjanobakterii, ale szczegóły jego przebiegu są różne. U roślin występuje kilka odmian fotosyntezy i kilka procesów fizycznych związanych z przebiegiem fotosyntezy. Główne typy fotosyntezy określane są jako fotosynteza C3 i C4. Fotosynteza C4 oraz kilka innych cech roślin wykształciły się jako przystosowanie roślin do wysokiego natężenia światła, podwyższonej temperatury (ponad 20 °C) i suszy. Wydajność fotosyntezy roślin typu C4 jest 1,5 - 2 razy większa od roślin typu C3, szczególnie w wyższej temperaturze i przy niedoborze wody. Wydajność większości roślin C4 spada w niższej temperaturze i około 15 °C oba typy są tak samo wydajne[17]. Rośliny ze ścieżką fotosyntetyczną C4 dominują w tropikalnych sawannach i łąkach, a wśród roślin uprawnych w między innymi kukurydza, trzcina cukrowa, wśród drzew paulownia. Rośliny typu C4 jako wydajniejsze od C3 są wykorzystywane jako źródło paszy i biomasy, w warunkach pogodowych takich jak w Polsce największe plony uzyskuje się z kukurydzy, uprawa której umożliwia uzyskanie do 15 ton ziarna lub 25 ton suchej biomasy z jednego hektara[18].
Trwają prace nad wiązaniem węgla przez fotosyntezę zwane biosekwestracją. Wyhodowano krzyżówkę paulowni o szczególnie dużym przyroście zwaną drzewem tlenowym, którego uprawy są zakładane w Europie[19]. Przeniesieniem niektórych cech roślin C4 do roślin uprawnych C3 celem poprawy ich wydajności. Takie zmodyfikowane genetycznie rośliny określane są jako C4-like[20].
Prowadzone są badania nad organizmami fotosyntezującymi w oceanach, zaobserwowano że fotosyntezę ograniczają niedobory niektórych pierwiastków niezbędnych do rozwoju fitoplanktonu, takich jak azot, fosfor i żelazo. Próby nawożenia żelazem wód oceanicznych przynosiły zwiększony wzrost fitoplanktonu i wiązania węgla w ich organizmach.
Wpływ zwiększenia stężenia CO
2 na rośliny
Badania prowadzone w szklarniach wykazały, że podwojenie stężenia CO
2 stymuluje wzrost różnych gatunków roślin średnio o 37%. Przy czym wpływ zwiększenia stężenia CO
2 różnił się znacznie w zależności od gatunku, niektóre wykazywały znacznie większe przyrosty, a niektóre nawet mniejsze. Na przykład podwojenie CO2 spowodowało, że przyrost suchej masy roślin bawełny podwoił się, ale dla kukurydzy przyrost wyniósł tylko 20%[21][22].
Oprócz badań w szklarni, pomiary terenowe i satelitarne próbują określić wpływ zwiększonego CO
2 w naturalnym środowisku. W eksperymentach wzbogacania dwutlenkiem węgla wolnego powietrza, rośliny uprawia się na polach, a w otaczającym je powietrzu zwiększa się stężenie CO
2. W tych eksperymentach rośliny wykazują mniejsze przyrosty wzrostu niż w badaniach szklarniowych, podobnie jak w badaniach w szklarniach zauważono różne przyrosty dla różnych gatunków roślin. Przy CO
2 w stężeniu 475–600 ppm, zauważono średni wzrost plonu o 17%, przy czym rośliny strączkowe zazwyczaj wykazywały większą odpowiedź niż inne gatunki, a rośliny C4 ogólnie wykazywały mniej[23].
Wyrażana jest hipoteza mówiąca, że zwiększenie poziomu CO
2 może mieć negatywny wpływ na jakość odżywczą niektórych roślin. Zwiększenie fotosyntezy zwiększy ilość węglowodanów, takich jak glukoza, przy jednoczesnym pozostawieniu lub obniżeniu ilości ważnych składników odżywczych, takich jak białko, żelazo i cynk. Uprawy, w których zauważono spadek białka, obejmują ryż, pszenicę, jęczmień i ziemniaki[24].
Pomiary satelitarne i badania naziemne prowadzone w ciągu ostatnich 35 lat wykazały wzrost wskaźnika powierzchni liści dla 25% - 50% obszarów wegetacyjnych Ziemi, podczas gdy mniej niż 4% powierzchni wykazuje zmniejszenie zazielenienia (brązowienie), co dowodzi istnieniu dodatniej korelacji między stężeniem CO
2 w atmosferze a fotosyntezą. Symulacje z wieloma modelami globalnego ekosystemu sugerują, że efekty nawożenia CO
2 wyjaśniają 70% zaobserwowanego trendu zazieleniania[25].
Zmiany stężenia CO2 w atmosferze
Pierwsza, druga i trzecia atmosfera
Wiedza o atmosferze Ziemi w okresie jej powstawania i jej wczesnych przemianach jest niepełna, wiąże się ona z wciąż doskonalonymi teoriami o ewolucji gwiazd, powstawaniu i ewolucji Układu Słonecznego i planet tego układu, w tym planet grupy ziemskiej[b].
Proces ewolucji ziemskiej atmosfery był wieloetapowy, wyróżniane są okresy[26][3][27][28]:
- „atmosfera pierwotna” (ang. Primary atmosphere), zawierająca głównie wodór i hel, utracona wkrótce po uformowaniu się Układu Słonecznego[c][29][30]
- „pierwsza atmosfera” – atmosfera utworzona około 4 mld lat temu (hadeik), przed osiągnięciem przez Słońce pełnej dojrzałości (zob. paradoks słabego, młodego Słońca[31]), przez odgazowanie stopionej materii bombardującej powierzchnię Ziemi (okres powstawania skorupy ziemskiej[32][33]) oraz przez gazy wyrzucane z głębi podczas erupcji wulkanicznych (zob. też Wielkie Bombardowanie). Prawdopodobnie około 90% tych gazów stanowiły: para wodna[d] (ok. 4/5 atmosfery) i dwutlenek węgla; towarzyszyły im m.in. metan[e] oraz siarkowodór, amoniak, tlenek węgla, azot i in. Duży udział pary wodnej w atmosferze był konsekwencją wysokiej temperatury.
- „druga atmosfera” – atmosfera utworzona po kondensacji większości pary wodnej, zawierająca głównie dwutlenek węgla (część CO2 rozpuściła się w wodzie i reagowała z zasadami co spowodowało tworzenie skał chemogenicznych np. wapieni)
- „trzecia atmosfera” – atmosfera zawierająca tlen, umożliwiająca życie na lądzie[3]
b, c – Ziemia, trzecia planeta Układu Słonecznego, krąży od 4,567 mld lat po orbicie eliptycznej o zmiennej ekscentryczności i nachyleniu względem ekliptyki; zmienne są również parametry precesji osi.
d – Zmiany położenia względem Słońca, wyjaśniające okresowe zmiany klimatu nazywane cyklami Milankovicia, prawdopodobnie sumowały się z cyklicznymi zjawiskami geologicznymi (zob. wędrówka kontynentów i cykl superkontynentalny, tektonika płyt, tętno Ziemi)
e – W czasie przemieszczania się poszczególnych fragmentów skorupy ziemskiej zachodzi subdukcja – zagłębianie się oceanicznej płyty litosfery (A) pod płytę kontynentalną (B) wskutek konwekcji w płaszczu (C). Przetapiane skały płyty oceanicznej ulegają kolejnym przemianom cyklu skalnego. Na wypiętrzanej granicy płyty kontynentalnej powstają łańcuchy górskie z licznymi wulkanami (np. pacyficzny pierścień ognia). Stężenie CO2 w atmosferze rośnie w czasie gwałtownych erupcji wulkanów, a obniża się w wyniku wietrzenia skał[34]. Szybkość karbonatyzacji jest bardzo zależna od klimatu (występują dodatnie sprzężenia zwrotne)[35].
Początkiem przemiany drugiej atmosfery w trzecią było prawdopodobnie pojawienie się w paleoproterozoiku pierwszych organizmów zdolnych do fotosyntezy. Zgodnie z teorią endosymbiozy (zob. Lynn Margulis) fotoautotrofy powstały w sąsiedztwie kominów hydrotermalnych w wyniku symbiozy przodków współczesnych przedstawicieli Eucariota z przodkami współczesnych cyjanobakterii i bakterii purpurowych (późniejsze chloroplasty i mitochondria[36][37][38]). Wytwarzany tlen był toksyczny dla anaerobów (spowodował 2,4–2,0 mld lat temu katastrofę tlenową). Długo nie przedostawał się do atmosfery, biorąc udział w reakcjach utleniania związków rozpuszczonych w wodzie morskiej. Produktem utleniania pochodzących z procesów hydrotermalnych soli żelaza Fe2+aq był tlenek żelaza(III), składnik wstęgowych rud żelazistych[3][39][40] (zob. żelazo w skorupie ziemskiej). Produktem życia sinic były też stromatolity, zbudowane z lamin węglanu wapnia. Prekambryjskie stromatolity z Zatoki Rekina i inne powstały w wyniku diagenezy, trwającej kilkaset milionów lat lub dłużej (np. stromatolid sprzed 3600–3200 mln lat z Pilbara)[41].
W kambrze rośliny zasiedliły lądy (sylur, dewon), co spowodowało dalszy wzrost stężenia tlenu w powietrzu (wkrótce rozpoczęła się eksplozja kambryjska)[40].
W kolejnych okresach dziejów Ziemi następowały znaczne, wzajemnie powiązane zmiany składu atmosfery, ziemskiego klimatu i gatunkowego składu biosfery (okresy wzrostu różnorodności biologicznej i masowego wymierania). Prawdopodobnie w późnym pliocenie, w warunkach stepowiejącego środowiska tropikalnej sawanny Afryki Wschodniej, rozpoczęła się antropogeneza – powstanie gatunku zdolnego do adaptacji do zmian warunków życia (zob. Homo przypadkiem sapiens), w tym zmian klimatu i wzrastającego zagęszczenia[f].
W XVIII wieku n.e. człowiek współczesny dokonał rewolucji przemysłowej, zwiększając emisje CO2 i przyspieszając naturalne zmiany klimatu i struktur ziemskich ekosystemów. Nasilił się też wpływ innych czynników antropogenicznych na środowisko (zob. środowisko antropogeniczne). Rozpoczął się proces nazwany „szóstym masowym wymieraniem”. Obserwowany jest też wyraźny niekorzystny wpływ zmian klimatu na zdrowie ludzi[42][43][44].
Atmosfera i klimat fanerozoiku
Rozwój życia spowodował, że skład ziemskiej atmosfery stał się zależny nie tylko od procesów astrofizycznych (np. cykle Milankovicia, zmiany aktywności Słońca), geologicznych (np. cykl superkontynentalny, wulkanizm) i geofizycznych (np. cykl skalny, cykl hydrologiczny), lecz dodatkowo od obiegu pierwiastków w cyklach biogeochemicznych. Odpowiedzialne za obieg węgla w przyrodzie procesy biologiczne – przebiegające z bezpośrednim lub pośrednim udziałem atmosferycznego CO2 – stały się ważnym czynnikiem zmienności ziemskiego klimatu[16]. Paleoklimatolodzy, podejmujący próby wyjaśnienia mechanizmu tej zmienności, są zmuszeni do korzystania z danych pośrednich (wskaźniki nazywane proxy) i z metody aproksymacji. Współcześni klimatolodzy korzystają z licznych wyników ilościowych pomiarów stężenia CO2 w atmosferze oraz z zaawansowanych matematycznych modeli klimatu (zob. poniżej: pomiary bezpośrednie i (zob. poniżej: pomiary bezpośrednie i modelowanie atmosfery i prognozowanie zmian).
Proxy klimatyczne
Pośrednich informacji o zmianach warunków życia na Ziemi dostarczają skamieniałości, które budziły zainteresowanie starożytnych i późniejszych filozofów (zob. historia paleontologii). Były opisywane przez Arystotelesa, Ksenofanesa, Marcjalisa i wielu innych. Mogli oni obserwować np. bryły węgla kamiennego, zawierające skamieniałości nieznanych roślin (współcześnie opisywanych jako produkty metamorfizmu torfu lub lignitu[45]), tworząc pierwsze opisy dawnego tropikalnego klimatu. Występujące na lądach ślady życia organizmów morskich mogły być również źródłem starych mitów o potopie, znanych na wszystkich kontynentach (zob. „historyczność” potopu).
Za twórcę współczesnej paleontologii jest uznawany Georges-Louis Leclerc (autor m.in. książki Histoire naturelle, générale et particulière contenant les époques de la nature, 1778[46]). Na przełomie XIX i XX w. Johannes H.F. Umbgrove (autor znanej książki „Tętno Ziemi”) stworzył podstawy geologii dynamicznej, paleontologii i stratygrafii. W tymże czasie opracowano teorie cykli Milankovicia, cykli oceanicznych Fischera, tektoniki płyt Wegenera (zob. wędrówka kontynentów, cykl superkontynentalny) i in. Pojawiła się możliwość stosowania nowych technik pomiarów (np. datowania izotopowego i wiekowej kalibracji tabeli stratygraficznej). Stały się dostępne metody analizy dużych zbiorów danych (zob. statystyka matematyczna, teoria prawdopodobieństwa), umożliwiające opracowywanie modeli ziemskiego klimatu (zob. poniżej: modelowanie atmosfery i prognozowanie zmian).



W latach 70. XX w. potwierdzono zgodność pośrednich danych, dotyczących klimatu Ziemi w fanerozoiku, z teorią Milankovicia[52]. Równocześnie z potwierdzeniem teorii została potwierdzona użyteczność danych proxy, uzyskiwanych np. w czasie badań rdzeni lodowych, pobieranych m.in. na antarktycznych stacjach Wostok, Concordia, Kohnen (zob. program EPICA) oraz w północnej i centralnej Grenlandii[53].
Datując zdarzenia z przeszłości Ziemi (zob. źródła danych, leżących u podstaw teorii Fischera)[g] stosuje się różne metody izotopowe. Polegają na wykorzystaniu właściwości izotopów:
- Charakterystycznego i niezależnego od wiązań chemicznych czasu połowicznego rozpadu izotopów promieniotwórczych.
- Jednym z przykładów jest datowanie radiowęglowe. Mierzona proporcja zawartości izotopu 14C do całej ilości węgla w próbce zależy od czasu, który upłynął od chwili pobierania CO2 do fotosyntezy z atmosfery do chwili badania jego szczątków lub szczątków pochodzących z niego materiałów (np. drewno, skóra). Takie postępowanie jest użyteczne w przypadku próbek o wieku < 40 tys. lat (maks. 60–70 tys. lat)[54].
- Efektów izotopowych polegających na różnicy dynamiki reakcji chemicznych i procesów fizycznych dla rożnych izotopów, prowadzące do różnic w składzie izotopowym substratów i produktów reakcji np. takich, których stosunek w próbkach charakteryzuje warunki w czasach historycznych, np.:
- – większe wartości stosunku 13C/12C lub wskaźnika δ13C[h] w próbkach osadów dennych oznaczają, że powstawały one w okresie pogrzebania dużych ilości materii organicznej, bez utlenienia do CO2 (do obiegu wraca mniej 12C, preferowanego przez rośliny morskie)[55]
- – większe wartości stosunku 18O/16O lub wskaźnika δ18O w próbkach z rdzenia lodowego oznaczają, że powstawały w okresie postępującego zlodowacenia. Z powierzchni łatwiej odparowuje woda z 16O. Jeżeli warunki sprawiają, że jest zatrzymywana (np. w lodzie na powierzchni), rośnie głębinowy wskaźnik δ18[h] w wodzie/lodzie lub skamieniałościach zamieszkujących ją organizmów (np. muszle małży, tj. rudysty, węglanowe skorupki otwornic w planktonie i bentosie[56][57][58][59].
Wyniki izotopowych badań rdzeni lodowych, osadów oceanicznych i innych próbek są gromadzone od ponad 50 lat[60][61][62][63][64]. W 2013 roku opublikowano m.in. wyniki pomiarów, wykonanych na Ziemi Baffina, które uznano za pierwszy bezpośredni dowód, że temperatury na obszarze północno-wschodniej Kanady są wyższe, niż w najcieplejszym okresie we wczesnym holocenie (9–5 tys. lat temu); Gifford Miller i wsp. stwierdzili, że nie mają one precedensu w ostatnich 120 tysiącach lat. Ostrzegają, że trwające topnienie lodu Ziemi Baffina nie zatrzyma się nawet wówczas, gdy zostanie zahamowane współczesne ocieplanie klimatu[65][66].
b, c – ostatnie 400 tys. lat (plejstocen, holocen); temperatura w kilku cyklach epoki lodowej (zob. mała epoka lodowa, Ziemia śnieżka[j], EPICA 2004) i stężenie CO2
Pomiary bezpośrednie
Różnorodne pomiary stężenia CO2 w powietrzu[72] obejmują m.in.:
- monitorowanie stężenia CO2 nad kontynentami i oceanami w sieciach laboratoriów naziemnych;
- satelitarne pomiary zawartości CO2 w słupie powietrza nad powierzchnią Ziemi;
- oznaczenia wielkości emisji z elektrowni, ciepłowni, elektrociepłowni, cementowni itp. i modelowanie rozprzestrzeniania się emitowanych zanieczyszczeń, badania przebiegu procesów oczyszczania gazów i sekwestracji dwutlenku węgla;
- badania emisji związanych z działalnością agrotechniczną i chowem zwierząt w fermach oraz oszacowania szybkości pochłaniania CO2 przez roślinność, wodę, gleby (naturalna sekwestracja);
- pomiary strumieni uwalnianych z różnych źródeł naturalnych (np. oddychanie, degradacja biomasy, wulkanizm) oraz pochłanianych w wyniku procesów naturalnych (np. wietrzenie skał, rozpuszczanie w wodzie oceanów, asymilacja), w tym pomiary „wymiany netto” w różnego rodzaju ekosystemach (NEE, ang. Net Ecosystem Exchange[73]), prowadzone z równoczesnym wykorzystaniem pomiarów naziemnych i satelitarnych[74][75]).
Wyniki pomiarów są gromadzone w specjalistycznych bazach danych, tj. baza IPCC i upowszechniane przez Data Distribution Centre[76] (różne rodzaje udostępnianych danych[77], obserwacje i prognozy dotyczące CO2[78]). Umożliwiają weryfikację modeli zmian stężenia atmosferycznego dwutlenku węgla i działania całego globalnego systemu klimatycznego. Weryfikacja prognoz wymaga interdyscyplinarnej współpracy geologów, geochemików, geofizyków, biologów i klimatologów[79]. Jest podstawą geoinżynierii i programów międzynarodowych działań, zmniejszających ryzyko katastrofy klimatycznej.
Laboratoria naziemne
Od lat 50. XX w. zmiany stężenia dwutlenku węgla w atmosferze są rejestrowane z użyciem metod ilościowej analizy chemicznej i instrumentalnej. Zostały podjęte przez Charlesa Keelinga (chemika zainteresowanego geologią). Keeling odbywał staż podoktorancki na utworzonym wówczas Wydziale Geochemii CalTech pod kierunkiem fizyka i geochemika Harrisona Browna (1917–1986)[80], bardzo zainteresowanego historią skorupy ziemskiej. Z inspiracji Browna rozpoczął sprawdzanie hipotezy, że stężenie węglanów w wodach gruntowych można oszacować, biorąc pod uwagę równowagę w układzie trójfazowym układzie wapienie–woda–powietrze (m.in. roztwarzanie CaCO3, rozpuszczanie CO2 z powstawaniem kwasu węglowego). Badania rozpoczął w laboratorium, stosując manometryczne i miareczkowe metody pomiarów, a następnie w warunkach środowiskowych (rejon Big Sur). Stwierdził potrzebę zgromadzenia dużego zbioru regularnych i wiarygodnych wyników pomiarów stężenia CO2 w powietrzu[81].


do badań kowariancji wirów (ang. Eddy covariance system, EC); zob. rys. schemat wirów nad lasem

W 1957 roku (Międzynarodowy Rok Geofizyczny) rozpoczęła działalność stacja pomiarowa z aparaturą do spektroskopii w podczerwieni, zlokalizowana w obserwatorium astronomicznym na szczycie Mauna Loa (Hawaiʻi)[81][82][83]. Próbki powietrza pobierano w sposób ciągły na szczycie pięciu wież (cztery 7-metrowe i jedna 27-metrowa). Próbki, pobierane co godzinę, przepływały z prędkością ok. 0,5 dm³/min przez kalibrowany co 30 min. analizator Siemens Ultramat 3 (spektrofotometr IR[86][87] z pułapką do wymrażania pary wodnej). W bazach danych gromadzono średnie wartości stężenia atmosferycznego CO2 oraz prędkość i kierunek wiatru[88][89]. Stacja w Mauna Loa działała od 1958 roku. Równocześnie z pomiarami stężenia dwutlenku węgla prowadzono badania roślinności otoczenia obserwatorium[90][91].
Wyniki pomiarów porównywano ze stężeniami CO2 w innych miejscach globu. W tym celu przewożono do laboratorium próbki powietrza, pobierane w sieci punktów SIO Air Sampling Network (Scripps Institution of Oceanography)[92]:
- Alert, NWT (Kanada)
- Point Barrow (Alaska od 1974)
- La Jolla Pier, od 1985
- Baja California Sur od 1997
- Cape Kumukahi (Hawaiʻi) od 1979
- Christmas Island 1975
- American Samoa
- Cape Matatula (Tutuila, Samoa)
- Kermadec Islands
- Baring Head (Wyspa Północna, Nowa Zelandia)
- Biegun południowy
Mimo wysokiej oceny znaczenia zgromadzonych danych, co znajduje wyraz m.in. w rosnącej liczbie cytowań, inne ośrodki długo nie podejmowały podobnych badań, wymagających wytrwałości i kosztownych[93].
Współcześnie pomiary stężeń CO2 i dynamiki strumieni, wymienianych między warstwami atmosfery lub między powietrzem i powierzchnią wody, gruntem oraz roślinnością ekosystemów, są prowadzone w setkach stacji monitoringu, m.in. zrzeszonych w sieciach międzykontynentalnych, tj. Fluxnet-Canada, AmeriFlux, LBA, CarboeuropeIP, NECC, Carboafrica i in.[94][95] (dostęp do zgromadzonych danych umożliwia FLUXNET Data Portal[95]).
W Polsce zintegrowany monitoring środowiska prowadzi m.in. Stacja Kompleksowego Monitoringu „Puszcza Borecka”, należąca do Instytutu Ochrony Środowiska w Warszawie (m.in. program EMEP)[96][97].
Trzyletni program badań wymiany gazowej pomiędzy powierzchnią ziemi a atmosferą na terenach bagiennych Biebrzańskiego Parku Narodowego (bilans absorpcji i emisji metanu, dwutlenku węgla i pary wodnej)[74][75] zrealizował Zespół Katedry Meteorologii i Klimatologii Wydziału Nauk Geograficznych Uniwersytetu Łódzkiego. Pomiary wykonywano m.in. mikrometeorologiczną metodą kowariancji wirów (ang. eddy covariance, EC)[98][99].
Poza metodą kowariancji wirów do bilansowania wymiany CO2 są stosowane[94][100]:
- komory zamknięte bez możliwości przepływu powietrza,
- komory zamknięte z możliwością przepływu powietrza,
- komory otwarte z możliwością przepływu powietrza,
- zautomatyzowane systemy komór otwartych z możliwością przepływu powietrza (ang. open-flow method),
- przenośne systemy pomiaru wymiany gazowej CO2, np. typu ACE (ang. Automatic CO2 Exchange System) lub SRS-1000 (przenośny Soil Respiration Systems[101]).
Pomiary są wykonywane m.in. w czasie badań procesu oddychania gleby[84][85] lub możliwości i szybkości adaptacji struktur różnych ekosystemów do zmian klimatu. Szybki wzrost stężenia CO2 może być dużym zagrożeniem dla ekologicznej równowagi ekosystemów leśnych (zob. sukcesja ekologiczna, klimaks, równowaga biocenotyczna)[102][103][104]. Prowadzone są również badania reakcji niektórych gatunków roślin uprawnych na zapowiadane podwojenie tego stężenia. W ZUT w Szczecinie zbadano np. reakcje wybranych genotypów rzepaku ozimego, wytypowanych ze względu na przewidywany rozwój produkcji biopaliw oraz wzrost popytu na wysokobiałkowe surowce do produkcji pasz. Stwierdzono m.in., że podwojenie stężenia dwutlenku węgla w atmosferze doświadczalnych minifitotronów przyczyniło się do zwiększenia powierzchni liści o ok. 47–126% i wzrostu zawartości chlorofilu o 6–21%. Świeża masa części nadziemnej wzrosła o 42–58%, a sucha masa o 64–96% (zależnie od odmiany)[105]. Nie jest pewne, czy zwiększone stężenie CO2 w atmosferze przełoży się na zwiększenie produktywności producentów pierwotnych. Z doświadczeń wynika, że pomimo zmian w składzie gatunkowym producentów pierwotnych w biocenozie pod wpływem zmian stężenia CO2 całkowita jej produktywność nie uległa zmianie[16].
Wyniki badań dotyczących poszczególnych gatunków roślin nie są wystarczające do określenia wpływu przewidywanego podwojenia stężenia CO2 na strukturę ziemskich biomów. Istnieje możliwość, że takie zmiany mogą np. wzmacniać niekorzystne oddziaływania gatunków inwazyjnych. Jednym z przykładów są trawy C4, które mogą stanowić zagrożenie dla bioróżnorodności pokrytego sawannami Cerrado[106][107].
Poza pomiarami w stacjach naziemnych oznaczenia stężeń CO2 w troposferze wykonuje się z użyciem urządzeń instalowanych w samolotach. Zbadano m.in. zależność tych stężeń od sezonu i zmian wydajności w rolnictwie, stwierdzając np. że wzrost produkcji kukurydzy, pszenicy, ryżu i soi na półkuli północnej o 240%, który nastąpił w latach 1961–2008, spowodował wyraźne zwiększenie ilości węgla wychwytywanego przez pola uprawne w okresie wegetacyjnym[108].
Obserwatoria satelitarne
Satelitarne obserwacje stężeń, źródeł emisji i miejsc pochłaniania CO2 rozpoczęto w latach 80. XX wieku z użyciem aparatury zainstalowanej na satelicie pogodowym NOAA-10 z serii TIROS (Television Infrared Observation Satellite). Za pierwszego satelitę, którego głównym celem były pomiary atmosferycznego CO2, jest uważany ADEOS I (NSDA, Japonia), wyniesiony na orbitę w 1996 roku przez H-II – japońską rakietę nośną firmy Mitsubishi[109]. ADEOS I był wyposażony (we współpracy międzynarodowej) w system AVNIR (ang. Advanced Visible and Near-Infrared Radiometer) do badań światła widzialnego (zakres 0,52–0,69 µm) i podczerwieni (zakresy 0,42–0,50, 0,52–0,60, 0,61–0,69 i 0,76–0,89 µm)[109][110][111][112]. Na początku XXI wieku rozpoczęły swoje misje: Aqua (2002), Aura (2004), PARASOL (2004), CALIPSO (2006), CloudSat (2006)[113]. Na początek 2009 roku zaplanowano umieszczenie na orbitach biegunowych synchronicznych ze Słońcem dwóch specjalistycznych satelitów. Były to:
- 23 stycznia 2009 – japoński Ibuki (GOSAT, Greenhouse Gases Observing Satellite); pomiary CO2, CH4, O2, O3, H2O[114][115]
- 24 lutego 2009 – amerykański OCO (Orbiting Carbon Observatory); urządzenia do pomiarów CO2 i O2[116][115]
Wyniesienie OCO nie powiodło się[116]. W lipcu 2014 roku został wyniesiony OCO-2 (Orbiting Carbon Observatory-2), wyposażony w udoskonaloną aparaturę[117]. W następnych latach do pierwszych satelitów systemu monitoringu atmosferycznego CO2 dołączyły kolejne. Stopniowo tworzono międzynarodową konstelację obiektów, wyposażonych w różnego typu urządzenia pomiarowe[118], nazwaną Afternoon Constellation lub A-Train[113].
Planuje się uruchomienie w 2020 roku Geostationary Carbon Cycle Observatory (GeoCARB), pierwszego obiektu umieszczonego na orbicie geostacjonarnej (zespół prowadzący: Uniwersytet Oklahomy, Institute for the Study of Earth, Oceans, and Space, kierownik: Berrien Moore). Przewidywane jest kontrolowanie stężenia CO2, CO i CH4 nad Ameryką Północną i Południową, miejsc emisji i pochłaniania tych gazów oraz fluorescencji indukowanej przez promieniowanie słoneczne (informacje o zmianach przebiegu fotosyntezy, związanych ze stanem roślinności)[119]. Przewiduje się, że od 2022 roku pomiary stężenia gazów cieplarnianych będzie wykonywać GOSat-3 (Greenhouse gases Observing SATellite-3, Ibuki 2)[120][121].
Modelowanie atmosfery i prognozowanie zmian
Obszerne bazy wyników pomiarów są powszechnie dostępne[122][123], co umożliwia opracowywanie modeli, pozwalających prognozować zmiany klimatu, zachodzące pod wpływem zmian emisji dwutlenku węgla (NOAA CarbonTracker wykonuje obliczenia na podstawie 397 zestawów danych pomiarowych z całego świata, pochodzących z 55 różnych laboratoriów)[124].
Matematyczne opisy zmian składu atmosfery, w tym zmian stężenia CO2, oparte na licznych danych proxy i prawach nauki (fizyki, chemii, biologii) są podstawą modeli ogólnej cyrkulacji i modeli ziemskiego systemu klimatycznego (wykorzystywanych m.in. w czasie międzynarodowych konferencji kimatycznych).

- Twórcy modeli i kontrowersje
Do czołówki geologów i geofizyków, zajmujących się komputerowym modelowaniem zmian stężenia atmosferycznego CO2 w fanerozoiku (m.in. rolą roślin w procesach wietrzenia skał krzemianowych[125]) jest zaliczany Robert Berner (1935–2015), autor licznych książek (m.in. Global Environment: Water, Air and Geochemical Cycles)[126] i wielu innych publikacji[127][79][128]. Dowodził m.in. że wyniki modelowania stężenia atmosferycznego CO2 z użyciem GEOCARB są w przybliżeniu zgodne z wartościami oszacowanymi w wyniku izotopowych badań skamieniałości roślin, co pozwala przypuszczać, że efekt cieplarniany był głównym czynnikiem kształtowania klimatu Ziemi przez ostatnie 600 mln lat[125]. Zamieszczony w Nature nekrolog R. Bernera opatrzono podtytułem Geochemik, który skwantyfikował cykl węglowy (ang. Geochemist who quantified the carbon cycle)[129].
Wielki wkład w badania czułości klimatu i wymuszania radiacyjnego, parametryzację procesów fizycznych w modelach ogólnej cyrkulacji itp. wniósł James Hansen, dyrektor Goddard Institute for Space Studies[130] w latach 1981–2013, autor książki Storms of My Grandchildren[131][132] i wielu artykułów naukowych[133][134][135][136]. Budową i weryfikacją modeli klimatycznych zajmowało się od lat 80. wielu innych naukowców, m.in. Michael Schlesinger[137][138][139] i John Mitchell (główny autor trzech raportów IPPC[140], współautor Climate model simulations of the equilibrium climatic response to increased carbon dioxide, Nature 1987)[141], B.D. Santer[142], Philip Jones i inni, m.in. współautorzy A search for human influences on the thermal structure of the atmosphere (Nature 1996). Podsumowując wyniki obszernych badań dotyczących okresu 1963–1987, uznano za prawdopodobne, że obserwowane zmiany klimatu są spowodowane działalnością człowieka, jednak wyrażono wątpliwości w odniesieniu do oszacowań zmienności naturalnej[143].
W 2011 roku, w czasie międzynarodowej konferencji nt. przeszłości i przyszłości klimatu, wykłady zaprezentowało 16 wybitnych paleoklimatologów. Ich stanowiska zostały opublikowane w specjalnym wydaniu Philosophical Transactions A (2013), zatytułowanym „Warm climates of the past – a lesson for the future?“[144]. Cztery lata później w tytule międzynarodowych warsztatów, które odbyły się w University of Bristol Cabot Institute, zastosowano tryb twierdzący: „Hothouse climates of the past – lessons for the future” (cieplarniane klimaty przeszłości – lekcja dla przyszłości). Stwierdzono m.in. że głównym powodem niebezpiecznego wzrostu temperatury jest wzrost stężenia dwutlenku węgla w atmosferze, stale notowany od czasu rewolucji przemysłowej[145].
Stopniowo udoskonalane i weryfikowane modele zostały zaakceptowane przez większość naukowców jako podstawa programów ochrony klimatu, lecz brakuje jednomyślności w sprawie stopnia wiarygodności prognoz[146] (zob. kontrowersje wokół globalnego ocieplenia, opinia naukowa o zmianie klimatu). Mniej liczni sceptycy[146] podkreślają, że ilość emitowanego CO2 jest tylko jednym z wielu zmiennych czynników, które powinny być uwzględniane w czasie prognozowania szybkości ocieplenia. Według części naukowców większą rolę mogą odgrywać zmiany aktywności Słońca (na które zwracano uwagę od początku prób modelowania[139]), chmury (zob. modyfikacje pokrywy, cirrusy i klimat), pyły i aerozole atmosferyczne, np. siarczanowe, wymiana gazów na powierzchni oceanów i aktywność oceanicznego fitoplanktonu[147], zmiany dynamiki prądów oceanicznych (zob. cyrkulacja termohalinowa, północnoatlantyckie wody głębinowe, NAO, El Niño i La Niña), subdukcja i wypiętrzanie się mas skalnych, wulkanizm itp. Sceptyczny wobec przypisywania głównej roli atmosferycznemu CO2 jest m.in. Michael Kelly – profesor fizyki w Uniwersytecie w Cambridge[148], członek Royal Society i Royal Academy of Engineering, który w 2000 roku brał udział w pracach niezależnego interdyscyplinarnego zespołu ekspertów (Climatic Research Unit), powołanego do przeanalizowania sprawy Climategate[149][150]. Kelly opisuje system klimatyczny jako „nieredukowalną złożoność” (analogia do pojęcia nieredukowalna złożoność w biologii)[151].
Robert Jastrow, amerykański astronom, fizyk i kosmolog (współzałożyciel George C. Marshall Institute) był również krytyczny wobec konsensusu naukowego w sprawie globalnego ocieplenia. Twierdził, że zmiany klimatu mogły mieć przyczyny naturalne[152]. Podobne stanowisko zajmował Zbigniew Jaworowski, polski lekarz-radiolog, kwestionujący poprawność datowania zdarzeń na podstawie badań rdzeni lodowych (zob. poglądy na temat ocieplenia klimatu)[153]. Również polski paleontolog Jerzy Dzik uważa, że ilość CO2 ponownie wprowadzanego do atmosfery z procesów spalania paliw kopalnych nie powinna zwiększyć stężenia w istotnym stopniu[154].
Po wielu latach badań i debat wiadomo, że osiągnięcie gwarantowanej sprawdzalności prognoz zmian klimatu nie jest możliwe (konieczne jest operowanie pojęciem obiektywnego prawdopodobieństwa). Tjeerd H. van Andel wyjaśnia to w epilogu do książki Nowe spojrzenie na Starą Planetę[155]: Szablon:CytatD Wiarygodne prognozowanie stężenia dwutlenku węgla w przyszłych dziesięcioleciach i stuleciach, umożliwiające racjonalną ochronę życia na planecie, dodatkowo utrudnia niepewność, dotycząca zmian wpływu antropogenicznego. Zależy on m.in. od szybkości rozwoju demograficznego oraz zmian potrzeb żywnościowych i energetycznych przyszłych mieszkańców Ziemi, kierunków i tempa rozwoju energetyki, przemysłu, rolnictwa i hodowli, skali degradacji naturalnych ekosystemów itp. Głód mieszkańców części obszarów (Róg Afryki, Etiopia i in.) sprzyja narastaniu niebezpiecznych konfliktów wewnętrznych i międzynarodowych oraz masowej emigracji. Rosnące zapotrzebowanie ludności państw uprzemysłowionych na energię jest trudno zaspokoić ze źródeł odnawialnych (zob. postulat 100% energii odnawialnej). Rozwojowi produkcji rolnej i hodowli często towarzyszy dewastacja naturalnych ekosystemów. Istotnymi składnikami diety mieszkańców rejonów zurbanizowanych są np. banany lub awokado[156], pochodzące z wielkoobszarowych plantacji na byłych terenach leśnych, zwanych „zielonymi płucami Ziemi”[157], lub mięso i mleko z masowej przemysłowej hodowli (zob. np. Meat Atlas, 2014[158]).
b – Wskazane jest upowszechnienie korzystania z odnawialnych źródeł energii i zastosowanie sekwestracja CO2 we wszystkich elektrowniach węglowych,
c – Zahamowanie wzrostu stężenia atmosferycznego dwutlenku węgla wymaga stałego kontrolowania i równoważenia wielkości strumieni CO2 wprowadzanych do atmosfery i pochłanianych z niej w skali lokalnej i globalnej.
Próby unormowania ochrony klimatu
W końcu XX w. przekonanie o względnej poprawności opracowanych modeli klimatycznych i o konieczności ograniczenia emisji dwutlenku węgla stało się niemal powszechne[159]. Próby wprowadzenia ograniczeń emisji podjęto pomimo braku całkowitej zgodności postaw naukowców w sprawie przyczyn ocieplenia, mimo konfliktów interesów między państwami znajdującymi się na różnym poziomie rozwoju i mimo świadomości, że osiągnięcie celu będzie trudne i kosztowne. W 2008 roku James Hansen pisał m.in., że całkowite wycofanie się w ciągu następnych 20–25 lat ze spalania węgla bez sekwestracji CO2 jest zadaniem herkulesowym; niezbędny wysiłek porównywał do poniesionego w czasie II wojny światowej, zwracając uwagę, że obecnie stawką jest życie na całej planecie[160][134].
- 1972 – Konferencja sztokholmska ONZ i UNEP
- 1988 – powołanie Międzynarodowego Zespołu ds. Zmian Klimatu (IPCC)
- 1989 – publikacja I raportu IPPC – pierwszego międzynarodowego porozumienia w sprawie zmian klimatu (podstawa do negocjacji Ramowej Konwencji ONZ)
- 1992 – Szczyt Ziemi 1992 w Rio de Janeiro i podpisanie Ramowej konwencji Narodów Zjednoczonych w sprawie zmian klimatu, która weszła w życie w 1994 roku, po ratyfikacji przez 50 krajów.
Od 1995 roku odbywają się coroczne spotkania sygnatariuszy i obserwatorów konwencji – Konferencje stron (Conferences of the Parties, COP)[161], organizowane w czasie kolejnych Konferencji Narodów Zjednoczonych w sprawie zmian klimatu, na których są opracowywane szczegóły dotyczące realizacji wspólnych postanowień oraz plany dalszych działań. Przedmiotem negocjacji są m.in. warunki handlu uprawnieniami do emisji, który uznano za ważny mechanizm działania.
- Konferencje stron (Conferences of the Parties, COP)[161]
- COP-1, Berlin 1995
- COP-2, Genewa 1996
- COP-3, Kioto 1997
- COP-4, Buenos Aires 1998
- COP-5, Bonn 1999
- COP-6, Haga 2000
- COP-7, Marrakesz 2001
- COP-8, Nowe Delhi 2002
- COP-9, Mediolan 2003
- COP-10, Buenos Aires 2004
- COP-11, Montreal 2005
- COP-12, Nairobi 2006
- COP-13, Bali 2007
- COP-14, Poznań 2008
- COP-15, Kopenhaga 2009
- COP-16, Cancún 2010
- COP-17, Durban 2011
- COP-18, Doha 2012
- COP-19, Warszawa 2013
- COP-20, Lima 2014
- COP-21, Paryż 2015
- COP-22, Marrakesz 2016
- COP-23, Bonn 2017
- COP-24, Katowice 2018
W programie Santiago Climate Change Conference (Santiago, grudzień 2019) znajduje się dwudziesta piąta konferencja stron (COP-25)[161].
Spośród wymienionych spotkań wyróżnia się konferencję w Kioto (COP-3), której efektem był Protokół z Kioto (1997), rozwijający konwencję ramową z 1992 roku. Ustalenia spełniły oczekiwania tylko połowicznie. Państwa rozwijające się nie zgodziły się na redukcję emisji, a przedstawiciele USA (25% światowej emisji CO2 w 1990 roku) stawiali warunek, że redukcję zadeklarują również państwa szybko rozwijające się (Chiny i Indie). Nieoczekiwanie ujawniono zakulisową umowę Japonii, USA i Kanady z Rosją, w której w latach 1990–1998 emisja zmniejszyła się o 30% (umowa dotyczyła handlu niewykorzystanymi limitami emisji)[163]. W załączniku B do „Protokołu” wymieniono kraje, które zobowiązały się do określonego ograniczenia emisji gazów cieplarnianych, liczonego jako wartość średnioroczna z okresu 2008–2012 odniesiona do wartości z 1990 roku (łącznie co najmniej o 5,2%). Mimo sprzeciwów autorów i sygnatariuszy petycji oregońskiej „Protokół z Kioto” wszedł w życie 16 lutego 2005 roku, po ratyfikowaniu przez 141 państw, wytwarzających 61% światowej emisji gazów cieplarnianych[162].
Za bardzo owocne uznaje się spotkanie COP-21 w Paryżu (2015). Już przed konferencją 187 krajów dobrowolnie zobowiązało się do redukcji emisji w okresie 2020–2030 (INDC, Intended Nationally Determined Contributions). Realizacja tych zobowiązań pozwoliłaby obniżyć temperaturę o 2,7–3,5 °C już do końca stulecia[109]. Tak zwane „Porozumienie paryskie”, podpisane 22 kwietnia 2016 roku i wkrótce ratyfikowane przez Unię Europejską (5 października 2016), określane jako „pierwsze powszechne i prawnie wiążące światowe porozumienie dotyczące klimatu”[164][165], zawiera m.in. sformułowania: Szablon:CytatD
Fakty i mity
Wpływ stężenia atmosferycznego CO2 i innych gazów cieplarnianych na klimat oraz potrzeba ograniczania ich emisji jest tematem licznych publikacji naukowych oraz opracowań popularnonaukowych (fakty)[166]. Poza nimi rozpowszechniane są również opinie, uznawane przez specjalistów za groźne mity, które łatwo trafiają do czytelników, zagubionych wśród nadmiaru faktów. W atmosferze gorączkowej „energetyczno-klimatycznej przepychanki”[167][168] część ludzi zadaje pytania: „Czy naukowcy sfabrykowali dane, żeby obronić tezę o globalnym ociepleniu i własne posady?”, „Czy cała klimatyczna kampania to spisek?”, „Kto robi z nas głupców?”[169]. Rozprzestrzenianiu się mitów starają się przeciwdziałać popularyzatorzy nauki, wśród nich tacy polscy popularyzatorzy, jak Szymon Malinowski[170], Łukasz Turski[167], Andrzej Pieńkowski[163][171][172] i inni.
Zobacz też
- agnotologia
- climategate
- denializm globalnego ocieplenia
- glaciergate
- Globalne ocieplenie – wielkie oszustwo
- Handlarze złudzeń
- Merchants of Doubt
- Niewygodna prawda
- Wiek głupoty
Uwagi
- ↑ 1 GtC (gigaton węgla) = 1 000 000 000 ton węgla = 1 PgC (petagramów węgla) = 1015 g = 1012 kg. Jedna jednostka masy węgla odpowiada 3,664 jednostkom masy CO2.
- ↑ Część wykazu bogatego piśmiennictwa zamieszczono w odrębnych artykułach na temat ewolucji gwiazd i Układu Słonecznego, historii pierwiastków chemicznych i innych.
- ↑ W czasie formowania się Układu Słonecznego w otoczeniu protoplanety znajdowały się przede wszystkim najbardziej rozpowszechnione we Wszechświecie (zob. historia pierwiastków chemicznych) lekkie gazy – wodór i hel, tzw. „atmosfera pierwotna” (ang. Primary atmosphere). Została ona utracona wskutek wysokiej temperatury (zob. „temperatura” według kinetycznej teorii gazów) oraz oddziaływania wiatru słonecznego[30][29][178].
- ↑ Woda nie jest zatrzymywana w atmosferze – ulega przemianom tworzącym cykl hydrologiczny. Dla pary wodnej nie określa się wartości GWP, jednak ma ona bardzo duży wpływ na inne zjawiska cieplne, zachodzące w atmosferze i na powierzchni Ziemi[173]. Stwierdzono istnienie silnych dodatnich sprzężeń zwrotnych… Przyjmuje się w przybliżeniu, że współcześnie 75% pochłanianego w atmosferze promieniowania podczerwonego jest absorbowane przez parę wodną i chmury, 20% przez dwutlenek węgla, a 5% przez pozostałe gazy cieplarniane[174].
- ↑ określony dla metanu potencjał tworzenia efektu cieplarnianego (GWP od ang. global warming potential) jest 23 razy większy niż dla CO2. Wartość GWP zależy stopnia absorpcji promieniowania podczerwonego i czasu „życia” związku w atmosferze.
- ↑ Tjeerd H. van Andel rozdział Życie, czas i zmiany w książce Nowe spojrzenie na starą planetę. Zmienne oblicze Ziemi zamyka zdaniem[179]:
To właśnie życie przekształciło ledwo zdatny do zamieszkania świat w dogodne siedlisko i utrzymało go w tym stanie w ciągu długich eonów. I jest ironią losu, że my, sami będąc wytworem współewolucji życia i Ziemi, zdążamy ku temu, by przywrócić na naszej planecie znacznie mniej znośne do życia warunki.
Poleca też wybrane książki na temat historii życia i dziejów istot ludzkich, napisane dla czytelników spoza kręgu specjalistów (niektóre z nich wymieniono w wykazie bibliografii).
- ↑ Za miarę aktywności słonecznej uważa się wartości stężenia izotopu 10Be, bardzo dobrze skorelowane z liczbą plam na Słońcu[177] (zob. też cykliczność aktywności Słońca, diagram Hertzsprunga-Russella i ciąg główny, przyszłość Ziemi, Układu Słonecznego i Wszechświata).
- ↑ a b Wskaźniki δ13C i δ18O wyznacza się, określając nadwyżkę/niedobór rzadziej występującego izotopu i porównując tę wartość z określoną dla próbki standardowej[58]. W 2007 roku opublikowano udoskonaloną metodę określania wieku skamieniałości. Polega na oznaczaniu zawartości związanych ze sobą rzadkich izotopów tlenu i węgla. Ponieważ tworzeniu wiązań między 18O i 13ć w skamieniałościach (muszle, koralowce) sprzyjają niskie temperatury, istnieje możliwość oszacowania temperatury wody morskiej, w której żyły organizmy (wiązanie 13C-18O jako „paleotermometr”). Badania potwierdziły istnienie silnego sprzężenia między wartościami temperatury i stężeniami CO2[176]
- ↑ Oszacowania obliczeniowe: GEOCARB III 2001[68], COPSE 2004[69] i Rothman (2001)[70]
Pomiary: Royer i wsp. (2004)[71] i średnie dla 30 mln lat. Oś po prawej – stosunek wartości zmierzonej do średniej dla poprzedniego miliona lat. - ↑ Prawdopodobnie w okresie od ok. 2 mln do ok. 200 tys. lat temu nastąpiła – pod wpływem bardzo silnego nacisku selekcyjnego – adaptacja Homo erectus do długotrwałych biegów w stepowiejącym środowisku tropikalnej sawanny Afryki Wschodniej (szczątki Homo sapiens, odkryte w Dżabal Ighud są datowane na 315 tys. lat[175]).
- ↑ Objaśnienia znaczenia symboli zamieszczono w opisie pliku w Commons.
Przypisy
- ↑ a b c d e f g h i Corinne Le Quéré i inni 2018 ↓.
- ↑ a b Redakcja portalu: Szymon Malinowski, Aleksandra Kardaś, Marcin Popkiewicz, Anna Sierpińska wsp: Efekt cieplarniany - jak to działa. [w:] Portal Nauka o klimacie dla sceptycznych [on-line]. Agencja Kreatywna Pong. [dostęp 2019-05-12].
- ↑ a b c d David C. Catling, Mark W. Claire. How Earth’s atmosphere evolved to an oxic state. A status report. „Earth and Planetary Science Letters (EPSL)”. 237, s. 1–20, 2005. Elsevier. ISSN 0012-821X. (ang.).
- ↑ a b Tony Eggleton: A Short Introduction to Climate Change. Cambridge University Press, 2013, s. 52. ISBN 978-1-107-61876-3.
- ↑ Atmospheric CO2 hits record high in May 2019 [online].
- ↑ A 40-million-year history of atmospheric CO2, DOI: 10.1098/rsta.2013.0096.
- ↑ Richard E. Zeebe, History of Seawater Carbonate Chemistry, Atmospheric CO2, and Ocean Acidification, „Annual Review of Earth and Planetary Sciences”, 40 (1), 2012, s. 141–165, DOI: 10.1146/annurev-earth-042711-105521, ISSN 0084-6597 [dostęp 2018-09-20] (ang.).
- ↑ Peoples Climate Movement. [w:] Strona internetowa PCM [on-line]. [dostęp 2019-03-29]. (ang.).
- ↑ a b c Trends in Atmospheric Carbon Dioxide. [dostęp 2019-11-03].
- ↑ Holli Riebeek, The Carbon Cycle, NASA, 2011.
- ↑ a b CarbonTracker CT2017. National Oceanic & Atmospheric Administration. [dostęp 2019-11-04].
- ↑ Climate Forcings and Global Warming. [w:] NASA [on-line]. [dostęp 2019-05-29].
- ↑ Spektroskopia w podczerwieni. [w:] Prezentacja dydaktyczna na enauczanie.pg.edu.pl [on-line]. Centrum Usług informatycznych Politechniki Gdańskiej. [dostęp 2019-03-11].
- ↑ Spektroskopia IR i spektroskopia Ramana jako metody komplementarne. [w:] Materiały dydaktyczne Wydziału Chemicznego Politechniki Łódzkiej [on-line]. Międzyresortowy Instytut Techniki Radiacyjnej. [dostęp 2019-05-18].
- ↑ The State of Greenhouse Gases in the Atmosphere Based on Global Observations through 2017. „WMO Greenhouse Gas Bulletin”, 22.11.2018. Word Meteorological Organization. ISSN 2078-0796.
- ↑ a b c d Weiner 2003 ↓, s. 142–175.
- ↑ Anna Drożak i inni, Fotosynteza typu C4, 2011.
- ↑ Małgorzata Fugol, Józef Szlachta, Zasadność użytkowania kiszonki z kukurydzy i gnojowicy świńskiej do produkcji biogazu, „Inżynieria Rolnicza” (1(119)), 2010.
- ↑ Witold Rzepiński, Alternatywą drzewo tlenowe, „Agroporady” (10), 16 marca 2016.
- ↑ Gao Zhiping, Shen Weijun, Chen Guoxiang, C4-like Photosynthesis has Important Functions in C3 Plant Vasculature, „Journal of Experimental Botany”, 2018, DOI: 10.1093/jxb/ery155.
- ↑ Hendrik Poorter, Interspecific variation in the growth response of plants to an elevated ambient CO2 concentration, „Vegetatio” (104/105), 1993, s. 77-97.
- ↑ S.C. Wong, Elevated Partial Pressure of CO2 and Plant Growth, „Oecologia”, 44, 1979, s. 68-74, DOI: 10.1007/BF00346400, PMID: 28310466 (ang.).
- ↑ Lisa Ainsworth, What have we learned from 15 years of free-air CO2 enrichment (FACE)? A meta-analytic review of the responses of photosynthesis, canopy properties and plant production to rising CO2., „New Phytologist”, 165, 2004, DOI: 10.1111/j.1469-8137.2004.01224.x, PMID: 15720649 (ang.).
- ↑ Helena Bottemiller Evich, The great nutrient collapse. The atmosphere is literally changing the food we eat, for the worse. And almost nobody is paying attention. [online], Politico - The Agenda, 13 września 2017.
- ↑ Z. Zhu i inni, Greening of the Earth and its drivers., „Nature Climate Change” (6), 2016, s. 791–795, DOI: 10.1038/nclimate3004, ISSN 1758-6798.
- ↑ J.M. Hayes: Evolution of the atmosphere. [w:] Encyclopedia Britannica [on-line]. [dostęp 2019-04-18]. (ang.).
- ↑ Heinrich D. Holland. The oxygenation of the atmosphere and oceans. „Philosophical Transactions of the Royal Society B”. 361 (1470), 2006-05-19. DOI: 10.1098/rstb.2006.1838. ISSN 0962-8436. (ang.).
- ↑ Gerhard Manier (Prof. Dr.): 1.2 Entstehung der Ur- oder Primordialatmosphäre. [w:] Einführung in die Umweltmeteorologie Ein Computer-Lernprogramm des Fachgebiets Meteorologie der TU Darmstadt; Die Zusammensetzung der Atmosphäre und ihre Entstehung [on-line]. TU Darmstadt. [dostęp 2019-03-13]. (niem.).
- ↑ a b James Schombert: Primary Atmospheres. [w:] Materiały dydaktyczne Department of Physics University of Oregon [on-line]. University Oregon. [dostęp 2019-05-08]. (ang.).
- ↑ a b Julia Rosen, Ph.D.; Anne E. Egger, Ph.D: La Historia de la Atmósfera de la Tierra I: El Origen de la Atmósfera de la Tierra. [w:] Visionlearning > Ciencias de la Tierra > Atmósfera y Océanos [on-line]. Visionlearning, Inc; La Fundación Nacional de la Ciencia y el Departamento de Educación de Estados, 2014. [dostęp 2019-03-13]. (hiszp.).
- ↑ Carl Sagan, George Mullen. Earth and Mars: Evolution of Atmospheres and Surface Temperatures. „Science”. 177 (4043), s. 52–56, 07 Jul 1972. DOI: 10.1126/science.177.4043.52. ISSN 0036-8075. (ang.).
- ↑ Stephen Moorbath. Oldest rocks, earliest life, heaviest impacts, and the Hadean–Archaean transition. „Applied Geochemistry”. 20 (5), s. 819–824, 2005. Elsevier. ISSN 0883-2927. (ang.).
- ↑ Martin J Van Kranendonk. Two types of Archean continental crust: Plume and plate tectonics on early Earth. „American Journal of Science”. 10 (310), s. 1187–1209, December 2010. DOI: 10.2475/10.2010.01. ISSN 0002-9599. (ang.).
- ↑ Marta Miedźwiedziew: Wietrzenie mechaniczne i chemiczne skał i minerałów. [w:] Materiały szkoleniowe dla uczniów szkół ponadgimnazjalnych [on-line]. Zespół Szkół Handlowo-Ekonomicznych im. Mikołaja Kopernika w Białymstoku. [dostęp 2019-03-18].
- ↑ Stanley 2002 ↓, s. 324–329.
- ↑ Lynn Sagan. On the origin of mitosing cells. „J Theor Bio.”. 14 (3), s. 255–274, 1967. DOI: 10.1016/0022-5193(67)90079-3. PMID: 11541392. (ang.).
- ↑ Lynn Margulis: Origin of Eukaryotic Cells; evidence and research implications for a theory of the origin and evolution of microbial, plant, and animal cells on the Precambrian earth. New Haven, Connecticut: Yale University Press, 1970, s. 1–349. ISBN 0-300-01353-1. (ang.).
- ↑ Lynn Margulis: Symbiotic planet; A New Look at Evolution. 1998.
- ↑ James St. John: Banded iron formations (BIFs). Ohio State University, Newark. [dostęp 2019-03-23]. [zarchiwizowane z tego adresu (2015-01-08)].
- ↑ a b Gunnar Ries: Auswirkungen wechselnder Sauerstoffgehalte der Erdatmosphäre auf das Leben. [w:] Strona internetowa autora [on-line]. Geo-Science WebRing, 2004. [dostęp 2019-03-23]. (niem.).
- ↑ Stanley 2002 ↓, s. 365–373.
- ↑ Rossati A. Global Warming and Its Health Impact. „Int J Occup Environ Med.”. 1 (8), s. 7–20, 2017 Jan. DOI: 10.15171/ijoem.2017.963. (ang.). (zob. też inne publikacje tegoż autora w PubMed).
- ↑ Kavya Balaraman. Doctors Warn Climate Change Threatens Public Health; Physicians are noticing an influx of patients whose illnesses are directly or indirectly related to global warming. „Scientific American”, March 17, 2017. Springer Nature. ISSN 0036-8733.
- ↑ Landsat’s Critical Role in Protecting Human Health. [w:] NASA Landsat Science [on-line]. NASA. [dostęp 2019-05-21]. (ang.).
- ↑ Stanley 2002 ↓, s. 64–65.
- ↑ Buffon, Georges Louis Leclerc, comte de, 1707-1788: Histoire naturelle, générale et particulière contenant les époques de la nature. A Paris: De l’Imprimerie royale, 1778. (The Epochs of Nature 2018, 9780226395432).
- ↑ EastGRIP The East Grenland Ice-Core Project. [w:] Strona internetowa [on-line]. eastgrip.org. [dostęp 2019-04-13]. (ang.).
- ↑ Bethan Davies: [West Antarctic Ice Sheet By Bethan Davies – Last updated 03/03/2014 West Antarctic Ice Sheet]. [w:] Strona internetowa Antarctic Glaciers [on-line]. Last updated 03/03/2014. [dostęp 2019-04-13]. (ang.).
- ↑ The National Science Foundation Ice Core Facility (NSF-ICF) – formerly the National Ice Core Laboratory (NICL). [w:] Strona internetowa NSF-ICF [on-line]. [dostęp 2019-04-13]. (ang.).
- ↑ NSF-ICF; About. [w:] Strona internetowa National Science Foundation Ice Core Facility (NSF-ICF) [on-line]. US Geological Survey. [dostęp 2019-04-04]. (ang.).
- ↑ NSF-ICF; Publications. [w:] Strona internetowa National Science Foundation Ice Core Facility (NSF-ICF) [on-line]. US Geological Survey. [dostęp 2019-04-04]. (ang.).
- ↑ J.D. Hays, John Imbrie, N.J. Shackleton. Variations in the Earth’s Orbit: Pacemaker of the Ice Ages For 500,000 years, major climatic changes have followed variations in obliquity and precession. „Science”. 194 (4270), s. 1121–1132, 10 December 1976. American Association for the Advancement of Science. ISSN 0036-8075. (ang.).
- ↑ K.K. Andersen, N. Azuma, Barnola, J.M., M. Bigler, P. Biscaye i wsp. (North Greenland Ice Core Project members). High-resolution record of Northern Hemisphere climate extending into the last interglacial period. „Nature”. 431 (7005), s. 147–151, 09 September 2004. DOI: 10.1038/nature02805. ISSN 0028-0836. (ang.). Kurt M. Cuffey, Palaeoclimate; Into an ice age s 133–134.
- ↑ van Andel 1997 ↓, s. 31–34.
- ↑ van Andel 1997 ↓, s. 157–163.
- ↑ Stanley 2002 ↓, s. 330–333.
- ↑ van Andel 1997 ↓, s. 58–60, 72–73.
- ↑ a b Marcin Popkiewicz i Aleksandra Kardaś, konstultacja merytoryczna: dr hab. Jarosław Tyszka i inni: Paleoklimatologia: izotopy tlenu a temperatura. [w:] Portal Nauka o klimacie dla sceptycznych [on-line]. Naukaoklimacie.pl ; Agencja Kreatywna Pong, 2017-11-27. [dostęp 2019-03-27].
- ↑ Lorraine E. Lisiecki, Maureen E. Raymo: Pliocene-Pleistocene stack of globally distributed benthic stable oxygen isotope records. PANGAEA. [w:] PANGAEA. Data Publisher for Earth & Environmental Science [on-line]. 2005. [dostęp 2019-03-27]. (ang.).; Supplement to: Lisiecki, LE; Raymo, ME (2005): A Pliocene-Pleistocene stack of 57 globally distributed benthic d18O records, Paleoceanography, 20, PA1003.
- ↑ W. Dansgaard. Stable isotopes in precipitation. „Tellus B”. XVI (4), s. 436–468, 1964. DOI: 10.3402/tellusa.v16i4.8993. ISSN 0280-6509. (ang.).
- ↑ C. Kendal, J.J. McDonnell (Eds.): Chapter 22. Isotopes as Indicators of Environmental Change. [w:] Resources on Isotopes; Isotope Tracers in Catchment Hydrology [on-line]. USGS National Research Program, Elsevier Science B.V., Amsterdam, 1998. s. 761–816. [dostęp 2019-03-17]. (ang.).
- ↑ Roland Werner. The online 18O/16O analysis: development and application. „Isotopes Environ Health Stud.”. 39 (2), s. 85–104, 2003 Jun. DOI: 10.1080/1025601031000108642. PMID: 12872801. (ang.).
- ↑ Matthias Saurer. The influence of climate on the oxygen isotopes in tree rings. „Isotopes Environ Health Stud.”. 38 (2), s. 105–112, 2003 Jun. DOI: 10.1080/1025601031000108633. (ang.).
- ↑ Holli Riebeek: Paleoclimatology, the Oxygen Balance. [w:] Earth Observatory NASA [on-line]. May 6, 2005. [dostęp 2019-03-20].
- ↑ Uniwersytet Colorado (Gifford H. Miller i wsp.), tłum.: Marcin Popkiewicz: Kiedy ostatnio w Arktyce bylo tak cieplo jak obecnie?. [w:] Portal 'Nauka o klimacie dla sceptycznych’ (red. Szymon Malinowski i wsp.) [on-line]. 2013-09-18. [dostęp 2019-03-28].
- ↑ Gifford H. Miller, Scott J. Lehman, Kurt A. Refsnider, John R. Southon, Yafang Zhong. Unprecedented recent summer warmth in Arctic Canada. „Geophysical Research Letters”. 40 (21), s. 5745–5751, 22 October 2013. American Geophysical Union (United States). DOI: 10.1002/2013GL057188. ISSN 1944-8007. (ang.).
- ↑ Robert A. Rohde, Richard A. Muller. Cycles in fossil diversity. „Nature”. 434, s. 208–210, 10 March 2005. Nature Publishing Group. ISSN 0028-0836. (ang.).
- ↑ a b Robert A. Berner, Zavareth Kothavala. Geocarb III: A Revised Model of Atmospheric CO2 over Phanerozoic Time. „American Journal of Science”. 301 (2), s. 182–204, February 2001. DOI: 10.2475/ajs.301.2.182. ISSN 0002-9599. (ang.).
- ↑ a b Noam M. Bergman, Timothy M. Lenton, Andrew. J. Watson. COPSE: A new model of biogeochemical cycling over Phanerozoic time. „American Journal of Science”. 304 (5), s. 397–437, May 2004. ISSN 0002-9599. (ang.).
- ↑ a b Daniel H. Rothman. Atmospheric carbon dioxide levels for the last 500 million years. „Proceedings of the National Academy of Sciences of the United States of America”. 99 (7), s. 4167–4171, April 2, 2002. DOI: 10.1073/pnas.022055499. (ang.).
- ↑ a b Royer i inni, CO2 as a primary driver of Phanerozoic climate, „GSA Today”, 14 (3), 2004, s. 4–10, DOI: 10.1130/1052-5173(2004)014<4:CAAPDO>2.0.CO;2 (ang.).
- ↑ wynik wyszukiwania dla „carbon dioxide measurements”. [w:] Strona internetowa California Institute of Technology [on-line]. caltech.edu. [dostęp 2019-04-06]. (ang.).
- ↑ Markus Reichstein Eva Falge, Dennis Baldocchi, Dario Papale, Marc Aubinet Paul Berbigier Christian Bernhofer Nina Buchmann, Tagir Gilmanov, André Granier, Thomas Grünwald i in. On the separation of net ecosystem exchange into assimilation and ecosystem respiration: review and improved algorithm. „Global Change Biology”. 11 (9), s. 1424–1439, September 2005. Wiley-Blackwell. (ang.).
- ↑ a b Katarzyna Dąbrowska-Zielińska, Maria Budzyńska, Monika Tomaszewska, Alicja Malińska, Maciej Bartold, Martyna Gatkowska, Konrad Turlej, Iwona Małek, Janusz Turbiak, Jacek Jaszczyński. Modelowanie wymiany netto ekosystemu (NEE). „Woda-Środowisko-Obszary Wiejskie”. 17 (1 (57)), s. 31–51, 2017. Wydawnictwo ITP (Instytut Technologiczno-Przyrodniczy). ISSN 1642-8145.
- ↑ a b 3. Podstawowe zagadnienia wyznaczania strumieni turbulencyjnych na podstawie pomiarów wykonanych metodą kowariancji wirów z otwartą ścieżką pomiarową. W: Krzysztof Fortuniak, Włodzimierz Pawlak: Wybrane problemy pomiarów wymiany gazowej pomiędzy powierzchnią ziemi a atmosferą na terenach bagiennych. Doświadczenia trzyletnich pomiarów w Biebrzańskim Parku Narodowym. Łódź: Katedra Meteorologii i Klimatologii WNG UŁ, 2016, s. 33–65. ISBN 978-83-944039-0-4.
- ↑ About the IPCC Data Distribution Centre. [w:] Strona internetowa IPPC [on-line]. IPPC. [dostęp 2019-04-11]. (ang.).
- ↑ The observational record. [w:] Strona internetowa IPCC Data Distribution Centre [on-line]. IPPC. [dostęp 2019-04-11]. (ang.).
- ↑ Carbon Dioxide: Projected emissions and concentrations record. [w:] Strona internetowa IPCC Data Distribution Centre [on-line]. IPPC. [dostęp 2019-04-11]. (ang.).
- ↑ a b R.A. Berner, Z. Kothavala. GEOCARB III: A Revised Model of Atmospheric CO2 over Phanerozoic Time. „American Journal of Science”. 301, s. 182–204, February, 2001. ISSN 0002-9599. (ang.).
- ↑ Roger Revelle. Harrison Brown (1917-1986). „Biographical Memoirs of the National Academy of Sciences”, s. 39–55, 1994. National Academy of Sciences. ISSN 0077-2933. (ang.).
- ↑ a b Daniel C. Harris. Charles David Keeling and the Story of Atmospheric CO2 Measurements. „Analytical Chemistry (Anal. Chem.)”. 82 (19), s. 7865–7870, 2010-06-11. American Chemical Society (ACS Publ.). DOI: 10.1021/ac1001492. ISSN 0003-2700. (ang.).
- ↑ a b Mauna Loa Observatory. [w:] Earth System Research Laboratory (ESRL), Global Monitoring Division; National Oceanic and Atmospheric Administration (NOAA) [on-line]. NOAA. [dostęp 2019-03-02]. (ang.).
- ↑ a b The Keeling Curve; A daily record of atmospheric carbon dioxide from Scripps Institution of Oceanography at UC San Diego: 411.47 parts per million (ppm) CO2 in air 06-Mar-2019. [w:] Strona internetowa Scripps Institution of Oceanography [on-line]. UC San Diego. [dostęp 2019-03-08]. (ang.).
- ↑ a b Pavel Blažka, Zofia Fischer. Woda a oddychanie gleby. „Kosmos: Problemy nauk biologicznych”. 66 (2 (315)), s. 167–173, 2017. ISSN 0023-4249.
- ↑ a b PD Dr. Gesine Hellberg-Rode: Bodenatmung. [w:] Projekt Hypersoil > Bodeneigenschaften [on-line]. hypersoil.uni-muenster. [dostęp 2019-04-12]. (niem.).
- ↑ Pomiar w podczerwieni (NDIR/FTIR). [w:] AKM Serwis; poradniki/techniki-pomiarowe; krótkie teoretyczne wprowadzenie do technik pomiarowych stosowanych w dostarczanych przez nas urządzeniach [on-line]. akm. [dostęp 2019-04-10].
- ↑ Jason Palidwar (Iridian Spectral Technologies): Optical Filters Open Up New Uses for MWIR, LWIR Systems. [w:] Strona internetowa Photonics Media [on-line]. Laurin Publishing Co., Inc.. [dostęp 2019-04-10]. (ang.).
- ↑ R.F. Keeling, S.C. Piper, A.F. Bollenbacher, J.S. Walker: Atmospheric Carbon Dioxide Record from Mauna Loa. [w:] Strona internetowa Scripps Institution of Oceanography, University of California; Carbon Dioxide Research Group [on-line]. Carbon Dioxid Information Analysis Center. [dostęp 2019-04-04]. (ang.).
- ↑ 40 Years of Mauna Loa CO2 Data from Keeling. [w:] Strona internetowa Carbon Dioxide Information Analysis Center [on-line]. CDIAC. [dostęp 2019-03-15].
- ↑ C.D. Keeling, J.F.S. Chin, T.P. Whorf. Increased activity of northern vegetation inferred from atmospheric CO2 measurements. „Nature”. 382, s. 146–149, 11 July 1996. DOI: 10.1038/386698a0. ISSN 1476-4687. (ang.).
- ↑ R.B. Myneni, C.D. Keeling, C.J. Tucker, G. Asrar, R.R. Nemani. Increased plant growth in the northern high latitudes from 1981 to 1991. „Nature”. 386, s. 698–702, 17 April 1997. DOI: 10.1038/386698a0. ISSN 1476-4687. (ang.).
- ↑ Atmospheric CO2 Records from Sites in the SIO Air Sampling Network (Scripps Institution of Oceanography Monitoring Sites). [w:] Strona internetowa Carbon Dioxide Information Analysis Center [on-line]. CDIAC. [dostęp 2019-03-15].
- ↑ Werner Marx, Robin Haunschild, Bernie French, Lutz Bornmann. Slow reception and under-citedness in climate change research: A case study of Charles David Keeling, discoverer of the risk of global warming. „Scientometrics”. 112 (2), s. 1079–1092, 2017-05-17. Springer Science+Business Media. DOI: 10.1007/s11192-017-2405-z. ISSN 0138-9130. (ang.).
- ↑ a b Andrzej Górnik. Możliwości bilansowania wymiany CO2 przy wykorzystaniu aparatury. „Polish Journal of Agronomy”, s. 3–10, 2015.
- ↑ a b FLUXNET2015 Dataset. [w:] FLUXNET Data Portal [on-line]. Lawrence Berkeley National Laboratory. [dostęp 2019-04-08]. (ang.).
- ↑ Zakres działalności. [w:] Instytut Ochrony Środowiska – Państwowy Instytut Badawczy w Warszawie [on-line]. ios.edu.pl. [dostęp 2019-04-07].
- ↑ Informacje na temat programu i celu pomiarów zanieczyszczenia powietrza na tłowych stacjach EMEP w Polsce. [w:] Strona internetowa GIOŚ [on-line]. GIOŚ. [dostęp 2019-04-13].
- ↑ George Burba, Dan Anderson: A Brief Practical Guide to Eddy Covariance Flux Measurements. [w:] A Field Book on Measuring Ecosystem Gas Exchange and Areal Emission Rates (informacje o książce) [on-line]. LI-COR Biosciences, November 2012. s. ss 331. [dostęp 2019-04-13]. (ang.).
- ↑ red. Krzysztof Fortuniak; wykonawcy projektu “Bilans absorpcji i emisji gazów cieplarnianych (metanu, dwutlenku węgla i pary wodnej) na obszarach bagiennych (studium Biebrzańskiego Parku Narodowego)”, sfinansowanego ze środków Narodowego Centrum Nauki (decyzja DECR2011/01/B/ST10/0): Wybrane problemy pomiarów wymiany gazowej pomiędzy powierzchnią ziemi a atmosferą na terenach bagiennych. Łódź: Katedra Meteorologii i Klimatologii WNG UŁ, 2016, s. ss 148. ISBN 978-83-944039-0-4.
- ↑ P. Rochette, B. Ellert, E.G. Gregorich, R.L. Desjardins, E. Pattey, R. Lessard, B.G. Johnson. Description of a dynamic closed chamber for measuring soil respiration and its comparison with other techniques. „Canadian Journal of Soil Science”. 77 (2), s. 195–206, 1997. Canadian Science Publishing. DOI: 10.4141/S96-110.
- ↑ SRS1000 T Portable Soil Respiration System. [w:] Strona internetowa The Analytical Development Company. BioScientific Ltd. [on-line]. SRS1000T. [dostęp 2019-04-10]. (ang.).
- ↑ D. Karnosky ed., R. Ceulemans, G. Scarascia-Mu, J. Innes: Impact of Carbon Dioxide and Other Greenhouse Gases on Forest Ecosystems. September 2001, s. ss 352, seria: IUFRO Research Series. ISBN 978-0-85199-551-9.
- ↑ Dieter Overdieck: CO2, Temperature, and Trees: Experimental Approaches. Springer, 22 paź 2016, s. ss 240. ISBN 981-10-1860-X.
- ↑ G. Esser, D. Overdieck: Modern Ecology: Basic and Applied Aspects. Elsevier, 29 lip 2016, s. ss 874. ISBN 1-4832-9125-1.
- ↑ Andrzej Mila, Antoni Murkowski. Oddziaływanie podwyższonego stężenia CO2 na wzrost i rozwój wybranych genotypów rzepaku ozimego. „Rośliny oleiste”. XXX, s. 65–73, 2009.
- ↑ A. P. de Faria i wsp: The increase of current atmospheric CO2 and temperature can benefit leaf gas exchanges, carbohydrate content and growth in C4 grass invaders of the Cerrado biome (abstract). [w:] CABI; Invasive Species Compendium Detailed coverage of invasive species threatening livelihoods and the environment worldwide [on-line]. CAB International, 2018. [dostęp 2019-04-15]. (ang.).
- ↑ A.P. de Fariaa, M.A. Marabesi, M. Gaspar, M.G.C.França. The increase of current atmospheric CO2 and temperature can benefit leaf gas exchanges, carbohydrate content and growth in C4 grass invaders of the Cerrado biome. „Plant Physiology and Biochemistry”. 127, s. 608–616, June 2018. Elsevier Inc.. DOI: 10.1016/j.plaphy.2018.04.042. ISSN 0032-0889. (ang.).
- ↑ Josh M. Gray, Steve Frolking, Eric A. Kort, Deepak K. Ray, Christopher J. Kucharik, Navin Ramankutty, Mark A. Friedl. Direct human influence on atmospheric CO2 seasonality from increased cropland productivity. „Nature”, s. 398–401, 19 November 2014. Nature Publishing Group. ISSN 0028-0836. (ang.).
- ↑ a b c Marcin Popkiewicz, konsultacja merytoryczne: prof. Szymon P. Malinowski: Satelitarne obserwacje stężeń, źrodeł emisji i miejsc pochłaniania CO2. [w:] Portal 'Nauka o klimacie dla sceptycznych’ (red. Szymon Malinowski i wsp.) [on-line]. 2018-06-18. [dostęp 2019-04-05].
- ↑ ADEOS (Advanced Earth Observing Satellite) / Midori. [w:] eoPortal [on-line]. [dostęp 2019-04-12]. (ang.).
- ↑ ADEOS Project Overview. [w:] Strona Earth Observation Research Center [on-line]. 6 Febrary 1998. [dostęp 2019-04-12]. (ang.).
- ↑ Science News Staff: Adios, ADEOS: Japanese Satellite Lost. [w:] Science Mag [on-line]. AAAS (American Association for the Advancement of Science), Jul. 1, 1997. [dostęp 2019-04-12].
- ↑ a b What is the A-Train? The Afternoon Constellation and Scientific Discovery. [w:] Strona internetowa National Aeronautics and Space Administration [on-line]. NASA. [dostęp 2019-04-13]. (ang.).
- ↑ Japan launches rocket with greenhouse-gas probe. [w:] CBC/Radio-Canada > Technology & Science [on-line]. CBC, January 23, 2009. [dostęp 2019-04-11]. (ang.).
- ↑ a b Herbert J. Kramer: GOSAT (Greenhouse gases Observing Satellite) / Ibuki. [w:] eoPortal [on-line]. eoPortal. [dostęp 2019-04-13]. (ang.).
- ↑ a b Orbiting Carbon Observatory Launch (OCO, misja 2009). [w:] Materiały prasowe [on-line]. NASA, luty 2009. s. 1–43. [dostęp 2019-04-04]. (ang.).
- ↑ Orbiting Carbon Observatory-2 (OCO-2) Watching the Earth breathe from space… Measuring carbon dioxide from space. [w:] Strona internetowa Jet Propulsion Laboratory (JPL Caltech), NASA [on-line]. JPL. [dostęp 2019-04-11]. (ang.).
- ↑ CEOS EO Handbook – Catalogue of Satellite Instruments. [w:] The CEOS Database [on-line]. Commitee on Earth Observation Sattelites (CEOS). [dostęp 2019-04-16]. (ang.).
- ↑ Alan Buis (Jet Propulsion Laboratory, Pasadena, California): GeoCarb: A New View of Carbon Over the Americas. [w:] Strona internetowa National Aeronautics and Space Administration [on-line]. NASA, Jan. 11, 2018. [dostęp 2019-04-14]. (ang.).(https://www.nasa.gov/press-release/nasa-announces-first-geostationary-vegetation-atmospheric-carbon-mission press-release).
- ↑ Stephen Clark: Japan launches satellite to study human causes of climate change. [w:] Spaceflight Now [on-line]. Pole Star Publications Ltd, October 29, 2018. [dostęp 2019-04-15]. (ang.).
- ↑ Greenhouse gases Observing SATellite-3. [w:] database.eohandbook.com [on-line]. ESA. [dostęp 2019-04-15]. (ang.).
- ↑ Jon Nelson: OCO-2 Data Center. [w:] Jet Propulsion Laboratory, California Institute of Technology [on-line]. NASA. [dostęp 2019-04-13]. (ang.).
- ↑ Robert Granat (Human Interfaces Group): Virtual Science Data Environment – Get All the CO2 Satelite Data in One Place. [w:] Strona internetowa Jet Propulsion Laboratory [on-line]. NASA. [dostęp 2019-04-13]. (ang.).
- ↑ CarbonTracker CT2017. [w:] Global Greenhouse Gas Reference Network [on-line]. NOAA. [dostęp 2019-04-15]. (ang.).
- ↑ a b Robert A. Berner. The carbon cycle and CO2 over Phanerozoic time: the role of land plants. „Philosophical Transactions of the Royal Society B”, s. 75–82, 1998. Royal Society (United Kingdom). DOI: 10.1098/rstb.1998.0192. ISSN 0962-8436. (ang.).
- ↑ Elizabeth Kay Berner, Robert A. Berner: Global Environment: Water, Air, and Geochemical Cycles. Princeton University Press, 2012, s. 444. ISBN 0-691-13678-5.
- ↑ Robert Berner (1935-2015); Professor of Geology and Geophysics, Yale University. [w:] Google Scholar (295 publikacji z lat 1958–2008) [on-line]. scholar.google.com. [dostęp 2019-03-02]. (ang.).
- ↑ Robert A. Berner. GEOCARBSULF: A combined model for Phanerozoic atmospheric O2 and CO2. „Geochimica et Cosmochimica Acta (A special issue honoring Bob Berner)”. 70 (23), s. 5653–5664, December 2006. Elsevier. DOI: 10.1016/j.gca.2005.11.032. ISSN 0016-7037. (ang.).
- ↑ Don Canfield. Robert A. Berner (1935–2015) ; Geochemist who quantified the carbon cycle. „Nature”. 518, s. 484, 26 February 2015. DOI: 10.1038/518484a. (ang.).
- ↑ NASA Goddard Institute for Space Studies (GISS). [w:] Strona internetowa GISS [on-line]. [dostęp 2019-03-29]. (ang.).
- ↑ James Hansen: Storms Of My Grandchildren: The Truth About The Climate Catastrophe And Our Last Chance To Save Humanity. Bloomsbury Publishing PLC, September 1st 2009, s. 320. ISBN 978-1-4088-0745-3.
- ↑ James Hansen, „Storms of My Grandchildren”. [w:] Informacje o książce; ilustracje [on-line]. columbia.edu. [dostęp 2019-03-24]. (ang.).
- ↑ Dr. James E. Hansen; Scholarly Publications. [w:] Strona internetowa Climate Science, Awareness and Solutions Program Earth Institute [on-line]. Columbia University. [dostęp 2019-03-24]. (ang.).
- ↑ a b James Hansen, Makiko Sato, Pushker Kharecha, David Beerling, Robert Berner, Valerie Masson-Delmotte, Mark Pagani, Maureen Raymo, Dana L. Royer, James C. Zachos. Target Atmospheric CO2: Where Should Humanity Aim?. „Open Atmos. Sci. J.”, s. 217–231, 2008. DOI: 10.2174/1874282300802010217. (ang.).
- ↑ James Hansen, Makiko Sato, Gary Russell, Pushker Kharecha. Climate sensitivity, sea level and atmospheric carbon dioxide. „Philosophical Transactions of the Royal Society A”. 371 (2001 (Discussion Meeting Issue ‘Warm climates of the past–a lesson for the future?’)), s. 1–31, 28 October 2013. Royal Society (United Kingdom). DOI: 10.1098/rsta.2012.0294. ISSN 1364-503X. (ang.).
- ↑ James Hansen, Makiko Sato, Pushker Kharecha i wsp. Young people’s burden: requirement of negative CO2 emissions. „Earth Syst. Dynam.”, s. 577–616, 2017. Copernicus Publications. DOI: 10.5194/esd-8-577-2017. (ang.).
- ↑ red: Schlesinger leaves donation after death. [w:] The Daily Illini The independent student newspaper at the University of Illinois [on-line]. University of Illinois, April 16, 2018. [dostęp 2019-05-01]. (ang.).
- ↑ wynik wyszukiwania dla: Michael E. Schlesinger. [w:] AGU100 Advancing Earth and Space Science [on-line]. American Geophysical Union (AGU). [dostęp 2019-05-01]. (ang.).
- ↑ a b Michael E. Schlesinger, Navin Ramankutty. Implications for global warming of intercycle solar irradiance variations. „Nature”, s. 330–333, 26 November 1992. Nature Publishing Group. ISSN 0028-0836. (ang.).
- ↑ Professor John Mitchell (Principal Research Fellow at the Met Office.). [w:] Met Office [on-line]. [dostęp 2019-05-01]. (ang.).
- ↑ Michael E. Schlesinger, John F. B. Mitchell. Climate model simulations of the equilibrium climatic response to increased carbon dioxide. „Reviews of Geophysics”. 25 (4), s. 760–798, May 1987. Wiley-Blackwell, AGU US. DOI: 10.1029/RG025i004p00760. ISSN 8755-1209. (ang.).
- ↑ Benjamin D. Santer (Atmospheric Scientist, Lawrence Livermore National Laboratory). [w:] Wyszukiwarka Google Scholar [on-line]. [dostęp 2019-05-01]. (ang.).
- ↑ B.D. Santer, K.E. Taylor, T. M.L. Wigley, T.C. Johns, P.D. Jones, D.J. Karoly, J.F.B. Mitchell, A.H. Oort, J.E. Penner, V. Ramaswamy, M.D. Schwarzkopf, R.J. Stouffer, S. Tett. A search for human influences on the thermal structure of the atmosphere. „Nature”, s. 39–46, 04 July 1996. Nature Publishing Group. DOI: 10.1038/382039a0. ISSN 0028-0836. (ang.).
- ↑ compiled and edited by Daniel J. Lunt, Harry Elderfield, Richard Pancost and Andy Ridgwell. Warm climates of the past–a lesson for the future?. „Philosophical Transactions A”. 371 (2001), 28 October 2013. Royal Society. DOI: 10.1098/rsta.2013.0146. (ang.).
- ↑ Hothouse climates of the past – lessons for the future. [w:] Strona internetowa University of Bristol; The Cabot Institute [on-line]. University of Bristol, 22 May 2017. [dostęp 2019-04-18]. (ang.).
- ↑ a b red. ProCon: Is Human Activity Primarily Responsible for Global Climate Change?. [w:] PROS AND CONS OF CONTROVERSIAL ISSUES [on-line]. ProCon.org. [dostęp 2019-05-16].
- ↑ Ocean fertilization (OF). [w:] Geoengineering Monitor ; Geoengineering Technology Briefing [on-line]. is a joint project of Biofuelwatch anis a joint project of Biofuelwatch, ETC Group, Heinrich Boell Foundationd, 30 May 2018. [dostęp 2019-05-07]. (ang.).
- ↑ Prof. Michael Kelly - Publications. [w:] Strona internetowa Uniwersytetu w Cambridge (Department of Engineering) [on-line]. University of Cambridge. [dostęp 2019-05-02]. (ang.).
- ↑ a b Michael J. Kelly. Why a collapse of global civilization will be avoided: a comment on Ehrlich & Ehrlich. „Proceedings of the Royal Society B: Biological Sciences”. 280 (1767), 22 September 2013. Royal Society. DOI: 10.1098/rspb.2013.1193. ISSN 0962-8452. (ang.).
- ↑ Prof. Kelly shows the middle way. [w:] Climate Conversation Group [on-line]. CCG, June 5, 2011. [dostęp 2019-05-01].
- ↑ Michael Kelly. Why my own Royal Society is wrong on climate change: A devastating critique of world’s leading scientific organisation by one of its Fellows. „Daily Mail”, 14 March 2015. Associated Newspapers Ltd. ISSN 0307-7578. (ang.).
- ↑ Robert Jastrow, William Nierenberg, Frederick Seitz. Global warming: What does the science tell us?. „Energy”. 16 (11–12), s. 1331–1345, November–December 1991. Elsevier. DOI: 10.1016/0360-5442(91)90006-8. ISSN 0360-5442. (ang.).
- ↑ Zbigniew Jaworowski. Czy człowiek zmienia klimat?. „Wiedza i Życie”, 1998. Prószyński Media. ISSN 0137-8929.
- ↑ Dzik 2003 ↓, s. 317.
- ↑ van Alden 1997 ↓, s. 290.
- ↑ Małgorzata Milian-Lewicka: Mroczna prawda o modnych tłuszczach. [w:] Kukbuk [on-line]. 17 marca 2019. [dostęp 2019-05-04].
- ↑ red. / źródło: Uniwersytet Maryland: Zielone Płuca Ziemi bezpowrotnie znikają. Takiej skali wycinki jeszcze nie widzieliśmy. [w:] Portal TwojaPogoda.pl [on-line]. 2018-06-29. [dostęp 2019-05-04].
- ↑ Damien McGuinness: ‘Meat Atlas’ charts a changing world of meat eaters By Damien McGuinness BBC News, Berlin. [w:] BBC News [on-line]. bbc.com, 9 January 2014. [dostęp 2019-05-02]. (ang.).
- ↑ Ziemia na rozdrożu. [w:] Portal internetowy [on-line]. [dostęp 2019-05-05].
- ↑ Philip Shabecaff. Global Warming Has Begun, Expert Tells Senate. „NYTimes”, June 24, 1988. The New York Times Company. (ang.).
- ↑ a b c d Conference of the Parties (COP). [w:] Strona internetowa United Nations Framework Convention on Climate Change (UNFCCC) [on-line]. UNFCCC. [dostęp 2019-05-05]. (ang.).
- ↑ a b Janina Kawałczewska: Ustalenia konwencji klimatycznych. [w:] Materiały Seminarium nt. Polityka energetyczna świata, Unii Europejskiej i Polski dla zrównoważonego rozwoju, RCEE Płock [on-line]. Regionalne Centrum Edukacji Ekologicznej w Płocku, 7 lutego 2011. [dostęp 2019-05-05].
- ↑ a b Andrzej Pieńkowski (współpracownik działu Nauka i Zdrowie, profil). „Wprost”. PMPG Polskie Media SA. ISSN 0209-1747.
- ↑ Porozumienie paryskie – Ramowa konwencja Narodów Zjednoczonych w sprawie zmian klimatu (2016). [w:] Baza EU Lex [on-line]. EUR-Lex, Urząd Publikacji. [dostęp 2019-03-02].
- ↑ Marcin Popkiewicz: Porozumienie klimatyczne w Paryżu. naukaoklimacie.pl, 13 grudnia 2015. [dostęp 2019-04-15].
- ↑ red. ProCon: Is Human Activity Primarily Responsible for Global Climate Change? – Footnotes & Sources. [w:] PROS AND CONS OF CONTROVERSIAL ISSUES [on-line]. ProCon.org. [dostęp 2019-05-16].
- ↑ a b Łukasz A. Turski. Energetyczne dylematy. „Wiedza i Życie”, 1998. Prószyński Media. ISSN 0137-8929.
- ↑ Andrzej Pieńkowski. Klimatyczna przepychanka. „Wprost”, 2008. Agencja Wydawniczo-Reklamowa „Wprost” Sp. z o.o.. ISSN 0209-1747.
- ↑ Andrzej Pieńkowski. Klimat się ociepla, głupcze. „Wprost”, 28 marca 2010. Agencja Wydawniczo-Reklamowa „Wprost” Sp. z o.o.. ISSN 0209-1747.
- ↑ Redakcja portalu: Szymon Malinowski, Aleksandra Kardaś, Marcin Popkiewicz, Anna Sierpińska wsp: Fakty i mity. [w:] Portal Nauka o klimacie dla sceptycznych [on-line]. Agencja Kreatywna Pong. [dostęp 2019-04-19].
- ↑ Andrzej Pieńkowski. Wyrok na CO2. „Wiedza i Życie”, 1998. Prószyński Media. ISSN 0137-8929.
- ↑ Andrzej Pieńkowski. Huragan huraganów. „Wprost”, 2008. Agencja Wydawniczo-Reklamowa „Wprost” Sp. z o.o.. ISSN 0209-1747.
- ↑ John Cook, tłum. Marcin Popkiewicz, konsultacja merytoryczna: prof. Szymon P. Malinowski, skrót na podstawie wersji pełnej: Marta Śmigowska: Mit: para wodna jest najważniejszym gazem cieplarnianym. [w:] Nauka o klimacie dla sceptycznych [on-line]. naukaoklimacie.pl, 2015. [dostęp 2019-02-28].
- ↑ Brian J. Soden, Isaac M. Held. An Assessment of Climate Feedbacks in Coupled Ocean–Atmosphere Models. „Journal of Climate”. 19, s. 3354–3360, 15 July 2006. American Meteorological Society (United States). DOI: 10.1175/JCLI3799.1. ISSN 0894-8755. (ang.).
- ↑ Ewen Callaway: Oldest Homo sapiens fossil claim rewrites our species’ history. Nature, 7 czerwca 2017. [dostęp 9 czerwca 2017].
- ↑ Rosemarie E. Came, John M. Eiler, Ján Veizer, Karem Azmy, Uwe Brand, Christopher R. Weidman. Coupling of surface temperatures and atmospheric CO2 concentrations during the Palaeozoic era. „Nature”. 449 (7159), s. 198–201, 13 September 2007. DOI: 10.1038/nature06085. (ang.).
- ↑ Marcin Popkiewicz, konstulacja merytoryczna: prof. Szymon Malinowski: Paleoklimatologia: Aktywność słoneczna i radioaktywne izotopy. [w:] Nauka o klimacie dla sceptycznych [on-line]. Agencja Kreatywna Pong, 2017-12-11. [dostęp 2019-04-16].
- ↑ Dieter Kasang: Geschichte der Erdatmosphäre. [w:] Hauptseite 1 Klimawandel Und Klimafolgen [on-line]. wiki.bildungsserver.de. [dostęp 2019-02-27]. (niem.).
- ↑ van Andel 1994 ↓, s. 284.
Bibliografia
- Steven M. Stanley, tłum. Ireneusz Walaszczyk: Historia Ziemi. Warszawa: Wydawnictwo Naukowe PWN, 2002-01-01, s. 705. ISBN 83-01-13625-1.
- Tjeerd H. van Andel: Nowe spojrzenie na starą planetę. Zmienne oblicze Ziemi. Warszawa: Wydawnictwo Naukowe PWN, 1997.
- January Weiner: Życie i ewolucja biosfery. Podręcznik ekologii ogólnej. Warszawa: Wydawnictwo Naukowe PWN, 2003. ISBN 83-01-14047-X.
- Jerzy Dzik: Dzieje życia na Ziemi. Warszawa: Wydawnictwo Naukowe PWN, 2003, s. 110–135. ISBN 83-01-14038-0.
- Corinne Le Quéré, Robbie M. Andrew, Pierre Friedlingstein, Global Carbon Budget 2018, „Earth System Science Data”, 2018, DOI: /10.5194/essd-10-2141-2018.