Paracetamol
| |||||||||||||||||||||||||||
 Krystaliczny paracetamol | |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||
| Wzór sumaryczny |
C8H9NO2 | ||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
HO−C | ||||||||||||||||||||||||||
| Masa molowa |
151,17 g/mol | ||||||||||||||||||||||||||
| Wygląd |
biały, bezwonny proszek[1] | ||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||
| DrugBank | |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||
| Pochodne | |||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||
| Klasyfikacja medyczna | |||||||||||||||||||||||||||
| ATC | |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
Paracetamol, acetaminofen (łac. paracetamolum) – organiczny związek chemiczny, hydroksylowa pochodna acetanilidu, stosowany jako lek o działaniu przeciwbólowym i przeciwgorączkowym. W handlu znajduje się od 1955[6]. W Polsce stał się popularny w latach 90. XX wieku, wypierając z rynku aminofenazon, powszechnie wówczas używany lek przeciwgorączkowy.
W odróżnieniu od leków przeciwbólowych z grupy niesteroidowych leków przeciwzapalnych wykazuje bardzo słabe działanie przeciwzapalne[7] i nie zaburza procesu krzepnięcia krwi. Dobrze wchłania się z przewodu pokarmowego, osiągając po 30–60 minutach maksymalne stężenie we krwi. Efekt przeciwbólowy utrzymuje się przez 3–5 godzin[5]. Działa przez blokowanie cyklooksygenazy prostaglandynowej (prawdopodobnie COX-3) w ośrodkowym układzie nerwowym, hamując syntezę prostaglandyn, chociaż mechanizm nie został jeszcze do końca wyjaśniony[8].
Paracetamol stosuje się u osób dorosłych oraz dzieci. Może być podawany doustnie, doodbytniczo oraz dożylnie. Dostępny bez recepty w postaci tabletek, czopków oraz syropów dla dzieci. Wskazaniami do jego podawania są bóle mięśni, stawów, kości, zębów, nerwobóle, bóle pleców, barku i głowy, ból miesiączkowy oraz stany gorączkowe, a także ból po zabiegach stomatologicznych i chirurgicznych.
Substancja ta występuje również w złożonych preparatach przeciwbólowych, na przykład w kombinacji z kodeiną, kofeiną, kwasem acetylosalicylowym, ibuprofenem, difenhydraminą, dekstrometorfanem, fenylefryną, propyfenazonem, tramadolem, czy witaminą C. W połączeniu z niesteroidowymi lekami przeciwzapalnymi i opioidowymi środkami przeciwbólowymi paracetamol jest stosowany w leczeniu silniejszych bóli[9]. Nie wolno natomiast łączyć go z izoniazydem, diflunizalem, ryfampicyną i barbituranami. Wykazuje poważne interakcje z większością leków przeciwwirusowych.
U chorych z niewydolnością nerek sprzężony paracetamol kumuluje się we krwi. Podczas metabolizowania tego związku w wątrobie przez cytochrom P450, powstaje w niewielkich ilościach N-acetylo-4-benzochinonoimina (NAPQI) – silny utleniacz, który zaburza gospodarkę wolnorodnikową w tym narządzie, prowadząc do nieodwracalnego uszkodzenia hepatocytów. Leku tego powinni wystrzegać się chorzy z przewlekłym zapaleniem lub marskością wątroby. Ze względu na narastające stężenie NAPQI, niebezpieczne są zwłaszcza duże dawki paracetamolu, zażyte na przykład omyłkowo. U osób regularnie spożywających alkohol istnieje szczególnie duże ryzyko uszkodzenia wątroby (synergiczne działanie toksyczne alkoholu i paracetamolu).
Specyfik ten charakteryzuje się korzystnym profilem działań niepożądanych w porównaniu do leków przeciwbólowych będących pochodnymi pirazolonu; jego wadą jest, że podawany w wysokich dawkach lub przez długi okres może prowadzić do trwałego martwiczego uszkodzenia wątroby. W krajach zachodnich toksyczność paracetamolu jest główną przyczyną ostrej niewydolności wątroby. W Stanach Zjednoczonych (w wolnej sprzedaży od 1955), Wielkiej Brytanii, Australii i Nowej Zelandii paracetamol jest najczęściej przedawkowywanym lekiem[10][11][12]. Przy prawidłowym zażywaniu jest na ogół dobrze tolerowany i stanowi alternatywę dla pacjentów, którzy nie tolerują leków przeciwbólowych z innych grup chemicznych.
Osoby dorosłe nabywające paracetamol w wolnej sprzedaży, bez uprzedniego skonsultowania się z lekarzem, nie powinny przekraczać maksymalnej dawki 4 gramów w ciągu 24 godzin (w przypadku obecności czynników ryzyka 2 gramy/dobę) oraz nie powinny stosować go dłużej niż 5 dni[13].
Paracetamol jest dostępny na rynku pod różnymi nazwami handlowymi w preparatach prostych (na przykład Acenol, Acetaminophen, Amipar, Apap, Benuron, Codipar, Doliprane, Dolonerv, Efferalgan, Etoran, Gemipar, Grippostad, Hascopar, Panadol, Paramax, Scanol, Tabcin) oraz złożonych (między innymi Antidol, Apap Extra, Codipar Plus, Coldrex, Dafalgan, Gripex, Saridon, Panadol Extra, Fervex). W związku z tym pacjenci zażywający więcej niż jeden lek przeciwbólowy powinni skontrolować, które z nich zawierają w swoim składzie paracetamol, i nie powinni przekraczać ani dopuszczalnej dawki jednorazowej, ani dawki dobowej paracetamolu (będącej sumą paracetamolu obecnego w różnych preparatach).
Historia[edytuj | edytuj kod]
Paracetamol został zsyntetyzowany po raz pierwszy w 1878 w Stanach Zjednoczonych, na Uniwersytecie Johnsa Hopkinsa, przez amerykańskiego chemika Harmona Northropa Morse’a, w reakcji redukcji 4-nitrofenolu cyną w kwasie octowym lodowatym[14]. Jako odkrywcę paracetamolu podaje się również Charlesa Frédérica Gerhardta, który substancję tę odkrył w roku 1852[15]. W 1893 roku paracetamol został znaleziony przez Josepha von Meringa w moczu osób, które przyjmowały fenacetynę. W 1899 roku dowiedziono, że paracetamol jest metabolitem acetanilidu. Owe odkrycia w tamtym okresie jednak zignorowano.

W 1946 roku Institute for the Study of Analgesic and Sedative Drugs otrzymał od New York City Department of Health fundusze na badania związane ze środkami przeciwbólowymi. Bernard Brodie i Julius Axelrod zostali wyznaczeni do prowadzenia badań, które miały wyjaśnić, dlaczego zażywanie środków, które nie były pochodnymi aspiryny, wiązało się z występowaniem methemoglobinemii – potencjalnie śmiertelnego stanu chorobowego, wiążącego się z upośledzeniem zdolności hemoglobiny do wiązania i przenoszenia tlenu. W 1948 Brodie i Axelrod powiązali występowanie methemoglobinemii z przyjmowaniem acetanilidu i stwierdzili, że efekt przeciwbólowy tego leku jest związany z działaniem jego metabolitu: paracetamolu. Stali się rzecznikami stosowania paracetamolu, jako leku pozbawionego działań ubocznych charakterystycznych dla acetanilidu[16].
Po raz pierwszy paracetamol został wypuszczony na rynek w 1955 przez McNeil Laboratories, jako lek uśmierzający ból i przeciwgorączkowy dla dzieci, pod nazwą handlową Tylenol Children’s Elixir[6].
W 1956 roku 500-miligramowe tabletki paracetamolu zostały wprowadzone do sprzedaży w Wielkiej Brytanii pod nazwą handlową Panadol przez Frederick Stearns & Co, filię Sterling Drug Inc. Miał on zastąpić preparat APC, zawierający kwas acetylosalicylowy, fenacetynę i kofeinę. Panadol był pierwotnie dostępny tylko na receptę, jako środek przeciwbólowy i przeciwgorączkowy. Reklamowano go jako „łagodny dla żołądka”, gdyż inne środki przeciwbólowe dostępne w owym czasie bazowały na aspirynie drażniącej błonę śluzową żołądka. W czerwcu 1958 roku został wypuszczony na rynek odpowiednik dla dzieci: Panadol Elixir. W 1963 roku paracetamol został wprowadzony do British Pharmacopoeia. Uzyskał znaczną popularność jako środek przeciwbólowy o niewielkiej liczbie działań niepożądanych i interakcji z innymi lekami – przy prawidłowym dawkowaniu niebezpieczeństwo groźnych dla życia powikłań było znikome.
W latach 60. XX wieku pojawiły się pierwsze doniesienia o niekorzystnych skutkach zażywania paracetamolu. W 1966 po raz pierwszy odnotowano ciężkie uszkodzenie wątroby po przedawkowaniu paracetamolu[17][18].
Spożycie paracetamolu systematycznie rosło na świecie. W krajach półkuli północnej pomiędzy 1978 a 1988 wzrosło pięciokrotnie, na przełomie lat 1994 i 1995 osiągając w niektórych krajach rozwiniętych poziom ponad 20 g/osobę/rok (w Wielkiej Brytanii, Stanach Zjednoczonych, Kanadzie, Australii, Nowej Zelandii poniżej 8 g/osobę/rok)[19][20]. W Belgii, liczącej 10 milionów mieszkańców, sprzedaje się rocznie w aptekach średnio 18,3 miliona opakowań paracetamolu[21]. W Polsce paracetamol należy do najczęściej sprzedawanych bez recepty leków przeciwbólowych[22].
Struktura i reaktywność[edytuj | edytuj kod]
Paracetamol zbudowany jest z pierścienia benzenowego podstawionego jedną grupą hydroksylową (-OH) i jedną acetylowaną grupą aminową (acetamidową) w układzie 1,4 (para). Jest to układ silnie sprzężony (patrz: dieny sprzężone), w którym delokalizacji ulega wolna para elektronowa tlenu hydroksylowego, chmura elektronowa π pierścienia, wolna para elektronowa azotu oraz elektrony grupy karbonylowej.
Obecność dwóch podstawników aktywujących sprawia, że pierścień benzenowy paracetamolu jest bardzo reaktywny w kierunku aromatycznej substytucji elektrofilowej. Oba podstawniki kierują w pozycje orto i para, co sprawia, że zaktywowane są wszystkie pozycje pierścienia. Podstawnik acetamidowy w pozycji para zwiększa kwasowość grupy hydroksylowej wskutek delokalizacji ładunku anionu fenoksylowego (pKa = 9,5 w porównaniu do pKa = 10,0 dla fenolu niepodstawionego)[23].
Synteza[edytuj | edytuj kod]
Początkowo w przemyśle stosowana była synteza, w której substratem wyjściowym do produkcji paracetamolu był fenol, który poddawano nitrowaniu za pomocą azotanu sodu w obecności kwasu siarkowego. W wyniku reakcji powstaje mieszanina zawierająca głównie p-nitrofenol i o-nitrofenol. Izomer para zostaje oddzielony od orto poprzez destylację frakcyjną:
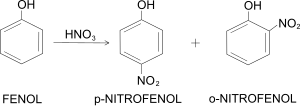
Następnie wyizolowany p-nitrofenol jest redukowany do p-aminofenolu, np. przy użyciu borowodorku sodu:
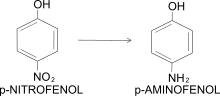
W ostatnim etapie syntezy p-aminofenol zostaje poddany acetylowaniu do N-acetylo-p-aminofenolu bezwodnikiem octowym w wodzie:

W latach 60. XX w. opatentowano modyfikację tej syntezy polegającą na otrzymywaniu w procesie elektrochemicznym paracetamolu wprost z p-nitrofenolu z pominięciem etapu redukcji do aminofenolu. W latach 70. XX w. zastąpiono syntezę nitrobenzenu z toluenu otrzymywaniem go z chlorobenzenu. Współcześnie istnieje wiele dróg syntezy paracetamolu i wciąż trwają badania nad znalezieniem nowych, bardziej ekonomicznych i omijających patenty największych producentów[24].
Farmakokinetyka[edytuj | edytuj kod]
Podany doustnie dobrze, szybko i prawie całkowicie wchłania się z przewodu pokarmowego, podany doodbytniczo wolniej. Dostępność biologiczna wynosi około 80%. Maksymalne stężenie we krwi osiąga po około 30–60 minutach. W około 25% wiąże się z białkami osocza, przy czym zwiększa się ono w miarę zwiększania dawki. Przenika do płynów ustrojowych i narządów wewnętrznych. Czas półtrwania T0,5 wynosi 3–4 godziny. Jest metabolizowany w wątrobie, wywołuje tam indukcję enzymów mikrosomalnych.
Wydalany jest z moczem głównie w postaci glukuronianów i siarczanów oraz po sprzężeniu z cysteiną i kwasem merkapturowym, a także produktów utleniania[25]. Mniej niż 5% opuszcza organizm w postaci niezmienionej[5]. W przypadku zaburzonej funkcji nerek dochodzi do kumulowania się sprzężonych metabolitów.
W moczu osób, które zażyły terapeutyczne dawki paracetamolu, stwierdzono obecność[26]:
- wolnego paracetamolu
- siarczanu paracetamolu
- siarczanu 3-hydroksy-paracetamolu
- siarczanu 3-metoksy-paracetamolu
- glukuronianu paracetamolu
- glukuronianu 3-metoksy-paracetamolu
- sprzężenia paracetamolu z cysteiną (w pozycji meta)
- sprzężenia paracetamolu z kwasem merkapturowym (w pozycji meta).
Te same związki były także obecne w moczu osób, które zażyły toksyczne dawki paracetamolu, ale w innych proporcjach – zanotowano wyraźny wzrost udziału sprzężenia paracetamolu z cysteiną oraz kwasem merkapturowym i nie odkryto innych, nowych metabolitów[26].
Mechanizm działania[edytuj | edytuj kod]

Paracetamol działa głównie przeciwbólowo i przeciwgorączkowo, a także wykazuje bardzo słabe działanie przeciwzapalne, lecz nie znosi objawów stanu zapalnego ani nie osłabia funkcji płytek krwi i charakteryzuje się niskim ryzykiem pojawienia się działań niepożądanych w porównaniu do aspiryny i niesteroidowych leków przeciwzapalnych[27].
Mechanizm działania w dalszym ciągu nie został ostatecznie wyjaśniony, pomimo że paracetamol już od ponad pół wieku jest stosowany w lecznictwie. Wiadomo, że za jego działanie odpowiadają co najmniej dwa szlaki metaboliczne[28][29][30][31]. Jeden z nich opiera się najprawdopodobniej na wybiórczym blokowaniu enzymu cyklooksygenazy COX-3[32], który u ludzi jest obecny w dużych ilościach w korze mózgowej i sercu[33]. Opierając się na doświadczeniach przeprowadzonych na psach, naukowcy wykazali, że enzym COX-3 jest wybiórczo blokowany przez leki przeciwbólowo-przeciwgorączkowe, tj. paracetamol i fenacetynę, natomiast silnie blokowany przez niektóre leki z grupy NLPZ, sugerując że ten mechanizm może być głównie odpowiedzialny za działanie przeciwbólowo-przeciwgorączkowe[32]. Paracetamol nie powoduje zahamowania syntezy prostaglandyn na obwodzie, dzięki czemu jest pozbawiony efektów ubocznych, które charakteryzują niesteroidowe leki przeciwzapalne z grupy NSAID.
Uważa się też, że wpływ paracetamolu na układ serotoninergiczny w korze mózgowej, moście i trombocytach (podczas krótkotrwałego stosowania paracetamolu dochodzi do zwiększenia poziomu serotoniny; długotrwałe podawanie prowadzi paradoksalnie do odwrotnego efektu)[34] oraz hamowanie syntezy prostaglandyny E2 w makrofagach obecnych w mózgu, są również częściowo odpowiedzialne za mechanizm działania przeciwbólowego[35].
Grupa innych naukowców zauważyła, opierając się na doświadczeniach przeprowadzonych na szczurach, że efekt przeciwbólowego działania paracetamolu został zniesiony przez dwa antagonisty receptora kannabinoidowego CB1, użyte w dawkach, które znosiły działanie przeciwbólowe agonisty receptora kannabinoidowego CB1 i wyciągnęła wniosek, że z mechanizmem działania przeciwbólowego paracetamolu związany jest także układ endokannabinoidowy odpowiedzialny za działanie kannabinoidów[36].

Badania przeprowadzone na szczurach, którym podawano paracetamol, doprowadziły do odkrycia w układzie nerwowym nowego, czynnego biologicznie metabolitu paracetamolu – N-arachidonoilofenolaminy (amidu kwasu arachidonowego i p-aminofenolu), określanej skrótem AM404. AM404 powstaje w wyniku deacetylacji paracetamolu do p-aminofenolu, który następnie ulega w mózgu, rdzeniu kręgowym i wątrobie acylowaniu resztą kwasu arachidonowego. Reakcje deacetylacji i kondensacji z kwasem tłuszczowym są katalizowane enzymatycznie przez hydrolazę amidu kwasu tłuszczowego FAAH. AM404 jest silnym agonistą receptora TRPV1, blokuje COX-1 i COX-2, hamując syntezę prostaglandyn w makrofagach, a także oddziałuje na układ endokannabinoidowy (receptor waniloidowy) – wszystkie te czynniki są związane z odczuwaniem bólu i regulacją temperatury ciała. AM404 należy do grupy amidów typu N-acyloamin (podobnie jak anandamid) i uważa się, że stanowi łącznik pomiędzy paracetamolem i układem endokannabinoidowym. Do tej pory nie udało się potwierdzić obecności AM404 u człowieka[27].
Metabolizm[edytuj | edytuj kod]

Paracetamol ulega metabolizowaniu (unieczynnieniu) w wątrobie na drodze reakcji sprzęgania oraz utleniania.
W wyniku sprzęgania paracetamolu z resztą kwasu siarkowego i glukuronowego powstają nieaktywne i nietoksyczne metabolity: siarczany (30%) i glukuroniany (50%), które nie ulegają zwrotnemu wchłanianiu w kanalikach nerkowych i są wydalane wraz z moczem[37].
Około 5% paracetamolu zostaje wydalone w postaci niezmienionej przez nerki.
W 5% (maks. 20%)[37] dochodzi do metabolizmu zależnego od układu enzymatycznego cytochromu P450 (głównie przez izoformę CYP2E1, rzadziej przez CYP1A2 i CYP3A4).
Enzymatyczne utlenianie niewielkiej ilości paracetamolu (3%) przy udziale CYP2A6 i CYP2B1 prowadzi do powstania 3-hydroksy-paracetamolu, który po metylacji do 3-metoksy-paracetamlu, jest sprzęgany z wytworzeniem glukuronianów i siarczanów wydalanych w moczu[37].
W wyniku reakcji utleniania przy udziale izoformy CYP2E1 (także obecnej w nerkach) dochodzi do powstania toksycznego metabolitu N-acetylo-4-benzochinonoiminy (NAPQI), utleniacza (reagującego z grupami -SH w zredukowanym glutationie), który jest odpowiedzialny za rozwój ewentualnego ciężkiego zatrucia paracetamolem w przypadku wysycenia obu szlaków metabolicznych, do którego dochodzi m.in. po przekroczeniu dawek terapeutycznych lub wyczerpaniu ustrojowych zapasów siarczanów i glukuronianów[37][38], albowiem wysycenie szlaku metabolicznego prowadzącego do powstawania siarczanów i glukuronianów paracetamolu prowadzi do wzmożonego metabolizowania paracetamolu na drodze utleniania i powstawania NAPQI[39].
NAPQI ulega detoksykacji poprzez nieenzymatyczną reakcję[37] z grupami sulfhydrolowymi glutationu, lub z innymi związkami zawierającymi grupę tiolową (N-acetylocysteina), z ostatecznym wytworzeniem sprzężenia z kwasem merkapturowym. Powstałe w ten sposób nieaktywne i nietoksyczne metabolity są wydalane przez nerki[38].
W niektórych przypadkach jako odtrutka polecana jest także metionina[40], chociaż większość badań dowodzi, że N-acetylocysteina jest skuteczniejszym antidotum przy przedawkowaniu paracetamolu[41]. Wyczerpanie komórkowych rezerw glutationu i kumulacja NAPQI prowadzi do całkowitego zniszczenia wątroby i śmierci[42].
U niemowląt paracetamol jest metabolizowany głównie do siarczanów, zaś u osób dorosłych paracetamol jest przede wszystkim sprzęgany z kwasem glukuronowym[39].
Zaobserwowano znaczne różnice osobnicze w zdolności do nieuczynniania paracetamolu poprzez sprzęgania z resztą kwasu glukuronowego i siarkowego[37].
W przypadku spożycia wysokich dawek paracetamolu (>10 g) dochodzi do wyczerpania glutationu z następczym toksycznym uszkodzeniem hepatocytów przez NAPQI, który wchodzi w reakcje z białkami. Tworzy się martwica centralnej części zrazików (strefy 3). Ten obszar charakteryzuje się największą aktywnością izoformy CYP2E1 i najmniejszym stężeniem glutationu[43].
Głównym miejscem toksycznego działania NAPQI jest wątroba. W mniejszym stopniu dochodzi również do uszkodzenia nerek (w komórkach cewek nerkowych również jest obecny i aktywny CYP2E1, a w wyniku działania NAPQI rozwija się ostra martwica cewkowa) oraz mięśnia sercowego i trzustki (efekt pierwotny wywołany kumulacją metabolitów lub wtórny do niewydolności wątroby i postępującej niewydolności wielonarządowej). Wydostający się z hepatocytów NAPQI uszkadza także białka osocza, hemoglobinę oraz nabłonek płuc[37].
Szczególnie narażone na toksyczne działanie paracetamolu są osoby nadużywające alkoholu[44], przewlekle przyjmujący leki indukujące CYP2E1 (szczególnie barbiturany, imidazol, ryfampicynę[45], karbamazepinę, fenytoinę[46][47], izoniazyd – w tym przypadku mechanizm jest dwufazowy: początkowa inhibicja enzymu, po której następuje indukcja[45][48]), cukrzycy i osoby głodzące się (ze względu na zwiększone powstawanie w organizmie ketonów) oraz palacze papierosów. Również niektóre choroby genetyczne prowadzące do zaburzeń w obrębie enzymów sprzęgających (zespół Gilberta) mogą prowadzić do poważnych powikłań przy jednoczesnym zażywaniu leku. W literaturze pojawiają się doniesienia o genetycznie uwarunkowanych indywidualnych różnicach w szybkości metabolizowania paracetamolu u ludzi, które związane są z indywidualnymi różnicami w aktywności cytochromu P450, szybkości sprzęgania do glukuronianów i siarczanów, dostępności glutationu oraz zdolnościach regeneracyjnych. Ten czynnik nie pozwala przewidzieć wielkości dawki paracetamolu, ani czasu podawania, które mogą okazać się toksyczne dla danego indywiduum[49].
Wśród innych czynników ryzyka związanych z wyczerpywaniem rezerw glutationu wymienia się:
- zaburzenia odżywiania
- mukowiscydozę
- zakażenie HIV[50]
- schorzenia wątroby i jelit
- systematyczne nadużywanie paracetamolu[39]
- przewlekłe nadużywanie alkoholu; przyjęcie nawet niewielkich dawek paracetamolu przez osoby systematycznie nadużywające napojów alkoholowych może prowadzić do uszkodzenia wątroby – jest to tzw. zespół alkoholowo-paracetamolowy.
Wskazania[edytuj | edytuj kod]
Paracetamol – lek uśmierzający ból i obniżający podwyższoną temperaturę ciała – stosuje się w następujących przypadkach:
- gorączce i bólu w przebiegu grypy
- przeziębieniu
- bólu głowy
- bólu zęba
- bólach menstruacyjnych
- lumbago
- nerwobólach
- bólu mięśniowym
- chorobie zwyrodnieniowej stawów (lekkie i średnio nasilone bóle w artrozie biodra i kolana)
- bólu po szczepieniu
- bólach pooperacyjnych
- bólach nowotworowych (pojedynczo oraz w połączeniu z kodeiną lub innym opioidem)[5].
Przeciwwskazania i środki ostrożności[edytuj | edytuj kod]
- Nadwrażliwość na paracetamol lub którykolwiek ze składników pomocniczych[51].
- Nie zaleca się długotrwałego ani częstego stosowania paracetamolu.
- Należy zachować ostrożność w przypadku zaburzenia funkcji wątroby i nerek, systematycznego spożywania napojów alkoholowych, stanu niedożywienia i odwodnienia.
- Dożylne podawanie paracetamolu należy ograniczyć wyłącznie do szczególnych przypadków klinicznych.
- W przypadku homozygotycznych pacjentów chorych na fenyloketonurię należy w przypadku tabletki do ssania wliczyć ilość fenyloalaniny w dietę[5].
- Nie zaleca się ponownego podawania dzieciom, u których wystąpiła encefalopatia po wcześniejszym podaniu paracetamolu[39].
- Nie powinny przyjmować paracetamolu osoby z wrodzonym niedoborem dehydrogenazy glukozo-6-fosforanowej[13].
- Osoby, u których stwierdzono występowanie zespołu Gilberta, zespołu Criglera-Najjara lub zespołu Dubina-Johnsona powinny skonsultować ewentualne zażycie paracetamolu z lekarzem.
- Paracetamolu nie powinny przyjmować osoby z niedokrwistością[13].
- Paracetamol jest przeciwwskazany w pierwszym trymestrze ciąży. Po upływie 3 miesiąca ciąży oraz w okresie laktacji – wyłącznie po zasięgnięciu opinii lekarza[13].
- Różne badania naukowe wykazały związek pomiędzy stosowaniem paracetamolu a diagnozowaniem nowo powstałej astmy oskrzelowej u dorosłych – o 63% więcej przypadków w grupie osób systematycznie zażywających paracetamol w porównaniu do grupy osób nie zażywających paracetamolu. Przypuszcza się, że mechanizm tego fenomenu może mieć związek ze zmniejszeniem ilości glutationu w płucach oraz stresem oksydacyjnym[52][53]. Autorzy stwierdzają, że nie ma jeszcze wystarczających dowodów, aby uznać paracetamol za lek przeciwwskazany dla pacjentów z astmą oskrzelową i sugerują przeprowadzanie dalszych badań w celu potwierdzenia lub wykluczenia związku pomiędzy paracetamolem a astmą oskrzelową[54]. W badaniu z 2008 stwierdzono związek pomiędzy podawaniem paracetamolu niemowlętom i dzieciom a częstszym występowaniem astmy w wieku 6–7 lat[55].
Działania niepożądane[edytuj | edytuj kod]
W dawkach terapeutycznych paracetamol nie wykazuje zbyt wielu działań niepożądanych oraz nie drażni błony śluzowej żołądka i jelit, tym niemniej przy zalecanych dawkach mogą pojawić się:
- odczyny alergiczne (świąd, pokrzywka, wysypka, rumień)
- zaburzenia ze strony przewodu pokarmowego (nudności, wymioty)
- uszkodzenie wątroby (żółtaczka, martwica) i nerek (zapalenie, martwica), głównie podczas długotrwałego przyjmowania wysokich dawek
- zaburzenia w układzie krwiotwórczym (methemoglobinemia, agranulocytoza, trombocytopenia)[5].
Interakcje[edytuj | edytuj kod]
- Kofeina wzmaga działanie paracetamolu. Interakcja wykorzystana w preparatach złożonych[13].
- Salicylamidy wydłużają okres działania paracetamolu[13].
- Jednoczesne stosowanie aspiryny i paracetamolu prowadzi do podwyższenia stężenia obu leków we krwi[56].
- Działanie doustnych leków przeciwzakrzepowych może ulec wzmożeniu podczas długotrwałego stosowania wysokich dawek paracetamolu.
- Węgiel aktywny i cholestyramina osłabiają wchłanianie paracetamolu.
- Spożywanie napojów alkoholowych łącznie z paracetamolem może prowadzić do toksycznego uszkodzenia wątroby, nawet w przypadku stosowania zalecanych w ulotce dawek.
- Jednoczesne stosowanie innych leków indukujących enzymy wątrobowe (cytochrom P450), do których należą na przykład barbiturany, izoniazyd, ryfampicyna, karbamazepina, fenytoina może prowadzić do toksycznego uszkodzenia wątroby nawet w przypadku stosowania dawek zalecanych w ulotce.
- Przy jednoczesnym i systematycznym stosowaniu paracetamolu z zydowudyną częściej dochodzi do neutropenii, najprawdopodobniej ze względu na zmniejszenie metabolizowania zydowudyny[5].
- Paracetamol wyraźnie wydłuża okres półtrwania chloramfenikolu[51].
- Jednoczesne stosowanie paracetamolu z innym lekiem z grupy NLPZ zwiększa ryzyko uszkodzenia nerek[56].
Dawkowanie[edytuj | edytuj kod]
Paracetamol jest lekiem przeciwbólowo-przeciwgorączkowym dozwolonym do stosowania u osób dorosłych oraz u dzieci. Paracetamol może być podawany doustnie (tabletki, syrop, tabletki do ssania, tabletki do żucia itp.), doodbytniczo (czopki) oraz pozajelitowo (dożylnie).
Osoby dorosłe i dzieci powyżej 12. roku życia[edytuj | edytuj kod]
| Drogi podawania | Dawkowanie[5] |
|---|---|
| Doustnie |
|
| Doodbytniczo |
|
| Pozajelitowo |
|
- Nie należy przekraczać maksymalnej dawki jednorazowej, czyli 500–1000 mg (1–2 tabletki po 500 mg).
- Nie należy przekraczać maksymalnej dawki dziennej, czyli 3000 mg (6 tabletek po 500 mg).
- Należy zachować co najmniej 4-godzinną przerwę między kolejnymi zażyciami leku.
- Dawkę powtarza się jedynie, gdy ból i gorączka nie ustąpiły całkowicie lub powróciły.
- Paracetamolu nie należy stosować często, ani długotrwale. Producent ostrzega, że w przypadku długotrwałego przyjmowania 3–4 gramów paracetamolu dziennie (6–8 tabletek 500-miligramowych) może dojść do uszkodzenia wątroby, także jednorazowe przyjęcie 6 gramów (12 tabletek 500-miligramowych) może prowadzić do uszkodzenia wątroby[51].
- Jeżeli objawy trwają dłużej niż 14 dni lub mają charakter nawracający – należy skontaktować się z lekarzem.
- W przypadku przyjęcia większej ilości paracetamolu (jednorazowo lub dziennie) niż zalecana w ulotce należy jak najszybciej skontaktować się z lekarzem. W przypadku zwłoki dochodzi do trwałego uszkodzenia wątroby. W zatruciu paracetamolem najczęściej nie występuje utrata przytomności.
- Nieprzyjęcie dawki paracetamolu nie powoduje żadnych negatywnych konsekwencji. Należy kontynuować według zlecenia, o ile jest to konieczne, ale bez zażywania zapomnianej dawki.
- Stosowanie paracetamolu można przerwać w dowolnym momencie bez wystąpienia jakichkolwiek negatywnych efektów.
- Paracetamol występuje na rynku pod różnymi nazwami handlowymi oraz wchodzi w skład licznych preparatów złożonych (patrz rozdział Preparaty dostępne w Polsce), w związku z tym pacjenci zażywający więcej niż jeden lek przeciwbólowy powinni skontrolować, które z nich zawierają paracetamol i nie przekraczać dopuszczalnej dawki jednorazowej i dobowej paracetamolu, będącej sumą ilości paracetamolu z różnych preparatów.
- Osoby przyjmujące inne leki powinny przed zażyciem paracetamolu sprawdzić w ulotce, czy nie istnieją przeciwwskazania do ich łączenia.
- Osoby cierpiące na choroby genetyczne, choroby chroniczne itd. w przypadku stosowania leku OTC zawsze powinny sprawdzić w ulotce, czy nie istnieją przeciwwskazania do stosowania paracetamolu.
Dzieci poniżej 12. roku życia[edytuj | edytuj kod]
| Wiek dziecka | Doustnie[5] | Doodbytniczo[5] |
|---|---|---|
| 3–12 miesięcy | jednorazowo 10 mg/kg masy ciała 4–6 razy/dobę | 60 mg 2–4 razy/dobę dla dzieci o wadze ciała 3–5,5 kg; 120–125 mg 2–3 razy/dobę przy wadze ciała 5,5–10 kg |
| 1–2 lata | 120 mg 4–6 razy/dobę | 240–250 mg 2–3 razy/dobę |
| 2–4 lata | 120–180 mg 4–6 razy/dobę | 240–250 mg 3 razy/dobę |
| 4–6 lat | 180 mg 4–6 razy/dobę | 240–250 mg 4 razy/dobę |
| 6–9 lat | 240–250 mg 4–6 razy/dobę | 500 mg 2–3 razy/dobę |
| 9–12 lat | 360–375 mg 4–6 razy/dobę | 500 mg 3 razy/dobę |
Paracetamol można dawkować dzieciom także w przeliczeniu na masę ciała, a nie na wiek. W takim przypadku powinno się podawać (zarówno doustnie, jak i doodbytniczo) od 10 do 15 mg na kilogram masy ciała. Maksymalna dawka dobowa wynosi 60 mg/kg m.c. i powinna być podawana co najmniej w czterech dawkach (po 15 mg/kg m.c.).
W przypadku pozajelitowego podawania paracetamolu (dożylnie) dawkę również oblicza się na podstawie masy ciała dziecka. Dawka jednorazowa wynosi 15 mg/kg masy ciała przy masie ciała od 10 do 50 kg. Dawkę można powtórzyć maksymalnie 4 razy w ciągu 24 godzin, zachowując przynajmniej 4-godzinną przerwę między jednym a drugim podaniem. Dawka maksymalna wynosi 60 mg/kg masy ciała/dobę. Należy zachować przynajmniej 6 godzinną przerwę między podaniami dożylnymi w przypadku współistnienia zaburzonej funkcji nerek (klirens kreatyniny < 30 ml/min)[5]. Paracetamol podaje się dożylnie jedynie przez krótki okres, w średnio nasilonych bólach pooperacyjnych oraz w przypadku wysokiej gorączki, gdy sytuacja wymaga podania pozajelitowego.
- Noworodkom oraz niemowlętom aż do ukończenia 3 miesiąca życia wolno podawać paracetamol wyłącznie na zalecenie lekarza.
- W przypadku dzieci poniżej 4. roku życia nie zaleca się podawać paracetamolu dłużej niż 2 dni.
Stosowanie w ciąży i podczas karmienia piersią[edytuj | edytuj kod]
Krótkotrwałe, doustne stosowanie paracetamolu ściśle według wskazań lekarza jest dozwolone dla kobiet w ciąży oraz matek karmiących piersią[5], ale niektórzy lekarze uważają, że paracetamolu nie powinny stosować kobiety w pierwszym trymestrze ciąży[13]. Podczas dłuższego podawania zaleca się zachowanie ostrożności. Paracetamol przenika przez łożysko. Do tej pory nie zaobserwowano szkodliwego wpływu paracetamolu na przebieg ciąży oraz stan zdrowia płodu i niemowlęcia. Paracetamol przenika w niewielkiej ilości do mleka matki, ale jak do tej pory nie zaobserwowano szkodliwego wpływu na dziecko. Powyższe informacje nie dotyczą dożylnego podawania paracetamolu kobietom w ciąży lub karmiącym. Ze względu na brak dostatecznej ilości danych klinicznych bezpieczeństwo dla tej drogi podania nie zostało określone[5].
Ryzyko astmy[edytuj | edytuj kod]
Jedno badanie naukowe wykazało istnienie związku pomiędzy pojawianiem się astmy oskrzelowej u dzieci we wczesnym dzieciństwie a narażeniem na paracetamol w okresie życia płodowego. Ryzyko pojawienia się astmy lub zapalenia oskrzeli zostało określone jako małe, ale statystycznie wyraźnie zwiększone. Najwyższe ryzyko wystąpienia zaburzeń astmatycznych zaobserwowano u dzieci matek, które stosowały paracetamol w pierwszych trzech miesiącach ciąży[57].
Wpływ na prowadzenie pojazdów[edytuj | edytuj kod]
Jak do tej pory nie zaobserwowano negatywnego wpływu paracetamolu na zdolność do prowadzenia pojazdów mechanicznych i obsługiwania maszyn[51].
Sposób zażywania[edytuj | edytuj kod]
W zależności od rodzaju tabletki: tabletki przeznaczone do rozpuszczenia w jamie ustnej należy ssać, ale nie gryźć; tabletki do żucia żuć lub przyjmować rozkruszone z płynem; zwykłe tabletki rozpuścić w dużej ilości wody, zamieszać i wypić. Rozpuszczenie tabletki w wodzie przed połknięciem przyśpiesza jej wchłanianie z przewodu pokarmowego do krwiobiegu, a tym samym przyśpiesza wystąpienie efektu leczniczego oraz skraca czas kontaktu paracetamolu z błoną śluzową żołądka, zmniejszając możliwość jej podrażnienia. Specjalnie dla dzieci znajdują się w handlu syropy z paracetamolem. Istnieją również preparaty paracetamolu do podania dożylnego.
Przedawkowanie[edytuj | edytuj kod]
Przedawkowanie paracetamolu może zakończyć się zejściem śmiertelnym pacjenta. U osób dorosłych przyjęcie jednorazowej dawki ≥ 6 gramom prowadzi do lizy hepatocytów. Przyjmuje się, że jednorazowa dawka wywołująca lizę komórek wątroby u dzieci wynosi > 140–150 mg/kg masy ciała. Dawka 20–25 gramów jest uważana za śmiertelną[5]. Według innych autorów już około 200 mg/kg masy ciała (~15 gramów) jest uważane za śmiertelne[13].
Objawy przedawkowania nie pojawiają się natychmiast, lecz dopiero po upływie 24 godzin, a nawet 48 lub 72 godzin, ale proces nieodwracalnego niszczenia wątroby rozpoczyna się już w pierwszych godzinach po przedawkowaniu[49], dlatego zatrucie paracetamolem ma bardzo podstępny charakter.
Dzieci są nieco mniej wrażliwe na zatrucie paracetamolem w porównaniu do osób dorosłych, albowiem mają większy zapas glutationu w wątrobie oraz w mniejszym stopniu zachodzi u nich reakcja utleniania do NAPQI[39].
- Zatrucie ostre
U dorosłych ostre zatrucie paracetamolem występuje po przyjęciu > 4 gramów paracetamolu w czasie mniejszym niż 8 godzin lub > 150 mg/kg masy ciała. W przypadku dzieci mówi się, że do ostrego zatrucia paracetamolem dochodzi po przyjęciu jednorazowej dawki większej od 150 mg/kg masy ciała. Jednorazowa dawka > 300 mg/kg masy ciała dziecka prowadzi do zgonu[39].
- Zatrucie przewlekłe
Związane jest z powtarzającym się zażywaniem podwyższonych dawek paracetamolu i jest coraz częściej asocjowane ze stwierdzanymi uszkodzeniami wątroby oraz zgonami z powodu niewydolności wątroby. Dla dzieci już dawki ≥90 mg/kg/dobę mogą okazać się toksyczne dla miąższu wątroby, jeżeli będą podawane przez kilka kolejnych dni. Działanie toksyczne może wystąpić nawet w przypadku podawania dzieciom dawek terapeutycznych, czyli 60–90 mg/kg/dobę. Najprawdopodobniej związane jest to z indywidualną nadwrażliwością danego pacjenta na paracetamol i uszkodzenie komórek wątrobowych[39].
Toksyczność paracetamolu zwiększa się w następujących sytuacjach:
- u osób starszych
- u małych dzieci
- u osób systematycznie spożywających napoje alkoholowe
- przy odwodnieniu organizmu
- przy poszczeniu
- przy niedożywieniu (mniejszy zapas glutationu)
- przy diecie ubogiej w białka
- w chorobach wątroby i nerek
- prawdopodobnie także u palaczy tytoniu[5]
- przy jednoczesnym stosowaniu innych leków zwiększających aktywność systemu enzymatycznego cytochromu P450, na przykład leków przeciwpadaczkowych[39]
- przy jednoczesnym stosowaniu innych leków przeciwbólowych (opioidów i NSLP) oraz preparatów złożonych
- przy genetycznie uwarunkowanym wolnym metabolizowaniu paracetamolu (związanym z osobniczymi różnicami w aktywności cytochromu P450, dostępnością glutationu, zdolnością do tworzenia glukuronianów i siarczanów oraz zdolnościami regeneracyjnymi), które na aktualnym poziomie rozwoju farmakogenetyki nie jest jeszcze możliwe do określenia dla indywidualnego pacjenta[49].
Objawy przedawkowania[edytuj | edytuj kod]
Wczesnymi objawami przedawkowania występującymi w pierwszych 24 godzinach od przyjęcia leku są:
- złe samopoczucie
- bladość
- zmniejszona samoświadomość, przy czym nie występuje utrata przytomności
- brak łaknienia
- nudności
- wymioty
- bóle brzucha.
Wczesnym, niekorzystnym wskaźnikiem rokowniczym w zatruciu paracetamolem jest zwiększone stężenie dehydrogenazy mleczanowej w osoczu. W badaniu laboratoryjnym krwi stwierdza się bardzo podwyższone wartości transaminaz (> 4000 U/l), a tylko lekko podwyższone wartości całkowitej bilirubiny (< 200 µmol/l), obok hipoglikemii, która występuje u 30% pacjentów. Ponadto w 12 do 48 godzin pojawia się obniżony poziom protrombiny[5]. Choroby metaboliczne oraz stany zapalne mogą maskować wyniki badań charakterystyczne dla zatrucia paracetamolem[39].
W drugiej dobie mogą pojawić się:
- żółtaczka
- objawy grypopodobne[58]
- świąd[58]
- zaburzenia orientacji i senność
- zaburzenia krzepnięcia krwi
- hipoglikemia
- kwasica metaboliczna
- encefalopatia
- śpiączka.
Stanowią one objawy ostrej niewydolności wątroby spowodowanej martwicą komórek wątroby i są najbardziej wyraźne po 4–6 dniach od zatrucia.
Inne ogólnoustrojowe objawy obserwowane w przebiegu zatrucia:
- zaburzenia rytmu serca
- spadek ciśnienia tętniczego krwi
- sinica wywołana methemoglobinemią
- skąpomocz
- drgawki
- niewydolność oddechowa
- zapaść krążeniowa[13].
Postępowanie w zatruciu[edytuj | edytuj kod]
W przypadku zatrucia paracetamolem pacjent zostaje natychmiast przyjęty do szpitala. Procedura detoksykacyjna obejmuje w zależności od czasu, który upłynął od przyjęcia ostatniej dawki oraz stanu pacjenta:
- płukanie żołądka
- podawanie węgla aktywnego (jako środka absorbującego) oraz siarczanu sodu (jako środka przeczyszczającego)
- jak najszybsze rozpoczęcie dożylnego (zalecane), przez sondę lub doustnego podawania odtrutki N-acetylocysteiny[5].
Podczas procesu detoksykacyjnego kontroluje się stężenie paracetamolu w osoczu pacjenta i na podstawie uzyskanych wyników określa czas podawania odtrutki. Terapia per os trwa z reguły 72 godziny. Doustne podawanie N-acetylocysteiny stosuje się w łagodniejszych postaciach zatruć paracetamolem u osób współpracujących z lekarzem, niemających nudności i niewymiotujących oraz u których nie podano jeszcze węgla aktywnego. W przypadku doustnego podawania odtrutki nie podaje się węgla aktywnego i siarczanu sodu ze względu na zaburzenie wchłaniania N-acetylocysteiny. Terapię doustną N-acetylocysteiną stosuje się także jako kontynuację uprzedniego dożylnego podania antidotum. W ciężkich zatruciach stosuje się dożylne podawanie N-acetylocysteiny[59].
Duże dawki N-acetylocysteiny mogą wywołać u pacjentów cierpiących na astmę napady duszności, w tym przypadku podaje się dodatkowo leki przeciwastmatyczne[59].
Antidotum: N-acetylocysteina – prekursor glutationu i przeciwutleniacz; najprawdopodobniej chroni hepatocyty przed dalszym uszkodzeniem, działając przeciwzapalnie i poprawiając krążenie w naczyniach krwionośnych włosowatych poprzez ich rozszerzenie. Podawanie N-acetylocysteiny zaleca się bez względu na czas który upłynął od momentu zażycia toksycznej dawki paracetamolu. Opisano przypadki korzystnego wpływu nawet w przypadku podania N-acetylocysteiny w 47 godzin od wystąpienia objawów chronicznego zatrucia paracetamolem. Efektywność postępowania odtruwającego w przedawkowaniu oraz czas, który upłynął od chwili przyjęcia ostatniej dawki paracetamolu mają znaczący wpływ na dalszą prognozę dla pacjenta. Osoby młode z ostrą niewydolnością wątroby w zatruciu paracetamolem mają większą szansę na przeżycie niż dorośli[39].
Ciężkie zatrucia paracetamolem często prowadzą do ostrej niewydolności wątroby. Jeżeli leczenie zachowawcze nie rokuje pomyślnych rezultatów, to pacjenta kwalifikuje się do przeszczepienia wątroby[60]. Ostra niewydolność wątroby może wymagać wykonania takiego zabiegu w ciągu kilku dni. Zwraca się również uwagę na psycho-socjalne konsekwencje dla pacjenta związane z dokonaniem przeszczepienia, wynikające np. z oczekiwania na właściwy organ, niepewności co do powodzenia zabiegu chirurgicznego i otrzymania na czas przeszczepu, zanim stan zdrowia pogorszy się na tyle, że zabiegu nie będzie można dokonać, konieczności zażywania do końca życia leków zapobiegających odrzuceniu przeszczepu oraz lęku przed możliwością odrzucenia przez organizm przeszczepionej wątroby[61]. W Stanach Zjednoczonych zatrucie paracetamolem jest odpowiedzialne za 40% przypadków ostrej niewydolności wątroby wywołanej lekami. Przeżycie zależy od ciężkości encefalopatii wątrobowej oraz pojawiających się komplikacji, głównie infekcji. Ponad 43% pacjentów udaje się pokonać ostrą niewydolność wątroby, 28% umiera, a u 29% dokonuje się przeszczepienia wątroby[62]. Po dokonaniu przeszczepienia wątroby 60–80% pacjentów ma szansę na przeżycie przynajmniej jednego roku. W przypadku niewykonania przeszczepu ta szansa wynosi 7–36%[63] w zależności m.in. od czasu, który upłynął od momentu wystąpienia żółtaczki do momentu pojawienia się encefalopatii.
Dane statystyczne i epidemiologiczne[edytuj | edytuj kod]
W Polsce jeszcze nie istnieje system monitorowania i kontroli zatruć paracetamolem[56]. W 2006 Szpital Praski udzielił około 160 porad związanych z przedawkowaniem tego leku[56]. Według FDA w latach 1993–1999 w USA miało miejsce 56 000 interwencji medycznych z powyższego powodu[56], zaś w latach 1990–1999 26 000 osób trafiło do szpitala[56]. Nieświadome przedawkowania paracetamolu wynikają z jednoczesnego zażywania dużej liczby leków przeciwbólowych różnych marek zawierających go w swoim składzie[56].
Według Ciszowskiego, Gomółki i Jennera – autorów artykułu w „Przeglądzie Lekarskim” – także w Polsce zatrucia paracetamolem oraz paracetamolem w połączeniu z innymi lekami stanowią poważny problem diagnostyczny i terapeutyczny[64]. W 2002 klinika toksykologii udzieliła pomocy 71 osobom, w 2003 82 osobom, a w 2004 47 pacjentom z powodu ostrego zatrucia paracetamolem o stężeniu w surowicy powyżej 20 mg/l[64].
Także problem uzależnienia od paracetamolu i innych leków przeciwbólowych jest rzadko dyskutowany, choć w krakowskiej klinice toksykologii, do której od grudnia 2002 do grudnia 2004 przyjęto 221 pacjentów zatrutych paracetamolem, uważa się, że powszechne zażywanie tego leku przyczynia się do wzrostu liczby zatruć[65].
Grażyna Świątkiewicz w czasopiśmie „Alkoholizm i Narkomania” zwróciła uwagę na negatywną rolę reklamy leków, która była odbierana przez konsumentów zbyt dosłownie, bez dystansu[65], szczególnie na początku lat 90. wraz z pojawieniem się wolnego rynku[65]. Zaznaczyła także, że intensywna reklama jest kierowana również do lekarzy, przy jednoczesnym ograniczonym dostępie do obiektywnej informacji o lekach[65].
W „Przeglądzie Lekarskim” podkreślono, że zatrucia paracetamolem są w Polsce coraz powszechniejszym problemem[64]. Zwrócono także uwagę na łatwą dostępność tego leku bez wymogu posiadania recepty[64].
Ewentualna profilaktyka[edytuj | edytuj kod]
Dodawanie metioniny do tabletek z paracetamolem w celu zapobiegania ewentualnym zatruciom przypadkowym lub umyślnym jest uzasadnione z biochemicznego punktu widzenia. Metionina okazała się skuteczna w badaniach wykonanych na zwierzętach oraz próbach klinicznych z osobami, które przedawkowały paracetamol. Najprawdopodobniej metionina wzmaga syntezę glutationu, który z kolei bierze udział w procesie unieczynniania hepatotoksycznego metabolitu paracetamolu NAPQI. Bardzo ważną rolę odgrywa czas, który upływa pomiędzy przyjęciem toksycznej dawki paracetamolu a podaniem metioniny, albowiem jedynie nieuszkodzone komórki wątrobowe są w stanie przemienić metioninę do cysteiny, która z kolei służy do syntezy glutationu. Badania kliniczne wykazały skuteczność doustnego lub dożylnego podania metioniny w zapobieganiu masywnemu zniszczeniu wątroby, jeżeli od momentu przedawkowania upłynęło do 10 godzin[66].
W Wielkiej Brytanii w handlu znajduje się jeden preparat o nazwie Paradote®, który zawiera w tabletce 500 mg paracetamolu i 100 mg metioniny. Podobne preparaty złożone, jak do tej pory, nie występują na rynku farmaceutycznym w innych krajach Europy, ani w Stanach Zjednoczonych[66].
Zastrzeżenia[66] w stosunku do łącznego stosowania paracetamolu i metioniny są następujące:
- wyższa cena dla konsumenta
- metionina ma niewiele działań ubocznych, lecz może wywoływać w niektórych przypadkach nudności i ból głowy
- nieprzyjemny smak
- stosowana jest mieszanina racemiczna metioniny, podczas gdy jedynie forma lewoskrętna jest wykorzystywana w metabolizmie u człowieka
- nie ustalono skutecznej i bezpiecznej dawki metioniny jako antidotum do łącznego stosowania z paracetamolem.
Należy ustalić bezpieczeństwo długoterminowej dodatkowej podaży metioniny w stosunku do ilości znajdującej się w pożywieniu. Badania na zdrowych osobach, którym dodatkowo podawano metioninę w diecie, wykazały:
- zmniejszenie stężenia kwasu foliowego w osoczu
- leukocytozę
- zmiany w pH i stężeniu potasu w osoczu
- zwiększone wydalanie wapnia z moczem
- u pacjentów chorych na schizofrenię doszło do rozwoju psychoz funkcjonalnych (podawano 10–20 g/24 h przez 2 tygodnie)
- pojedyncze dawki 8 g cysteiny wywoływały encefalopatię wątrobową u chorych z marskością wątroby
- nie oszacowano wpływu dodatkowej i długotrwałej konsumpcji metioniny na proces karcynogenezy u człowieka
- nie przebadano wpływu zwiększonego poziomu homocysteiny w osoczu na choroby obwodowych naczyń krwionośnych, niedokrwienną chorobę serca, zaburzenia krzepnięcia krwi, ryzyko wylewu i śródbłonek.
Autorzy cytowanego artykułu uważają, że do czasu poznania wszystkich efektów długoterminowego stosowania metioniny u ludzi nie powinna ona być dodawana do każdego leku z paracetamolem[66].
Paracetamol a niesteroidowe leki przeciwzapalne[edytuj | edytuj kod]
Paracetamol, w odróżnieniu od innych popularnych środków przeciwbólowych (kwas acetylosalicylowy, ibuprofen), wykazuje niewielkie działanie przeciwzapalne, w związku z czym nie jest klasyfikowany jako niesteroidowy lek przeciwzapalny (NLPZ).
Skuteczność[edytuj | edytuj kod]
Przeprowadzone badania stwierdzają różną skuteczność paracetamolu, jako leku przeciwbólowego, w porównaniu do NLPZ. Randomizowane badanie wśród dorosłych pacjentów z przewlekłymi dolegliwościami bólowymi spowodowanymi chorobą zwyrodnieniową stawów wykazało podobną skuteczność paracetamolu i ibuprofenu[67]. Jednakże inne badanie wśród dzieci z pourazowymi bólami mięśniowo-szkieletowymi, stosującymi standardowe dawki ibuprofenu (400 mg) i paracetamolu (1000 mg), wykazało większe działanie przeciwbólowe ibuprofenu[68]. Podobne wyniki osiągnięto w przypadku bólów ortodontycznych[69].
Jeśli chodzi o działanie przeciwgorączkowe u dzieci, to skuteczność paracetamolu w stosunku do ibuprofenu była identyczna[70] albo mniejsza[71][72][73].
Skutki uboczne[edytuj | edytuj kod]
W zalecanych dawkach paracetamol nie wykazuje drażniącego działania na śluzówkę żołądka, nie wpływa też w tak dużym stopniu jak niesteroidowe leki przeciwzapalne na krzepnięcie krwi oraz funkcję nerek. Jednakże niektóre badania wykazały, że paracetamol stosowany w ilości większej niż 2000 mg/dobę, może zwiększać ryzyko powikłań żołądkowo-jelitowych[74].
Stosowanie paracetamolu jest dozwolone w ciąży. Nie wpływa, jak NLPZ, na możliwość zamknięcia płodowego przewodu tętniczego. W przeciwieństwie do kwasu acetylosalicylowego jest bezpieczny dla dzieci, gdyż jego stosowanie nie powoduje wystąpienia zespołu Reye’a u dzieci z infekcją wirusową.
Podobnie jak NLPZ, a w przeciwieństwie do opioidów, nie powoduje odczucia euforii ani obniżonego nastroju. Wykazuje niskie ryzyko wystąpienia uzależnienia, tolerancji czy zespołu odstawiennego, natomiast w porównaniu z opioidami może wywoływać uszkodzenie wątroby.
Paracetamol, szczególnie w połączeniu ze słabymi opioidami, częściej niż NLPZ, może powodować bóle głowy z odbicia, chociaż ryzyko jest mniejsze niż w przypadku stosowania ergotaminy czy tryptanów, używanych w terapii migreny[75].
Preparaty dostępne w Polsce[edytuj | edytuj kod]

Preparaty proste[edytuj | edytuj kod]
| Preparat | Postacie | Firma |
|---|---|---|
| Acenol | Acenol | FSP Galena |
| Acenol forte | ||
| Apap | Apap | US Pharmacia |
| Calpol | Calpol 6 Plus | GlaxoSmithKline |
| Calpol 80 | ||
| Calpol 125 | ||
| Calpol dla niemowląt i małych dzieci | ||
| Codipar | Codipar | GlaxoSmithKline Pharmaceuticals S.A. |
| Codipar 250 | ||
| Codipar 500 | ||
| Efferalgan | Bristol-Myers Squibb Polska | |
| Gemipar | Gemipar 50 | Gemi |
| Gemipar 125 | ||
| Gemipar 500 | ||
| Panadol | Panadol | GlaxoSmithKline Consumer Healthcare |
| Panadol dla dzieci | ||
| Panadol Rapid | ||
| Panadol Extra | ||
| Paracetamol | Paracetamol | Aflofarm Fabryka Leków |
| Aflofarm Farmacja Polska | ||
| Biofarm | ||
| Farmina | ||
| Farmjug | ||
| Galena | ||
| Hasco-Lek | ||
| Herbapol Wrocław | ||
| Polfarmex | ||
| Filofarm | ||
| Polfa Łódź | ||
| Paramol | Gemi | |
| Perfalgan | Bristol-Myers Squibb Polska | |
| Tazamol | Polfa Tarchomin |
Preparaty złożone[edytuj | edytuj kod]

| Preparat | Postacie | Firma | Skład |
|---|---|---|---|
| Antidol | Antidol 15 | Lek Polska | paracetamol, fosforan kodeiny |
| Antidol 20 pro | |||
| Apap | Apap Extra | US Pharmacia | paracetamol, kofeina |
| Apap Noc | paracetamol, chlorowodorek difenhydraminy | ||
| Cefalgin | Polfa Pabianice | paracetamol, propyfenazon, kofeina | |
| Codipar | Codipar Plus | GlaxoSmithKline Pharmaceuticals S.A. | paracetamol, kofeina |
| Coldrex | Coldrex MaxGrip o smaku cytrynowym | GlaxoSmithKline Pharmaceuticals S.A. | paracetamol, kwas askorbinowy, fenylefryna |
| Coldrex saszetki o smaku cytrynowym | paracetamol, kwas askorbinowy, fenylefryna | ||
| Coldrex saszetki o smaku czarnej porzeczki | paracetamol, kwas askorbinowy, fenylefryna | ||
| Coldrex Tabletki | paracetamol, kofeina, wodzian terpinu, fenylefryna, kwas askorbinowy | ||
| Dafalgan | Dafalgan Codeine | Bristol-Myers Squibb Polska | paracetamol, kodeina |
| Efferalgan | Efferalgan Codeine | Bristol-Myers Squibb Polska | paracetamol, kodeina |
| Efferalgan Vitamin C | paracetamol, kwas askorbinowy | ||
| Excedrin | Excedrin MigraStop | Herbapol Lublin | paracetamol, kwas acetylosalicylowy, kofeina |
| Febrisan | Altana Pharma | paracetamol, kwas askorbinowy, fenylefryna | |
| Fervex | Fervex | Bristol-Myers Squibb Polska | paracetamol, kwas askorbinowy, maleinian feniraminy |
| Fervex D | |||
| Fervex Junior | |||
| Gripex | Gripex | US Pharmacia | paracetamol, chlorowodorek pseudoefedryny, bromowodorek dekstrometorfanu |
| Gripex Max | |||
| Gripex Noc | paracetamol, chlorowodorek pseudoefedryny, bromowodorek dekstrometorfanu, maleinian chlorfenaminy | ||
| Grippostad | Grippostad | Stada | |
| Grippostad C | paracetamol, kwas askorbinowy, kofeina, chlorfenamina | ||
| Grypostop | Grypostop | Omega Rex | paracetamol, chlorowodorek pseudoefedryny, dekstrometorfan |
| Grypostop Mix | paracetamol, chlorowodorek pseudoefedryny, bromowodorek dekstrometorfanu, maleinian chlorfenaminy | ||
| MaxFlu | Pliva Kraków | paracetamol, pseudoefedryna, kwas askorbinowy | |
| Metafen | Polfa Łódź | paracetamol, ibuprofen | |
| Neopiryn | Neopiryn Asa | Biofarm | paracetamol, kwas acetylosalicylowy, kofeina[76] |
| Panadol | Panadol Extra | GlaxoSmithKline Consumer Healthcare | paracetamol, kofeina |
| Panadol Femina | paracetamol, butylobromek hioscyny | ||
| Saridon | Bayer | paracetamol, propyfenazon, kofeina | |
| Solpadeine | GlaxoSmithKline Consumer Healthcare | paracetamol, kodeina, kofeina | |
| Tabcin | Tabcin Trend | Bayer | paracetamol, chlorowodorek pseudoefedryny, maleinian chlorfenaminy |
| Talvosilen | Talvosilen | Bene Arzneinmittel | paracetamol, kodeina |
| Talvosilen forte | |||
| Theraflu | Theraflu Extra Grip | Novartis Consumer Health | paracetamol, chlorowodorek fenylefryny, maleinian feniraminy |
| Theraflu Zatoki | paracetamol, chlorowodrek fenylefryny | ||
| Vegantalgin | Vegantalgin H | GlaxoSmithKline Pharmaceuticals S.A. | paracetamol, hioscyna |
| Zaldiar | Grunenthal | paracetamol, chlorowodorek tramadolu |
Wpływ na zwierzęta[edytuj | edytuj kod]
- Stosowanie paracetamolu u kotów jest zabronione[77], gdyż jest dla nich wysoce toksyczny[78]. Do zatruć, które mogą się skończyć śmiercią kota nawet po niewielkiej dawce[79], dochodzi w wyniku podawania paracetamolu zwierzęciu przez właściciela, bez uprzedniego skonsultowania się z lekarzem weterynarii. Koty nie są zdolne do metabolizowania (unieczynniania) paracetamolu, co wynika z braku enzymu transferazy glukuronylowej[77], co ogranicza możliwość sprzęgania tego związku z glutationem i przyczynia się do jego utleniania do uszkadzających DNA epoksydów[80]. Szybko dochodzi do przedawkowania (już w dawce dziennej 10 mg/kg)[77] i pojawienia się objawów zatrucia. W wyniku patologicznych zmian wywołanych stresem oksydacyjnym, na który hemoglobina kotów jest szczególnie wrażliwa[77], dochodzi w pierwszej kolejności (2–4 godzin po podaniu)[77] do wystąpienia methemoglobinemii i hemolizy[81], a dopiero później do pojawienia się objawów wynikających z uszkodzenia hepatocytów. Erytrocyty nie są w stanie transportować wystarczającej ilości tlenu, co prowadzi do niedotlenienia. W rezultacie postępującej methemoglobinemii śluzówka w pysku zmienia kolor na brązowy[77]. Inne objawy zatrucia paracetamolem u kotów obejmują wymioty, otępienie, trudności z oddychaniem, ślinienie, obrzęk głowy i łap[82], zaś w późniejszym stadium pojawia się bolesność brzucha oraz żółte zabarwienie dziąseł, oczu i skóry jako rezultat rozwijającej się żółtaczki spowodowanej uszkodzeniem wątroby[81]. Obraz kliniczny pogarsza dołączające się uszkodzenie nerek[77]. Postępowanie lecznicze, które należy zastosować bezzwłocznie, polega na podawaniu acetylocysteiny (odtrutka) i tlenu, jednak rokowanie jest zazwyczaj złe[82]. Nie zaleca się dodatkowego podawania cymetydyny (blokuje cytochrom P450)[77], natomiast zaleca się łączne podawanie acetylocysteiny i witaminy C, która zwiększa efektywność odtruwania[77].
- Paracetamol jest używanym i bezpiecznym środkiem przeciwbólowym w przypadku psów, lecz można go podawać psom tylko z zalecenia lekarza weterynarii. Preparat zawierający w składzie paracetamol i kodeinę (nazwa handlowa Pardale-V)[83] jest dopuszczony do stosowania u psów i dostępny w oparciu o receptę w Wielkiej Brytanii[84]. W przypadku psów zatrucie paracetamolem występuje, gdy dawka osiągnie około 100 do 150 mg/kg masy ciała[85], przy czym (odwrotnie niż u kotów) najpierw pojawiają się objawy wynikające z hepatotoksyczności, a dopiero w drugiej kolejności uwidaczniają się symptomy związane z postępującą methemoglobinemią[77]. Podając paracetamol psu należy liczyć się z ryzykiem wystąpienia objawów toksycznych[77]. Znane są przypadki zgonów psów po podaniu paracetamolu[78]. Paracetamol stosuje się u psów jako doustny lek przeciwbólowy. Dawkowanie wynosi 10 mg/kg masy ciała zwierzęcia, 1 do 2 razy dziennie, przy czym podawanie ogranicza się do zaledwie kilku dni[77]. Do możliwych objawów niepożądanych należą apatia i nudności. W przypadku przedawkowania (> 100 mg/kg/dobę) pojawiają się objawy hepatotoksyczne, zaś wyższe dawki (200 mg/kg/dobę) wywołują dodatkowo methemoglobinemię[77]. W każdym przypadku spożycia paracetamolu przez kota lub jego przedawkowania u psa, należy niezwłocznie udać się ze zwierzęciem do lekarza weterynarii w celu dokonania detoksykacji[86].
- Paracetamol okazał się trujący dla niektórych węży. Na wyspie Guam przeprowadzono eksperymenty stosując martwe myszy z wprowadzonym paracetamolem jako przynętę dla brązowych węży drzewnych Boiga irregularis w celu zmniejszenia populacji tych węży. Ryzyko dla innych dziko żyjących zwierząt określono jako minimalne[87].
- Paracetamolu i innych leków stosowanych u ludzi nie należy podawać ptakom i jeżom bez uprzedniego skonsultowania się z lekarzem weterynarii, gdyż może to skończyć się dla nich śmiercią[88].
Przypisy[edytuj | edytuj kod]
- ↑ a b c d e f g Acetaminophen, karta charakterystyki produktu Sigma-Aldrich, Merck, 28 marca 2021, numer katalogowy: A7085 [dostęp 2022-06-24]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Stefanidis, Dimitrios, Cho, Sayeon, Dhe-Paganon, Sirano, Jencks, William P. Structure-reactivity correlations for reactions of substituted phenolate anions with acetate and formate esters. „Journal of the American Chemical Society”. 115 (5), s. 1650–1656, 1993. DOI: 10.1021/ja00058a006.
- ↑ Nichols, Gary, Frampton, Christopher S. Physicochemical characterization of the orthorhombic polymorph of paracetamol crystallized from solution. „Journal of Pharmaceutical Sciences”. 87 (6), s. 684–693, 1998. DOI: 10.1021/js970483d.
- ↑ a b Lee, Hung Lin, Lin, Hong Yu, Lee, Tu. Large-Scale Crystallization of a Pure Metastable Polymorph by Reaction Coupling. „Organic Process Research & Development”. 18 (4), s. 539–545, 2014. DOI: 10.1021/op500003k. [Supporting Information].
- ↑ a b c d e f g h i j k l m n o p q Farmacotherapeutisch Kompas – Paracetamol. [dostęp 2016-04-09]. (niderl.).
- ↑ a b History of Tylenol. [dostęp 2012-12-17]. (ang.).
- ↑ Ernst Mutschler: Mutschler. Farmakologia i toksykologia. Podręcznik. Gerd Geisslinger, Heyo K. Kroemer, Monika Schafer-Korting, red. wyd. Andrzej Danysz. Wyd. 1. Wrocław: Elsevier Urban & Partner, 2004, s. 248. ISBN 83-89581-80-9.
- ↑ R.M. Botting, Mechanism of action of acetaminophen: is there a cyclooxygenase 3?, „Clinical Infectious Diseases”, 31 (Supplement 5), 2000, S202–210, DOI: 10.1086/317520, PMID: 11113024 [dostęp 2021-01-26] (ang.).
- ↑ Michele Curatolo, Gorazd Sveticic, Drug combinations in pain treatment, „Best Practice & Research Clinical Anaesthesiology”, 4, 16, 2002, s. 507–519, PMID: 12516888 [dostęp 2012-12-17] [zarchiwizowane z adresu 2014-10-29].
- ↑ Daly FF., Fountain JS., Murray L., Graudins A., Buckley NA. Guidelines for the management of paracetamol poisoning in Australia and New Zealand-explanation and elaboration. A consensus statement from clinical toxicologists consulting to the Australasian poisons information centres. „Med J Aust”. 188 (5), s. 296–301, 2008. PMID: 18312195.
- ↑ Khashab M., Tector AJ., Kwo PY. Epidemiology of acute liver failure. „Curr Gastroenterol Rep”. 91 (1), s. 66–73, 2007. PMID: 17335680.
- ↑ Hawkins LC., Edwards JN., Dargan PI. Impact of restricting paracetamol pack sizes on paracetamol poisoning in the United Kingdom: a review of the literature. „Drug Saf”. 6 (30), s. 465–479, 2007. PMID: 17536874.
- ↑ a b c d e f g h i Co wiemy o paracetamolu? Artykuł dr n. med. P. Grzesiowskiego i mgr J. Walorego. [dostęp 2012-12-18].
- ↑ H.N. Morse. Ueber eine neue Darstellungsmethode der Acetylamidophenole. „Berichte der deutschen chemischen Gesellschaft”. 11 (1), s. 232–233, 1878. DOI: 10.1002/cber.18780110151.
- ↑ Neil Schlager, Jayne Weisblatt, David E. Newton (red.): Chemical Compounds. Thomson Gale, 2006, s. 19–22. ISBN 978-1-4144-0150-8.
- ↑ B.B. Brodie, J. Axelrod. The fate of acetanilide in man. „J Pharmacol Exp Ther”. 94 (1), s. 29–38, 1948. PMID: 18885611.
- ↑ J.S. Thomson, L.F. Prescott. Liver damage and impaired glucose tolerance after paracetamol overdosage. „Br Med J”. 2 (5512), s. 506–507, 1966. PMID: 5913085. PMCID: PMC1943497.
- ↑ D.G. Davidson, W.N. Eastham. Acute liver necrosis following overdose of paracetamol. „Br Med J”. 2 (5512), s. 497–499, 1966. PMID: 5913083. PMCID: PMC1943529.
- ↑ JB Spooner, JG Harvey, The history and usage of paracetamol, „Journal of International Medical Research”, 4 (4 Suppl), 1976, s. 1–6, DOI: 10.1177/14732300760040S403, PMID: 799998.
- ↑ R.B. Newson, S.O. Shaheen, S. Chinn, P.G. Burney. Paracetamol sales and atopic disease in children and adults: an ecological analysis. „Eur Respir J”. 16 (5), s. 817–823, 2000. PMID: 11153577.
- ↑ Paracetamolactie in Hulst. [dostęp 2008-06-23]. [zarchiwizowane z tego adresu (23 stycznia 2009)].
- ↑ Polacy łykają miliardy w tabletkach. [dostęp 2008-06-23].
- ↑ G. Kortüm, W. Vogel, K. Andrussow: Dissociation Constants of Organic Acids in Aqueous Solution. London: Butterworth, 1961.
- ↑ Paracetamol manufacture review. [dostęp 2008-06-26].
- ↑ Direct determination of paracetamol and its metabolites in urine and serum by capillary electrophoresis with ultraviolet and mass spectrometric detection. [dostęp 2008-06-19]. [zarchiwizowane z tego adresu (2017-09-17)]. (ang.).
- ↑ a b R.S. Andrews, C.C. Bond, J. Burnett, A. Saunders i inni. Isolation and identification of paracetamol metabolites. „J Int Med Res”. 4 (4 Suppl), s. 34–39, 1976. DOI: 10.1177/14732300760040S408. PMID: 1026559.
- ↑ a b E.D. Högestätt, B.A. Jönsson, A. Ermund, D.A. Andersson i inni. Conversion of acetaminophen to the bioactive N-acylphenolamine AM404 via fatty acid amide hydrolase-dependent arachidonic acid conjugation in the nervous system. „J Biol Chem”. 280 (36), s. 31405–31412, 2005. DOI: 10.1074/jbc.M501489200. PMID: 15987694.
- ↑ Bertolini A., Ferrari A., Ottani A., Guerzoni S., Tacchi R., Leone S. Paracetamol: new vistas of an old drug. „CNS Drug Rev”. 3–4 (12), s. 250–275, 2007. DOI: 10.1111/j.1527-3458.2006.00250.x. PMID: 17227290.
- ↑ Graham GG., Scott KF. Mechanism of action of paracetamol. „Am J Ther”. 1 (12), s. 46–55, 2005. PMID: 15662292.
- ↑ Aronoff DM., Oates JA., Boutaud O. New insights into the mechanism of action of acetaminophen: Its clinical pharmacologic characteristics reflect its inhibition of the two prostaglandin H2 synthases. „Clin Pharmacol Ther”. 79. 1, s. 9–19, 2006. DOI: 10.1016/j.clpt.2005.09.009. PMID: 16413237.
- ↑ Kis B., Snipes JA., Busija DW. Acetaminophen and the cyclooxygenase-3 puzzle: sorting out facts, fictions, and uncertainties. „J Pharmacol Exp Ther”. 315. 1, s. 1–7, 2005. DOI: 10.1124/jpet.105.085431. PMID: 15879007.
- ↑ a b N.V. Chandrasekharan, H. Dai, K.L. Roos, N.K. Evanson i inni. COX-3, a cyclooxygenase-1 variant inhibited by acetaminophen and other analgesic/antipyretic drugs: cloning, structure, and expression. „Proc Natl Acad Sci U S A”. 99 (21), s. 13926–13931, 2002. DOI: 10.1073/pnas.162468699. PMID: 12242329. PMCID: PMC129799.
- ↑ R.J. Flower, J.R. Vane. Inhibition of prostaglandin synthetase in brain explains the anti-pyretic activity of paracetamol (4-acetamidophenol). „Nature”. 240 (5381), s. 410–411, 1972. DOI: 10.1038/240410a0. PMID: 4564318.
- ↑ Central Serotonin Receptor Changes: A Mechanism for Analgesic-Abuse Headaches?. [dostęp 2008-06-20].
- ↑ A. Greco, M.A. Ajmone-Cat, A. Nicolini, M.G. Sciulli i inni. Paracetamol effectively reduces prostaglandin E2 synthesis in brain macrophages by inhibiting enzymatic activity of cyclooxygenase but not phospholipase and prostaglandin E synthase. „J Neurosci Res”. 71 (6), s. 844–852, 2003. DOI: 10.1002/jnr.10543. PMID: 12605411.
- ↑ A. Ottani, S. Leone, M. Sandrini, A. Ferrari i inni. The analgesic activity of paracetamol is prevented by the blockade of cannabinoid CB1 receptors. „Eur J Pharmacol”. 531 (1–3), s. 280–281, 2006. DOI: 10.1016/j.ejphar.2005.12.015. PMID: 16438952.
- ↑ a b c d e f g h K.D. Rainsford: Aspirin and Related Drugs. CRCPress, 2004, s. ?. ISBN 978-0-7484-0885-6.
- ↑ a b Nonsteroidal Anti-inflammatory Drugs. W: William O. Foye, Thomas L. Lemke, David A. Williams: Principles of Medicinal Chemistry. Wyd. 4. Williams & Wilkins, 1995, s. 544–545. ISBN 0-683-03323-9.
- ↑ a b c d e f g h i j P. Hameleers-Snijders, M. Hogeveen, J.A. Smeitink, C. Kramers i inni. Risico van acute leverinsufficiëntie bij kinderen door chronische accidentele overdosering van paracetamol. „Ned Tijdschr Geneeskd”. 151 (16), s. 897–900, 2007. PMID: 17500339.
- ↑ T.G. Mant, J.H. Tempowski, G.N. Volans, J.C. Talbot. Adverse reactions to acetylcysteine and effects of overdose. „Br Med J (Clin Res Ed)”. 289 (6439), s. 217–219, 1984. DOI: 10.1136/bmj.289.6439.217. PMID: 6234965. PMCID: PMC1442311.
- ↑ Alsalim, W.; Fadel, M. Oral methionine compared with intravenous n-acetyl cysteine for paracetamol overdose. „Emerg. Med. J”. 20, s. 366–367, 2003.
- ↑ Grieb P. Wpływ leków na procesy wolnorodnikowe w organizmie. „Farmacja Polska”. LVII, s. 01–15.08, 2001.
- ↑ Toxic responses of the liver. W: M Treinen-Moslen: Casarett and Doull’s Toxicology. The basic science of poisons. Sixth Edition. McGraw-Hill Medical Publishing Division, 2001. ISBN 0-07-134721-6.
- ↑ G.P. Bray, C. Mowat, D.F. Muir, J.M. Tredger i inni. The effect of chronic alcohol intake on prognosis and outcome in paracetamol overdose. „Hum Exp Toxicol”. 10 (6), s. 435–438, 1991. PMID: 1687856.
- ↑ a b L. Nicod, C. Viollon, A. Regnier, A. Jacqueson i inni. Rifampicin and isoniazid increase acetaminophen and isoniazid cytotoxicity in human HepG2 hepatoma cells. „Hum Exp Toxicol”. 16 (1), s. 28–34, 1997. PMID: 9023573.
- ↑ N.A. Minton, J.A. Henry, R.J. Frankel. Fatal paracetamol poisoning in an epileptic. „Hum Toxicol”. 7 (1), s. 33–34, 1988. PMID: 3346037.
- ↑ S.M. Suchin, D.C. Wolf, Y. Lee, G. Ramaswamy i inni. Potentiation of acetaminophen hepatotoxicity by phenytoin, leading to liver transplantation. „Dig Dis Sci”. 50 (10), s. 1836–1838, 2005. DOI: 10.1007/s10620-005-2947-4. PMID: 16187183.
- ↑ N. Vuilleumier, M.F. Rossier, A. Chiappe, F. Degoumois i inni. CYP2E1 genotype and isoniazid-induced hepatotoxicity in patients treated for latent tuberculosis. „Eur J Clin Pharmacol”. 62 (6), s. 423–429, 2006. DOI: 10.1007/s00228-006-0111-5. PMID: 16770646.
- ↑ a b c Verduijn M.M., Folmer H. Wat is de maximale dagdosering van paracetamol voor langdurig gebruik bij benigne aandoeningen?. „NHG-standpunt”, s. september, 2004.
- ↑ R. Buhl, H.A. Jaffe, K.J. Holroyd, F.B. Wells i inni. Systemic glutathione deficiency in symptom-free HIV-seropositive individuals. „Lancet”. 2 (8675), s. 1294–1298, 1989. PMID: 2574255.
- ↑ a b c d Panadol Gladde Tablet. [dostęp 2012-12-18].
- ↑ I. Eneli, K. Sadri, C. Camargo, R.G. Barr. Acetaminophen and the risk of asthma: the epidemiologic and pathophysiologic evidence. „Chest”. 127 (2), s. 604–612, 2005. DOI: 10.1378/chest.127.2.604. PMID: 15706003.
- ↑ T.M. McKeever, S.A. Lewis, H.A. Smit, P. Burney i inni. The association of acetaminophen, aspirin, and ibuprofen with respiratory disease and lung function. „Am J Respir Crit Care Med”. 171 (9), s. 966–971, 2005. DOI: 10.1164/rccm.200409-1269OC. PMID: 15735054.
- ↑ R.G. Barr, C.C. Wentowski, G.C. Curhan, S.C. Somers i inni. Prospective study of acetaminophen use and newly diagnosed asthma among women. „Am J Respir Crit Care Med”. 169 (7), s. 836–841, 2004. DOI: 10.1164/rccm.200304-596OC. PMID: 14711794.
- ↑ R. Beasley, T. Clayton, J. Crane, E. von Mutius i inni. Association between paracetamol use in infancy and childhood, and risk of asthma, rhinoconjunctivitis, and eczema in children aged 6-7 years: analysis from Phase Three of the ISAAC programme. „Lancet”. 372 (9643), s. 1039–1048, 2008. DOI: 10.1016/S0140-6736(08)61445-2. PMID: 18805332.
- ↑ a b c d e f g Mateusz Kusiak, Ból to jest nasz ostatni, Tygodnik “NIE” nr 1/2008.
- ↑ C. Rebordosa, M. Kogevinas, H.T. Sørensen, J. Olsen. Pre-natal exposure to paracetamol and risk of wheezing and asthma in children: a birth cohort study. „Int J Epidemiol”. 37 (3), s. 583–590, 2008. DOI: 10.1093/ije/dyn070. PMID: 18400839.
- ↑ a b Death is not an acceptable side affect. [dostęp 2008-06-27]. [zarchiwizowane z tego adresu (22 lutego 2008)].
- ↑ a b Fluimucil Antidotum. [dostęp 2008-06-23].
- ↑ A.M. Larson, J. Polson, R.J. Fontana, T.J. Davern i inni. Acetaminophen-induced acute liver failure: results of a United States multicenter, prospective study. „Hepatology”. 42 (6), s. 1364–1372, 2005. DOI: 10.1002/hep.20948. PMID: 16317692.
- ↑ G. Pool, F. Heuvel, A.V. Ranchor, R. Sanderman: Handboek psychologische interventies bij chronisch-somatische aandoeningen. Van Gorcum, s. ?. ISBN 90-232-3844-3.
- ↑ W.M. Lee. Acute liver failure in the United States. „Semin Liver Dis”. 23 (3), s. 217–226, 2003. DOI: 10.1055/s-2003-42641. PMID: 14523675.
- ↑ Acuut leverfalen. [dostęp 2012-12-18].
- ↑ a b c d Ciszowski K., Gomółka E., Jenner B. Wpływ dawki, czasu od zażycia i stężenia ksenobiotyku na stan kliniczny i stopień uszkodzenia wątroby u pacjentów zatrutych paracetamolem. „Przegląd Lekarski”. 62 (6), s. 456–461, 2005.
- ↑ a b c d Świątkiewicz G. Problem nadużywania legalnych psychoaktywnych farmaceutyków na tle społeczno-ekonomicznej transformacji w Polsce. „Alkoholizm i Narkomania”. 18 (4), s. 73–92, 2005.
- ↑ a b c d A.L. Jones, P.C. Hayes, A.T. Proudfoot, J.A. Vale i inni. Should methionine be added to every paracetamol tablet?. „BMJ”. 315 (7103), s. 301–304, 1997. DOI: 10.1136/bmj.315.7103.301. PMID: 9274554. PMCID: PMC2127197.
- ↑ J.D. Bradley, K.D. Brandt, B.P. Katz, L.A. Kalasinski i inni. Comparison of an antiinflammatory dose of ibuprofen, an analgesic dose of ibuprofen, and acetaminophen in the treatment of patients with osteoarthritis of the knee. „N Engl J Med”. 325 (2), s. 87–91, 1991. DOI: 10.1056/NEJM199107113250203. PMID: 2052056.
- ↑ E. Clark, A.C. Plint, R. Correll, I. Gaboury i inni. A randomized, controlled trial of acetaminophen, ibuprofen, and codeine for acute pain relief in children with musculoskeletal trauma. „Pediatrics”. 119 (3), s. 460–467, 2007. DOI: 10.1542/peds.2006-1347. PMID: 17332198.
- ↑ R.L. Bradley, P.E. Ellis, P. Thomas, H. Bellis i inni. A randomized clinical trial comparing the efficacy of ibuprofen and paracetamol in the control of orthodontic pain. „Am J Orthod Dentofacial Orthop”. 132 (4), s. 511–517, 2007. DOI: 10.1016/j.ajodo.2006.12.009. PMID: 17920505.
- ↑ Autret-Leca E, Gibb IA, Goulder MA. Ibuprofen versus paracetamol in pediatric fever: objective and subjective findings from a randomized, blinded study. „Curr Med Res Opin.”. Sep;23(9), s. 2205–2211, 2007. PMID: 17686209.
- ↑ J. McIntyre, D. Hull. Comparing efficacy and tolerability of ibuprofen and paracetamol in fever. „Arch Dis Child”. 74 (2), s. 164–167, 1996. PMID: 8660083. PMCID: PMC1511501.
- ↑ D.A. Perrott, T. Piira, B. Goodenough, G.D. Champion. Efficacy and safety of acetaminophen vs ibuprofen for treating children’s pain or fever: a meta-analysis. „Arch Pediatr Adolesc Med”. 158 (6), s. 521–526, 2004. DOI: 10.1001/archpedi.158.6.521. PMID: 15184213.
- ↑ A. Van Esch, H.A. Van Steensel-Moll, E.W. Steyerberg, M. Offringa i inni. Antipyretic efficacy of ibuprofen and acetaminophen in children with febrile seizures. „Arch Pediatr Adolesc Med”. 149 (6), s. 632–637, 1995. DOI: 10.1001/archpedi.1995.02170190042007. PMID: 7767417.
- ↑ L.A. Garcia Rodríguez, S. Hernández-Díaz. The risk of upper gastrointestinal complications associated with nonsteroidal anti-inflammatory drugs, glucocorticoids, acetaminophen, and combinations of these agents. „Arthritis Res”. 3 (2), s. 98–101, 2001. DOI: 10.1186/ar146. PMID: 11178116. PMCID: PMC128885.
- ↑ R. Colás Chacartegui, R. Temprano González, C. Gómez Arruza, P. Muñoz Cacho i inni. Patrón de abuso de analgésicos en la cefalea crónica diaria: un estudio en población general. „Rev Clin Esp”. 205 (12), s. 583–587, 2005. PMID: 16527179. (hiszp.).
- ↑ Neopiryn Asa. Encyklopedia leków. [dostęp 2010-12-12]. [zarchiwizowane z tego adresu (2011-08-21)].
- ↑ a b c d e f g h i j k l m Risico’s en baten van het gebruik van paracetamol bij gezelschapsdieren, BCFI Vet [zarchiwizowane 2022-09-14] (niderl.).
- ↑ a b DAP Walcheren: Nieuwe generatie pijnstillers voor honden. [dostęp 2008-07-15]. (niderl.).
- ↑ Andrew L. Allen, The diagnosis of acetaminophen toxicosis in a cat, „Can Vet J”, 44 (6), 2003, s. 509–510, PMID: 12839249, PMCID: PMC340185.
- ↑ Karlik W. Niesteroidowe leki przeciwzapalne w postępowaniu antyhomotoksycznym. „Heel.pl”. 36.
- ↑ a b Manning A.M: Acetaminophen (Tylenol) Toxicity in Dogs. [dostęp 2008-07-16]. [zarchiwizowane z tego adresu (9 lutego 2009)]. (ang.).
- ↑ a b WHG Dierenartsen: Giftige stoffen voor huisdieren – Vergiftiging. [dostęp 2011-09-13]. (niderl.).
- ↑ Pardale-V Tablets: Presentation, UK National Office of Animal Health Compendium of Animal Medicines, 28 września 2006 [dostęp 2011-09-13].
- ↑ Pardale-V Tablets: Legal Category, UK National Office of Animal Health Compendium of Animal Medicines, 15 listopada 2005 [dostęp 2011-09-13] [zarchiwizowane z adresu 2014-03-24].
- ↑ Vergiftigingen. Dierenartsenpraktijk in de IJmond. [dostęp 2012-12-18]. [zarchiwizowane z tego adresu (2016-03-04)]. (niderl.).
- ↑ Villar D., Buck WB., Gonzalez JM. Ibuprofen, aspirin and acetaminophen toxicosis and treatment in dogs and cats. „Vet Hum Toxicol”. 40 (3), s. 156–162, 1998. PMID: 9610496.
- ↑ J.J. Johnston, P.J. Savarie, T.M. Primus, J.D. Eisemann i inni. Risk assessment of an acetaminophen baiting program for chemical control of brown tree snakes on Guam: evaluation of baits, snake residues, and potential primary and secondary hazards. „Environ Sci Technol”. 36 (17), s. 3827–3833, 2002. DOI: 10.1021/es015873n. PMID: 12322757.
- ↑ wetenswaardigheden. [dostęp 2011-09-13]. [zarchiwizowane z tego adresu (2016-12-24)]. (niderl.).
Linki zewnętrzne[edytuj | edytuj kod]
- Lista ośrodków ostrych zatruć w Polsce. resmedica.pl. [zarchiwizowane z tego adresu (2011-12-13)].
- Przemysław Skibiński: Paracetamol – wilk w owczej skórze?. [w:] Postępy Farmacji [on-line]. [dostęp 2014-11-26].

