Naczelne
| Primates | |||||
| Linnaeus, 1758[1] | |||||
| Okres istnienia: paleocen–holocen 55,8 mln lat temu–dziś | |||||
 Przedstawiciele różnych rodzin naczelnych, od góry do dołu: Daubentoniidae, Tarsiidae, Lemuridae, Lorisidae, Cebidae, Callitrichidae, Atelidae, Cercopithecidae, Hylobatidae, Hominidae | |||||
| Systematyka | |||||
| Domena | |||||
|---|---|---|---|---|---|
| Królestwo | |||||
| Typ | |||||
| Podtyp | |||||
| Gromada | |||||
| Podgromada | |||||
| Infragromada | |||||
| (bez rangi) | Boreoeutheria | ||||
| Nadrząd | |||||
| Rząd |
naczelne | ||||
| |||||
| Podrzędy[15] | |||||
| |||||
| Zasięg występowania | |||||
 Zasięg występowania naczelnych z wyjątkiem człowieka | |||||
Naczelne (Primates, z łaciny „pierwsze”) – rząd ssaków[16]. Taksonomia wyróżnia w nim dwie odrębne linie (podrzędy): Strepsirrhini i Haplorrhini[15]. Naczelne powstały z przodków żyjących na drzewach lasów tropikalnych. Wiele z nich przedstawia adaptacje do życia w tym wymagającym, trójwymiarowym środowisku. Większość z nich zachowała przynajmniej częściowo nadrzewny tryb życia.
Nie licząc zamieszkującego wszystkie kontynenty człowieka, większość naczelnych zamieszkuje zwrotnikowe lub podzwrotnikowe obszary obu Ameryk, Afryki i Azji[17]. Przedstawicieli tego rzędu cechuje duże zróżnicowanie pod względem wielkości ciała: obok gatunków o małych wymiarach, jak np. ważący jedynie 30 g Microcebus berthae należą do nich gatunki o dużych wymiarach, jak np. osiągające masę ponad dwieście kilogramów goryle Gorilla beringei graueri. Najstarsze znane skamieniałości zwierząt należących do tego rzędu pochodzą sprzed 55,8 milionów lat, i przyporządkowane są do rodzaju Teilhardina[18]. Najwcześniejszy bliski krewny naczelnych, którego szczątki są licznie reprezentowane, to późnopaleoceński Plesiadapis, żyjący około 55–58 milionów lat temu[19]. Z analiz materiału genetycznego wynika, że linia naczelnych powstała jeszcze przed granicą kreda-trzeciorzęd, około 63-74 milionów lat temu[20][21][22][23].
Rząd naczelnych tradycyjnie dzielono na dwie podgrupy: małpiatki i małpy właściwe. Małpiatkom przypisywano w większym stopniu cechy najwcześniejszych naczelnych. Zaliczano doń Lemuridae z Madagaskaru, Lorisidae i Tarsiidae. Małpy właściwe obejmowały małpy zwierzokształtne, małpy człekokształtne i człowiekowate. Obecnie taksonomowie preferują podział na dwa podrzędy Strepsirrhini, w skład których weszły dawne Prosimia oprócz Tarsiidae, oraz Haplorrhini, obejmujące Tarsiidae, jak też dawne małpy właściwe.
Małpy właściwe dzielą się znów na dwie grupy: małpy wąskonose, małpy Starego Świata zamieszkujące pierwotnie Afrykę i Azję południowo-wschodnią, oraz małpy szerokonose, małpy Nowego Świata zamieszkujące Amerykę Środkową i Południową. Przedstawiciele wąskonosych to pawiany, makakowate, gibbony i człowiekowate, zwane też wielkimi małpami. Do szerokonosych należą kapucynki, czepiakowate, oraz pazurkowce. Ludzie to jedyni współcześni przedstawiciele wąskonosych, którym udało się skolonizować rozległe tereny innych kontynentów poza Afryką i Azją, ale dowody kopalne wskazują na to, że w przeszłości wiele gatunków zamieszkiwało Europę[potrzebny przypis]. Ciągle odkrywane są nowe gatunki: w pierwszej dekadzie XXI wieku opisano 26 gatunków, w kolejnej zaś już 17.[potrzebny przypis]
Naczelne uznawane są za ssaki mało wyspecjalizowane. Niektóre z nich, jak część wielkich małp i pawiany, wiodą głównie naziemny tryb życia, jednak wszystkie gatunki cechują się przystosowaniami do wspinaczki po drzewach. Przedstawiciele naczelnych mogą przemieszczać się poprzez skakanie z drzewa na drzewo, chód na dwóch bądź czterech kończynach (w tym niektóre wspierać się mogą na knykciach), i przez brachiację).
Naczelne cechują się mózgowiami względnie większymi niż u innych zwierząt. W większym stopniu polegają też na wzroku zamiast na węchu, najważniejszym ze zmysłów u większości ssaków. Cechy te rozwinęły się w większym stopniu u małp, słabiej zaś u Lorisidae czy Lemuridae. U części naczelnych rozwinęło się widzenie barwne. Większość z nich posiada także przeciwstawny kciuk, niektóre z nich posiadają również chwytny ogon. Większość gatunków wykazuje dymorfizm płciowy, obejmujący różnice w masie ciała, wielkości kłów i ubarwieniu. Przedstawicieli naczelnych cechuje wolniejsze tempo rozwoju osobniczego niż innych ssaków o podobnych rozmiarach: później osiągają dojrzałość, jednakże żyją dłużej. Zależnie od gatunku osobniki dorosłe mogą żyć samotnie, w parach bądź w grupach, liczących zazwyczaj do setki osobników.
Terminologia[edytuj | edytuj kod]
Powiązania pomiędzy różnymi grupami naczelnych były do niedawna słabo poznane, wobec czego powszechnie używane terminy bywają mylące. Przykładowo w języku angielskim nazwy "ape" ("małpa człekokształtna") używano jako synonimu "monkey" ("małpa zwierzokształtna") bądź do wszystkich nieposiadających ogona, względnie przypominających człowieka naczelnych[24].
Sir Wilfrid Le Gros Clark należał do prymatologów, którzy rozwinęli pomysł trendów w ewolucji naczelnych i metodologię układania żyjących ich przedstawicieli w jakoby wznoszące się aż do człowieka serie[25]. Powszechnie używane nazwy określające grupy w obrębie naczelnych, jak „małpiatki”, „małpy”, angielskie "lesser ape" i „wielkie małpy” ("great ape") odzwierciadlają ten pogląd. Zgodnie ze współczesnym rozumieniem historii ewolucyjnej naczelnych część z tych grup to taksony parafiletyczne – nie obejmują one wszystkich potomków swego ostatniego wspólnego przodka[26].
Odmiennie od pomysłu Clarka współczesne klasyfikacje wyróżniają (i nazywają) jedynie te grupy, które są monofiletyczne, a więc obejmują wszystkich potomków swego ostatniego wspólnego przodka[27].
Poniższy diagram przedstawia jedną z możliwych klasyfikacji współcześnie żyjących naczelnych[28][29]. Dawne, tradycyjne grupy zaznaczono kolorami: małpiatki, małpy zwierzokształtne, małpy człekokształtne: niezaliczane do wielkich małp i zaliczane do wielkich małp, człowieka.
| Primates |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Wszystkie grupy o podanych nazwach naukowych są monofiletyczne (a więc stanowią klady), a klasyfikacja kladystyczna odzwierciedla historię ewolucyjną danej grupy. Kolorem zaznaczono nazwy tradycyjne, część z nich oznacza grupy parafiletyczne:
- „małpiatki” obejmują dwie grupy monofiletyczne: podrząd Strepsirrhini, czyli Lemuroidea, Lorisoidea i tym podobne, a także Tarsiiformes z podrzędu Haplorrhini. Parafiletyzm grupy wynika z niewłączenia doń Simiiformes, pochodzących również od ostatniego wspólnego przodka tych, ale też wszystkich naczelnych.
- „małpy” zawierają w sobie dwie monofiletyczne grupy, określane mianem małp Nowego Świata i małp Starego Świata. Parafiletyzm wynika z wykluczenia nadrodziny Hominoidea, pochodzącej także od ostatniego wspólnego przodka Simiiformes.
- „małpy człekokształtne” w ogólności, w szczególności zaś „wielkie małpy” – parafiletyzm obu grup wynika z wykluczenia z nich człowieka.
W związku z powyższym zakresy nazw z dwu ich zestawów nie zgadzają się ze sobą, z czego wynikają problemy związane również z nazwami zwyczajowymi, zazwyczaj tradycyjnymi. Przykład stanowi nadrodzina Hominoidea. W powszechnym rozumieniu składa się ona z małp człekokształtnych i ludzi, nie ma zwyczajowej nazwy określającej taką grupę. W języku angielskim poradzono sobie, tworząc taką nazwę: "hominoids". Inna możliwość wyjścia z problemu to poszerzenie znaczenia jednej z nazw tradycyjnych. Przykładowo w swej książce z 2005 Benton, paleontolog kręgowców, określa mianem "apes" („małpy człekokształtne”, Hominoidea) gibbony, orangutany, goryle, szympansy i ludzi[30]; a więc Benton używa słowa "apes" w znaczeniu "hominoids", Hominoidea. W takim jednak przypadku grupa poprzednio nazywana "apes" musi być teraz określana "non-human apes" (co oznacza „małpy człekokształtne inne niż człowiek”.
Do roku 2005 nie było jeszcze konsensusu, który sposób klasyfikacji ma obowiązywać: czy zaakceptować tradycyjne, zwyczajowe, ale określające parafiletyczne grupy nazwy, czy też używać wyłącznie nazw grup monofiletycznych, czy też może używać nowych nazw zwyczajowych, czy też zaadaptować stare nazwy. Wszystkie rozwiązania można znaleźć w pracach biologów, niekiedy nawet różne rozwiązania obserwuje się w pracach tego samego autora, a nawet w tej samej pracy. Wspomniany Benton definiuje wpierw „małpy człekokształtne” ("apes"), włączając w nie człowieka, po czym powtarza "ape-like" w znaczeniu "like an ape rather than a human" („bardziej podobny do małp człekokształtnych niż do człowieka”)[31].
Klasyfikacja współczesnych naczelnych[edytuj | edytuj kod]







Rząd naczelnych ustanowił Karol Linneusz w 1758 w 10. wydaniu Systema Naturae[32], umieszczając w nim rodzaje Homo (ludzi), Simia (małpy), Lemur (małpiatki) oraz Vespertilio (nietoperze). W pierwszym wydaniu tej książki (1735) używał miana Anthropomorpha dla Homo, Simia i Bradypus (leniwce)[33]. W 1839 Henri Marie Ducrotay de Blainville, idąc za przykładem Linneusza i naśladując jego nazewnictwo, utworzył rzędy Secundates (włączając doń nietoperze, owadożerne i drapieżne), Tertiates (zawierające podrząd Glires) i Quaternates (gdzie znalazły się Gravigrada, Pachydermata i przeżuwacze)[34]. Obecnie taksony te nie są akceptowane.
Nim Anderson i Jones wprowadzili klasyfikację Strepsirrhini i Haplorhini w 1984[35], za czym poszła praca McKenny i Bella z 1997 Classification of Mammals: Above the species level[36], naczelne dzielono na dwie nadrodziny: Prosimii i Anthropoidea[37]. Prosimii obejmowały małpiatki (jako Strepsirrhini) oraz wyrakowate. Termin Anthropoidea obejmował wszystkie małpy.
W obrębie naczelnych wyróżnia się następujące rodziny, zgrupowane za jedną z możliwych klasyfikacji[38][39][40][41][15][28][42][43] (istnieją również inne sposoby klasyfikacji, na przykład podział współczesnych Strepsirrhini na dwa infrarzędy: Lemuriformes i Lorisiformes[44]).
- Rząd: Primates Linnaeus, 1758 – naczelne
- Podrząd: Strepsirrhini É. Geoffroy Saint-Hilaire, 1812 – lemurowe
- Infrarząd: Lemuriformes J.E. Gray, 1821 – lemurokształtne
- Nadrodzina: Cheirogaleoidea J.E. Gray, 1873 – lemurkowce
- Rodzina: Cheirogaleidae J.E. Gray, 1873 – lemurkowate
- Nadrodzina: Lemuroidea J.E. Gray, 1821 – lemurowce
- Rodzina: Lepilemuridae J.E. Gray, 1870 – lepilemurowate
- Rodzina: †Megaladapidae Major, 1893
- Rodzina: Lemuridae J.E. Gray, 1821 – lemurowate
- Rodzina: †Archaeolemuridae Major, 1896
- Rodzina: †Palaeopropithecidae Tattersall, 1973
- Rodzina: Indriidae Burnett, 1828 – indrisowate
- Nadrodzina: Cheirogaleoidea J.E. Gray, 1873 – lemurkowce
- Infrarząd: Chiromyiformes Anthony & Coupin, 1931 – palczakokształtne
- Rodzina: Daubentoniidae J.E. Gray, 1863 – palczakowate
- Infrarząd: Lorisiformes Gregory, 1915 – lorisokształtne
- Rodzina: Galagidae J.E. Gray, 1825 – galagowate
- Rodzina: Lorisidae J.E. Gray, 1821 – lorisowate
- Infrarząd: Lemuriformes J.E. Gray, 1821 – lemurokształtne
- Podrząd: Haplorrhini Pocock, 1918 – wyższe naczelne
- Infrarząd: Tarsiiformes Gregory, 1915 – wyrakokształtne
- Rodzina: Tarsiidae J.E. Gray, 1825 – wyrakowate
- Infrarząd: Simiiformes Haeckel, 1866 – małpokształtne
- Parvordo: Platyrrhini É. Geoffroy Saint-Hilaire, 1812 – małpy szerokonose
- Rodzina: Callitrichidae J.E. Gray, 1821 – pazurkowcowate
- Rodzina: Aotidae Elliot, 1913 – ponocnicowate
- Rodzina: Cebidae Bonaparte, 1831 – płaksowate
- Rodzina: Pitheciidae Mivart, 1865 – sakowate
- Rodzina: Atelidae J.E. Gray, 1825 – czepiakowate
- Parvordo: Catarrhini É. Geoffroy Saint-Hilaire, 1812 – małpy wąskonose
- Nadrodzina: Cercopithecoidea J.E. Gray, 1821 – koczkodanowce
- Rodzina: Cercopithecidae J.E. Gray, 1821 – koczkodanowate
- Nadrodzina: Hominoidea J.E. Gray, 1825 – człekokształtne
- Rodzina: Hylobatidae J.E. Gray, 1870 – gibbonowate
- Rodzina: Hominidae J.E. Gray, 1825 – człowiekowate
- Nadrodzina: Cercopithecoidea J.E. Gray, 1821 – koczkodanowce
- Parvordo: Platyrrhini É. Geoffroy Saint-Hilaire, 1812 – małpy szerokonose
- Infrarząd: Tarsiiformes Gregory, 1915 – wyrakokształtne
- Podrząd: Strepsirrhini É. Geoffroy Saint-Hilaire, 1812 – lemurowe
Choć monofilia Lemuroidea i Lorisoidea jest szeroko akceptowana, nazwy kladów to nie dotyczy. Użyta tutaj nazwa pochodzi z popularnej taksonomii wyróżniającej klad cechujący się grzebieniem zębowym jako jeden infrarząd, a wymarłe, nieposiadające grzebienia zębowego Adapiformes w inny, obie włączając w podrząd[45][46]. Jednak inna popularna taksonomia, alternatywna względem tamtej, umieszcza Lorisidae w ich własnym infrarzędzie Lorisiformes[44].
Inną klasyfikację proponuje Polskie nazewnictwo ssaków świata[41].
- Rząd: naczelne (Primates)
- Podrząd: małpiatki (Prosimii) / podrząd lemurowe (Strepsirrhini)
- Infrarząd: lemurokształtne (Lemuriformes)
- Nadrodzina: lemurkowce (Cheirogaleoidea)
- Rodzina: lemurkowate (Cheirogaleidae)
- Rodzaje: lemurak (Allocebus), lemurek (Cheirogaleus), mikrus (Mirza), mikrusek (Microcebus), widłogłówka (Phaner)
- Rodzina: lemurkowate (Cheirogaleidae)
- Nadrodzina: lemurowce (Lemuroidea)
- Rodzina: indrisowate (Indriidae)
- Rodzina: lemurowate (Lemuridae)
- Rodzina: lepilemurowate (Lepilemuridae)
- Rodzaje: lepilemur (Lepilemur)
- Nadrodzina: lemurkowce (Cheirogaleoidea)
- Infrarząd: lorisokształtne (Lorisiformes)
- Rodzina: galagowate (Galagidae)
- Rodzina: lorisowate (Lorisidae)
- Rodzaje: angwantibo (Arctocebus), kukang (Nycticebus), lori (Loris), nibypotto (Pseudopotto), potto (Perodicticus)
- Infrarząd: palczakokształtne (Chiromyiformes)
- Rodzina: palczakowate (Daubentoniidae)
- Rodzaje: palczak (Daubentonia)
- Rodzina: palczakowate (Daubentoniidae)
- Infrarząd: lemurokształtne (Lemuriformes)
- Podrząd: wyższe naczelne (Haplorrhini)
- Infrarząd: wyrakokształtne (Tarsiiformes)
- Rodzina: wyrakowate (Tarsiidae)
- Rodzaje: wyrak (Tarsius)
- Rodzina: wyrakowate (Tarsiidae)
- Infrarząd: wyrakokształtne (Tarsiiformes)
- Podrząd: małpokształtne (Simiiformes)
- Infrarząd: małpy szerokonose (Platyrrhini)
- Rodzina: czepiakowate (Atelidae)
- Rodzina: płaksowate (Cebidae)
- Rodzina: ponocnicowate (Aotidae)
- Rodzaje: ponocnica (Aotus)
- Rodzina: sakowate (Pitheciidae)
- Infrarząd: małpy wąskonose (Catarrhini)
- Nadrodzina: koczkodanowce (Cercopithecoidea)
- Rodzina: koczkodanowate (Cercopithecidae)
- Podrodzina: gerezy (Colobinae)
- Podrodzina: koczkodany (Cercopithecinae)
- Rodzina: koczkodanowate (Cercopithecidae)
- Nadrodzina: człekokształtne (Hominoidea)
- Rodzina: gibbonowate (Hylobatidae)
- Rodzina: człowiekowate, małpy człekokształtne (Hominidae)
- Nadrodzina: koczkodanowce (Cercopithecoidea)
- Infrarząd: małpy szerokonose (Platyrrhini)
- Podrząd: małpiatki (Prosimii) / podrząd lemurowe (Strepsirrhini)
Ewolucja[edytuj | edytuj kod]
| Euarchontoglires |
| ||||||||||||||||||||||||||||||
Rząd naczelnych (Primates) stanowi część kladu Euarchontoglires, zagnieżdżonego z kolei w kladzie ssaków wyższych (Eutheria) gromady ssaków. Niedawne badania genetyki molekularnej naczelnych, skóroskrzydłych i wiewióreczników wykazały, że dwa gatunki skóroskrzydłych są bliżej spokrewnione z naczelnymi, niż z wiewiórecznikami[47], mimo że tupaje uznawano niegdyś za naczelne[48]. Te trzy rzędy tworzą razem klad euarchontów (Euarchonta). Wraz z kladem siekaczowców (Glires, obejmującym gryzonie plus zajęczaki) tworzy klad Euarchontoglires. Rangę nadrzędu nadaje się różnie, i Euarchonta, i Euarchontoglires. Niektórzy naukowcy uznają skóroskrzydłe (Dermoptera) za podrząd naczelnych i wyróżniają podrząd Euprimates na określenie „właściwych” naczelnych[49].
Ewolucja[edytuj | edytuj kod]
Linia naczelnych oddzieliła się przynajmniej 65 milionów lat temu[50], choć najstarsze znane ze skamielin naczelne pochodzą z późnego paleocenu z Afryki (Altiatlasius)[51] lub z paleoceńsko-eoceńskiej wymiany pomiędzy kontynentami północnymi, około 55 milionów lat temu (Cantius, Donrussellia, Altanius i Teilhardina)[52]. Z badań genetycznych wynika, że przodkowie naczelnych oddzielili się od pozostałych ssaków w środkowej części kredy, ok. 85 mln lat temu[53][54][55].
W ujęciu kladystycznym naczelne są monofiletyczne. Uważa się ogólnie, że podrząd Strepsirrhini odłączył się od linii prymitywnych naczelnych około 63 milionów lat temu[56], choć istnieją też dane wskazujące na wcześniejsze daty[57]. Siedem rodzin Strepsirrhini obejmuje 5 spokrewnionych ze sobą rodzin Lemuroidea oraz dwie rodziny: lorisowate i galagowate[15][42]. Starsze schematy klasyfikacyjne włączają lepilemurowate do lemurowatych i galagowate do lorisowatych, proponując podział na 4+1 rodzin zamiast dzisiejszego 5+2[15]. W eocenie większość kontynentów północnych zdominowały dwie grupy: Adapiformes i Omomyidae[58][59]. Te pierwsze uważa się za Strepsirrhini, jednakże nie miały one grzebienia zębowego jak współczesne Lemuroidea. Niedawne analizy pokazały, że należy do nich Darwinius masillae[60]. Druga grupa była blisko spokrewniona z wyrakami i małpami. Jednakże powiązania tych dwóch grup ze współczesnymi naczelnymi pozostają niejasne. Omomyidae zniknęły około 30 milionów lat temu[59], natomiast Adapiformes – 10 milionów lat temu[61].

Zgodnie z badaniami genetycznymi madagaskarskie Lemuroidea oddzieliły się od lorisowatych szacunkowo 75 milionów lat temu[57]. Badania te, jak też dowody chromosomalne i molekularne pokazują, że grupy te są ze sobą bliżej spokrewnione niż z innymi Strepsirrhini[57][62]. Jednakże Madagaskar oddzielił się od Afryki 160 milionów lat temu, a od Indii 90 milionów lat temu[63]. Te fakty biorąc pod uwagę, populacja założycielska Lemuroidea złożona z kilku osobników dotarła na Madagaskar z Afryki poprzez pojedynczy rejs na tratwie, który miał miejsce w okresie od 80 mln a 50 mln lat temu[57][62][63]. Sprawdzono też inne możliwości kolonizacji, jak wielokrotna kolonizacja z Afryki i Indii, lecz żadnej z nich nie wspierają dowody genetyczne ani molekularne[58].

Do niedawna trudno było umiejscowić wśród Strepsirrhini palczaka madagaskarskiego[15]. Zaproponowano różne wyjścia. Jego rodzinę palczakowatych umieszczano wśród Lemuriformes, co oznaczałoby, że jego przodkowie oddzielili się od linii Lemuroidea już po podziale na Lemuroidea i Lorisoidea, bądź jako grupę siostrzaną wszystkich innych Strepsirrhini. W 2008 potwierdzono najbliższe pokrewieństwo palczakowatych z innymi Lemuroidea Madagaskaru; prawdopodobnie pochodzą one od tej samej populacji, która niegdyś skolonizowała wyspę[57].
Podrząd Haplorrhini tworzą dwa siostrzane klady[15]. Wyrakowate – monotypowa rodzina w infrarzędzie Tarsiiformes – reprezentuje najbardziej pierwotną ich grupę, powstałą około 58 mln lat temu[64][65]. Najwcześniejszy znany szkielet przedstawiciela Haplorrhini należy do żyjącego przed 55 milionami lat przypominającego wyraka Archicebus a znaleziono go w środkowych Chinach[66], co wspiera podejrzewane wcześniej azjatyckie pochodzenie grupy[67]. Infrarząd Simiiformes, obejmujący małpy, powstał 40 milionów lat temu[59] możliwe, że także w Azji. Jeśli tak było, to niedługo później nastąpiła ich dyspersja oceaniczna poprzez Ocean Tetydy do Afryki[68]. Wyróżnia się 2 klady Simia w randze parworzędów: małpy wąskonose (Catarrhini), które rozwijały się w Afryce i składają się z makakowatych (małp Starego Świata), ludzi i małp człekokształtnych, oraz małpy szerokonose (Platyrrhini), które rozwijały się w Ameryce Południowej i do których należą małpy Nowego Świata[15]. Trzeci klad, obejmujący rozwijające się w Azji Eosimiidae, zniknął przed milionami lat[69].
Tak jak jest w przypadku Lemuroidea, małpy Nowego Świata mają niejasne pochodzenie. Badania molekularne sekwencji DNA jądrowego przyniosły różniące się daty podziału na Platyrrhini i Catarrhini, pomiędzy 33 i 70 milionami lat temu[70]. Natomiast badania 7 genów DNA mitochondrialnego przeprowadzone przez zespół Chatterjee określiły ten czas na 43 miliony temu lat[19].
Kolonizację Ameryki Południowej (kontynentu wyspowego od kredy późnej do wytworzenia się pomostu lądowego z Ameryką Północną w pliocenie) przez naczelnych porównuje się do kolonizacji tego kontynentu przez gryzonie Caviomorpha. Zespół Poux na podstawie analizy Bayesa sekwencji 3 genów jądrowych oszacował czas dotarcia małp na ten kontynent na pomiędzy 37,0 ± 3,0 miliony lat a 16,8 ± 1 miliona lat. Ta pierwsza wartość wyznacza czas oddzielenia się linii małp szerokonosych, druga natomiast – ich radiacji[71]. Pierwsze skamieliny małp południowoamerykańskich pochodzą z oligocenu, czyli sprzed 35-35,6 milionów lat (Branisella boliviana). Jedna z hipotez podaje, że małpy zasiedliły Amerykę Południową tak jak gryzonie, w późnym eocenie poprzez dyspersję z Ameryki Północnej. Nie ma na to jednak dowodów[72]. Obecnie uważa się raczej, że zwierzęta te najprawdopodobniej dostały się na kontynent południowoamerykański przez Ocean Atlantycki pod koniec eocenu bądź na początku oligocenu[71].
Badacze sugerują, że niewielkie (jednokilogramowe) naczelne mogły przetrwać do 13 dni na tratwie pozbawionej pokarmu[73].

Małpy zwierzokształtne rozprzestrzeniły się z Afryki na Europę i Azję, rozpoczynając dyspersję w epoce mioceńskiej[74]. Niedługo później Lorisoidea i wyraki podążyły tą samą drogą. Pierwsze skamieniałości Homininae odkryto w północnej Afryce. Datuje się je na 5–8 milionów lat[59]. Małpy Starego Świata zniknęły w Europie około 1,8 miliona lat temu[75]. Obecnie poza człowiekiem Europę zamieszkuje tylko makak berberyjski, introdukowany na Gibraltarze[76]. Badania molekularne i skamieniałości ogólnie pokazały, że ludzie współcześni powstali w Afryce 100 000–200 000 lat temu[77].
Choć naczelne w porównaniu z innymi grupami zwierząt przebadano dobrze, niedawno odkryto kilka nowych gatunków, a testy genetyczne ujawniły wcześniej nierozpoznawane gatunki wśród znanych już populacji. Primate Taxonomy w 2001 wymieniała około 350 gatunków[29]; jej autor, Colin Groves, podwyższył tę liczbę do 376 w 3. wydaniu Mammal Species of the World (MSW3)[15]. Od kompilacji taksonomii w 2003 w MSW3 zwiększono liczbę gatunków do 424, podgatunków zaś do 658[43].
Mieszańce[edytuj | edytuj kod]
Mieszańce naczelnych zazwyczaj powstają w niewoli[78], ale odnotowywano też takie przypadki na wolności[79][80]. Krzyżowanie zdarza się, gdy zasięg występowania dwóch gatunków zachodzi na siebie, tworząc strefy hybrydyzacji. Krzyżówki mogą też być tworzone przez ludzi trzymających te zwierzęta w zoo bądź z powodu presji środowiska, np. drapieżnictwa[79]. Hybrydyzacja międzyrodzajowa, a więc krzyżowanie się osobników należących do różnych rodzajów, została zaobserwowana na wolności. Choć należą do rodzajów, których linie rozdzieliły się przed milionami lat, dżelada i pawian płaszczowy ciągle rozmnażają się ze sobą[81].
Anatomia, fizjologia i morfologia[edytuj | edytuj kod]
Naczelne cechują się skierowanymi do przodu oczyma ulokowanymi na przedzie czaszki. Widzenie obuoczne pozwala im na dokładną ocenę odległości, ważną podczas brachiacji, wykorzystywanej też przez przodków wszystkich człowiekowatych[82]. Wał kostny sklepienia oczodołu wzmacnia słabe kości twarzy, poddane naprężeniom podczas żucia. Lemurowe posiadają kostny wał zaoczodołowy chroniący oczy. Dla odmiany wyższe naczelne rozwinęły w trakcie ewolucji oczodoły w pełni zamknięte[83].

Szkielet naczelnych cechuje się dużą czaszką, szczególnie dobrze rozwiniętą u małpokształtnych. Czaszka ochrania duży względem wielkości ciała mózg, charakterystyczny dla tej grupy[82]. Pojemność czaszki u człowieka jest trzykrotnie większa niż największa u pozostałych naczelnych, co odzwierciedla wielkość mózgu[84]. U człowieka średnia pojemność czaszki wynosi 1,201 cm³, u goryla 469 cm³, u szympansa 400 cm³, u orangutana 397 cm³[84].
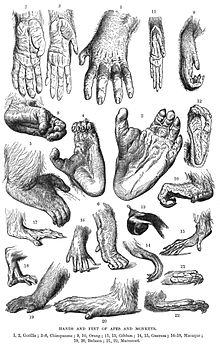
Naczelne mają ogólnie 5 palców na każdej z kończyn, a ich palce kończą się keratynowymi paznokciami. Wewnętrzna strona dłoni i stóp ma czułe opuszki palców na paliczkach dystalnych. Większość przedstawicieli dysponuje przeciwstawnym kciukiem, stanowiącym charakterystyczną cechę naczelnych, występującą jednak także poza tym rzędem, przykładowo u dydelfokształtnych[82]. Kciuki pozwalają pewnym gatunkom na wykorzystywanie narzędzi. Połączenie przeciwstawnego kciuka, krótkich paznokci zamiast pazurów i długich, zginających się do wnętrza dłoni palców stanowi pozostałość przystosowania do chwytania gałęzi przez przodków, pozwoliła ona pewnym naczelnym na rozwinięcie brachiacji, która stała się dlań ważnym środkiem lokomocji. Małpiatki mają paznokcie przypominające pazury na drugim palcu każdej stopy. Wykorzystują go do prowadzenia toalety[82].

Obojczyk naczelnych wchodzi w skład obręczy barkowej jako jej ważny element. Pozwala to na znaczną ruchomość w stawie barkowym[85]. Małpy człekokształtne dysponują bardziej ruchomym stawem ramiennym i ręką z powodu grzbietowego położenia łopatki, szerokiej klatki piersiowej, bardziej spłaszczonej w kierunku strzałkowym, i krótszemu, mniej ruchomym kręgosłupowi w porównaniu z małpami Starego Świata, o niższych kręgach znacznie zredukowanych, co u niektórych gatunków doprowadziło do utraty ogona. Koczkodanowce w przeciwieństwie do nich w większości posiadają ogony. Czepiakowate, w tym wyjec, czepiak, muriki i wełniak, oraz kapucynki mają chwytny ogon[86][87]. Zwykle samce cechuje zwisające prącie i jądra w mosznie[88][89].
Trend ewolucyjny naczelnych prowadził w kierunku redukcji pyska[85]. Koczkodanowce odróżnia się od małp Nowego Świata po budowie nosa, od małp człekokształtnych zaś po uzębieniu[90]. U małp szerokonosych nozdrza otwierają się ku bokom, u koczkodanowców zaś do dołu[90]. Wzór zębowy naczelnych wykazuje znaczne zróżnicowanie. Niektóre utraciły większość siekaczy, a wszystkie – przynajmniej 1 dolny siekacz[90]. U większości lemurowych dolne siekacze i kły tworzą grzebień zębowy, wykorzystywany do toalety i czasami podczas żerowania[90][89], a pierwszy dolny przedtrzonowiec przybiera kształt kła[89]. Koczkodanowce mają 8 przedtrzonowców, małpy szerokonose zaś 12[90]. Wśród małp Starego Świata człekokształtne i koczkodanowce różnią się od siebie liczbą guzków na zębach trzonowych: u człekokształtnych występuje zazwyczaj 5 guzków, u koczkodanowców 4[90], aczkolwiek u ludzi może ich być po 4 lub 5[91].


Główny trend ewolucyjny naczelnych obejmował rozwój mózgu, zwłaszcza zaś kory nowej zaliczanej do kory mózgu, zaangażowanej w percepcję zmysłową, nadzorowanie ruchów, myślenie przestrzenne, świadomość, a u ludzi także język[17]. Podczas gdy inne ssaki polegają w znacznym stopniu na węchu, nadrzewne życie naczelnych doprowadziło do tego, że wykorzystują głównie dotyk i wzrok[17]. Badania Gilada i współpracowników dotyczące mniejszej liczby genów związanych z odczuwaniem zapachów u naczelnych ujawniły, że pogorszenie węchu w tej grupie zwierząt postępowało wraz z rozwojem widzenia trójbarwnego. Szczególnie dużo genów kodujących receptory węchowe przekształciło się w pseudogeny u człowieka rozumnego – ponad połowa[92], a wedle starszych danych 63% z ponad 900 genów[93]. U innych małp człekokształtnych swoją funkcję straciło ponad 30% genów receptorów węchowych, dla koczkodanowców odsetek ten osiąga również około 30%. Znacznie mniej pseudogenów receptorów węchowych (kilkanaście procent) mają małpy Nowego Świata, jak też małpiatki (lemuria manguścia). Wyjątek stanowi wyjec z wynikiem ponad 30% (badanym gatunkiem był wyjec czarny) – cechujący się w pełni rozwiniętym widzeniem trójbarwnym[92].
Ewolucja widzenia barwnego u naczelnych jest wyjątkowa wśród łożyskowców. Podczas gdy zaliczani do wczesnych kręgowców przodkowie naczelnych widzieli w trzech kolorach, prowadzące nocne tryb życia ciepłokrwiste ssaki ery mezozoicznej straciły jeden z trzech rodzajów czopków siatkówki. Ryby, gady i ptaki widzą więc trójchromatycznie bądź tetrachromatycznie, podczas gdy wszystkie ssaki z wyjątkiem naczelnych właśnie i torbaczy[94] widzą dichromatycznie bądź nawet monochromatycznie, co oznacza całkowitą ślepotę barwną[89]. Nocne naczelne, jak ponocnicowate czy galagowate, odróżniają jedynie odcienie szarości. Catarrhini widzą zazwyczaj trójchromatycznie dzięki duplikacji genu czerwono-zielonej opsyny, do której doszło u ich przodka przed 30-40 milionami lat[89][95]. Natomiast wśród Platyrrhini trójchromatyzm nie występuje u wszystkich ich przedstawicieli[96]. W szczególności samice muszą być heterozygotami dwóch alleli genu opsyny, czerwonego i zielonego, zajmujących ten sam locus chromosomu X. Mogą więc widzieć w dwóch lub trzech kolorach. Natomiast samce mogą być jedynie dichromatyczne[89]. Pełne widzenie barwne występuje tylko u wyjców i rozwinęło się niezależnie od widzenia barwnego małp Starego świata[92]. Widzenie barwne u Strepsirrhini nie jest tak dobrze poznane. Jednak badania wskazują u nich na zakres widzianych barw podobny do spotykanego u Platyrrhini[89].
Jak Catarrhini, należące do szerokonosych wyjce wykazują zazwyczaj widzenie trójbarwne, które umożliwiła niedawna w sensie ewolucyjnym duplikacja genu[97]. Wyjce należą do najbardziej wyspecjalizowanych zwierząt liściożernych wśród małp Nowego Świata. Owoce nie stanowią głównego składnika ich jadłospisu[98]. Rodzaj liści, które preferują (młode, odżywcze, łatwostrawne), rozpoznawany jest jedynie dzięki barwom czerwonej i zielonej. Badania terenowe preferencji pokarmowych wyjców sugerują, że całkowity trichromatyzm utrwalił się dzięki selekcji środowiskowej[96].
Dymorfizm płciowy[edytuj | edytuj kod]

Małpokształtne często wykazują dymorfizm płciowy, aczkolwiek u małp Starego Świata, w tym małp człekokształtnych, jest on lepiej wyrażony niż u szerokonosych. U naczelnych samce i samice zazwyczaj różnią się masą ciała[99][100] i wielkością kłów[101][102], jak też barwą sierści i skóry[103] czy cechami twarzy, jak większy prognatyzm czy węższa i głębsza szczęka u samców[104].
Dymorfizm można powiązać z różnymi czynnikami, jak system rozrodu[105], wielkość[105], habitat i pożywienie[106].
Analizy porównawcze przyczyniły się do kompletniejszego zrozumienia powiązań pomiędzy doborem płciowym, doborem naturalnym i systemem rozrodu u naczelnych. Wykazano, że dymorfizm płciowy wynika ze zmian ewolucyjnych dotyczących zarówno cech samców, jak i samic[107]. Pewne dowody kopalne wskazują na ewolucję równoległą dymorfizmu, a pewne wymarłe człowiekowate prawdopodobnie rozwinęły dymorfizm w stopniu większym niż jakikolwiek współczesny naczelny[107].
Poruszanie się[edytuj | edytuj kod]

Przedstawiciele naczelnych mogą przemieszczać się na różne sposoby: poprzez brachiację, wspinanie się po drzewach, na dwóch nogach, skokami, na czterech kończynach na ziemi i na drzewach, chód z podpieraniem się knykciach bądź przez kombinację tych sposobów. Pewne małpiatki poruszają się głównie za pomocą wspinaczki i skoków. Wymienia się tu wiele galagowatych, wszystkie indrisowate, lepilemurowate, a ponadto wszystkie wyrakowate[108]. Inne małpiatki poruszają się po drzewach na czworakach i wspinają się na nie. Niektóre naczelne poruszają się na czterech kończynach po ziemi, inne przemieszczają się dzięki skokom. Większość małp porusza się na czworakach po drzewach i po ziemi, jak też się wspina. Gibbonowate, muriki i czepiak stosują brachiację[75], gibbonowate czasami przemieszczają się wyjątkowo akrobatycznie. Wełniak także czasami stosuje brachiację[98]. Orangutany wykorzystują podobny sposób lokomocji, wspinając się za pomocą wszystkich czterech kończyn, by przenosić swe ciężkie ciało wśród drzew[75]. Szympansy i goryle chodzą na knykciach[75], a na krótkich dystansach potrafią też chodzić na dwóch kończynach. Choć liczne gatunki, jak Australopithecina czy wczesne Homo, wykształciły lokomocję w pełni dwunożną, obecnie cecha ta wśród naczelnych przysługuje jedynie człowiekowi rozumnemu[109].
Zachowanie[edytuj | edytuj kod]
Systemy społeczne[edytuj | edytuj kod]
Naczelne należą do najbardziej społecznych ze zwierząt. Tworzą pary, grupy rodzinne, haremy z jednym samcem oraz stada złożone z wielu samców i samic[110]. Richard Wrangham stwierdził, że systemy społeczne innych niż człowiek naczelnych najlepiej sklasyfikować na podstawie wymiany samic pomiędzy grupami[111]. Idąc dalej, zaproponował 4 kategorie:
- Female transfer systems, system wymiany samic – samice odchodzą z grupy, w której przyszły na świat. W związku z tym samice tworzące 1 grupę nie są ze sobą blisko spokrewnione. Natomiast samce pozostają w swej rodzimej grupie i ich bliskie pokrewieństwo ze sobą może wywiera wpływ na ich zachowania społeczne. Tworzą się niewielkie grupy. Taka organizacja społeczna obserwowana jest u szympansów, u których samce, typowo spokrewnione ze sobą, współpracują ze sobą w obronie terytorium grupy. Wśród małp Nowego Świata czepiak i muriki również wykorzystują ten system[112].

- Male transfer systems, system wymiany samców – samice pozostają w swej rodzinnej grupie, natomiast samce migrują w młodym wieku. Do tej kategorii należą systemy poligeniczne i o wielu samcach. Liczebność grupy jest zazwyczaj większa. System taki występuje u lemura katta, kapucynek i pazurkowców[75].
- monogamia – występuje związek pomiędzy samcem a samicą, czasami z towarzyszącym im potomstwem. Partnerzy dzielą między sobą obowiązki opieki nad dzieckiem oraz obrony terytorium. Potomstwo opuszcza terytorium rodziców, gdy dorośnie. System ten występuje szczególnie u gibbonowatych, aczkolwiek „monogamia” nie oznacza tutaj koniecznie całkowitej wierności seksualnej[113].
- gatunki żyjące samotnie – często samce bronią terytorium zazębiającego się z terytoriami kilku samic. Taki typ organizacji społecznej spotykany jest u małpiatek, jak kukang. Występuje też u orangutanów, które jednak nie bronią swych terytoriów[114].
Występuje również i inne systemy. Na przykład u wyjców i samce, i samice typowo zmieniają grupę społeczną po osiągnięciu dojrzałości płciowej, w efekcie grupy składają się ze zwierząt niespokrewnionych ze sobą[98]. System ten występuje także u niektórych małpiatek, gerez i pazurkowców[75].
Wymiana samców lub samic stanowi prawdopodobnie adaptację pozwalającą zmniejszyć ryzyko chowu wsobnego[115]. Analiza rozrodu grup wielu różnych gatunków żyjących w niewoli wskazują na wyższą śmiertelność noworodków w przypadku chowu wsobnego niż u dzieci niespokrewnionych rodziców[116][115].

Prymatolożka Jane Goodall, która prowadziła badania w Parku Narodowym Gombe Stream, zauważyła u szympansów społeczności typu fission-fusion society[117]. Grupa rozszczepia się, gdy zwierzęta żerują za dnia (fission), natomiast w nocy osobniki ponownie zbierają się razem do snu (fusion). Taką strukturę społeczną obserwowano także u pawiana płaszczowego[118], czepiaka[98] i bonobo[118]. Dżelada brunatna tworzy podobną strukturę społeczną. Liczne mniejsze grupki zbierają się, tworząc okresowo stada liczące do 600 małp[118].
Na te systemy społeczne wpływają 3 główne czynniki ekologiczne: rozmieszczenie zasobów, liczebność grupy oraz drapieżnictwo[119]. W obrębie grupy wytwarza się równowaga pomiędzy współpracą a współzawodnictwem. Ta pierwsza obejmuje iskanie (obejmujące usuwanie pasożytów i czyszczenie ran), dzielenie się jedzeniem oraz wspólną obronę terytorium lub przed drapieżnikami. Zachowania agresywne często wyrażają konkurencję o pokarm, miejsca do snu bądź partnera. Agresja służy także ustaleniu hierarchii[119][120].
Zgromadzenia międzygatunkowe[edytuj | edytuj kod]
Kilka gatunków naczelnych znanych jest z gromadzenia się razem na wolności. Niektóre z takich zgromadzeń poddano obszernym badaniom. W lesie w Parku Narodowym Taï (Afryka) kilka gatunków wspólnie przeciwdziała drapieżnikom. Chodzi o następujące gatunki naczelnych, ostrzegające się wzajemnie przed drapieżnikiem: koczkodan Diany, koczkodan liberyjski, koczkodan oliwkowy, gerezanka ruda, gereza białobroda i mangaba szara[121]. Do drapieżników należy z kolei szympans zwyczajny[122].
Koczkodan rudoogonowy zbiera się z kilkoma gatunkami, jak gerezanka ruda, koczkodan czarnosiwy, koczkodan barwny, gereza abisyńska, mangabka czarna i koczkodanek błotny[118]. Na pewne gatunki z wymienionych również poluje szympans zwyczajny[123].
W Ameryce Południowej sajmiri gromadzą się wraz z kapucynkami[124], raczej ze względu na korzyści związane ze wspólnym żerowaniem dla sajmiri niż w ochronie przed drapieżnictwem[124].
Funkcje poznawcze i komunikacja[edytuj | edytuj kod]

Naczelne (nie tylko człowiek) wykształciły zaawansowane zdolności poznawcze. Niektóre z nich wykorzystują narzędzia w celu zdobywania pożywienia i w pokazach przed innymi osobnikami[125][126]. Niektóre stosują wysublimowane strategie polowań, w których różne osobniki współpracują ze sobą[127]. Rozwinęły świadomość, zdolności manipulacyjne i oszukańcze[128]. Potrafią rozpoznawać swych krewnych i inne osobniki tego samego gatunku[129][130]. Mają zdolności nauki symboli i zrozumienia pewnych aspektów języka człowieka rozumnego, w tym składni wyznaczającej relacje pomiędzy składnikami zdania i sekwencji numerycznych[131][132][133]. Badania zdolności poznawczych obejmują rozwiązywanie problemów, pamięć, interakcje społeczne, teorię umysłu, myślenie numeryczne, przestrzenne i abstrakcyjne[134]. Badania porównawcze wykazują trend ku wyższej inteligencji w kierunku od Prosimia przez małpy Nowego Świata i małpy Starego Świata do wielkich małp o znacznie wyższych zdolnościach kognitywnych[135][136]. Jednak w obrębie każdej z tych grup istnieje duża zmienność. Na przykład wśród małp szerokonosych czepiak[135] i kapucynki[136] osiągają w pewnych badaniach wysokie wyniki. Różnice istnieją także pomiędzy różnymi badaniami[135][136].
Lemuridae, Lorisidae i wyrakowate, jak też małpy Nowego Świata polegają w wielu kwestiach życia społecznego i rozrodu głównie na zmyśle węchu[17]. Wyspecjalizowane gruczoły służą do oznaczania terytorium z użyciem feromonów, wykrywanych przez narząd lemieszowo-nosowy. Procesy te stanowią znaczną część zachowań związanych z komunikacją tych zwierząt[17]. Koczkodanowce i małpy człekokształtne rozwinęły tę zdolność szczątkowo. To wzrok stał się najważniejszym zmysłem, rozwinęło się widzenie trójbarwne[137]. Naczelne używają też odgłosów, gestów i mimiki, by przekazywać swe stany psychiczne[138]. Wyrak filipiński osiągnął wysoką barierę słyszalnych częstotliwości, średnio 91 kHz. Dominuje u niego jednak częstotliwość 70 kHz. Wartości te należą do najwyższych zarejestrowanych wśród ssaków lądowych i ukazują względnie ekstremalny przykład komunikacji ultradźwiękowej. Wokalizacje ultradźwiękowe wyraków filipińskich mogą reprezentować prywatny kanał komunikacji, nie pozwalają na wykrycie przez drapieżniki, zdobycz i konkurentów, zwiększają wydajność energetyczną lub poprawiają detekcję wśród niskoczęstotliwościowego szumu tła[139].
Cykl życiowy[edytuj | edytuj kod]

Naczelne cechują się wolniejszym tempem rozwoju niż inne ssaki[75]. Wszystkie naczelne karmią swe młode mlekiem (wyjątek stanowią pewne społeczności ludzkie i naczelne trzymane w ogrodach zoologicznych karmione w inny sposób), młode zależą od swych matek także w kwestiach ich toalety i transportu[75]. U niektórych gatunków młode są chronione i przenoszone przez samce, zwłaszcza samce mogące być ich ojcami[75]. Inni krewni niemowlęcia, jak rodzeństwo czy ciotki, również mogą brać udział w opiece[75]. Większość matek naczelnych zaprzestaje owulować podczas karmienia piersią. Kiedy niemowlę zostaje odstawione od piersi, matka może znowu przystąpić do rozrodu[75]. Prowadzi to często do konfliktu – starsze dziecko stara się kontynuować ssanie piersi[75].
Dzieciobójstwo zdarza się często wśród gatunków poligamicznych, jak hulmany czy goryle. Dorosłe samce mogą zabijać niesamodzielne młode niebędące ich dziećmi. Wtedy ich matka powtórnie wchodzi w ruję i może dać potomstwo samcowi-mordercy. Społeczna monogamia u pewnych gatunków mogła wyewoluować jako adaptacja przeciwko temu zachowaniu[140]. Promiskuityzm także obniża ryzyko dzieciobójstwa, ponieważ ojcostwo pozostaje niepewne[141].
Naczelne cechują się dłuższym okresem młodocianym od odstawienia od piersi do osiągnięcia dojrzałości płciowej niż inne ssaki podobnej wielkości[75]. Niektóre z nich, jak galagowate i małpy Nowego Świata wykorzystują jako gniazda dziuple drzew, a podczas żerowania pozostawiają młode w kępach liści. Inne naczelne noszą na sobie swe potomstwo podczas żerowania. Dorosłe zwierzęta mogą budować lub tylko wykorzystywać gniazda, czasami pomagają im osobniki młodociane. Gniazda służą wypoczynkowi. Zachowanie rozwinęło się wtórnie u wielkich małp[142][143]. Podczas okresu młodocianego naczelne są bardziej od dorosłych wrażliwe na ataki drapieżników i głód. Zdobywają dopiero doświadczenie w żerowaniu i unikaniu drapieżników[75]. Zdobywają umiejętności społeczne i uczą się walczyć, często podczas zabawy[75]. Naczelne, zwłaszcza samice, cechują się dłuższym życiem niż inne ssaki podobnych rozmiarów[75]. Może za to częściowo odpowiadać wolniejszy metabolizm[144]. W późnym okresie życia samice małp wąskonosych przestają się rozmnażać, pojawia się menopauza. Inne grupy naczelnych zostały gorzej zbadane[145].
Pożywienie[edytuj | edytuj kod]


Naczelne wykorzystują szeroki wachlarz źródeł pokarmu. Stwierdzono, że wiele cech współczesnych naczelnych, w tym także ludzi, rozwinęło się dzięki żywieniu się ich wczesnych przodków w większości w koronach drzew tropikalnych[146]. Do diety większości naczelnych zaliczają się owoce, dostarczające im łatwostrawnych węglowodanów i tłuszczów, źródła energii[75]. Potrzebują też jednak jeszcze innego pokarmu, jak liście czy owady, by zdobyć aminokwasy, witaminy i sole mineralne. Członkowie podrzędu Strepsirrhini potrafią sami syntetyzować kwas askorbinowy, podczas gdy naczelne rzędu Haplorrhini tę zdolność utraciły. Muszą więc dostarczać sobie witaminy C z pożywieniem[147].
Wiele naczelnych wykształciło przystosowania anatomiczne pozwalające im na eksploatację szczególnych rodzajów pożywienia, jak owoce, liście, gumy roślinne czy owady[75]. Przykładowo liściożerne wyjce, gerezy i lepilemurowate mają wydłużone przewody pokarmowe, zdolne do absorbowania składników odżywczych z trudnych do strawienia liści[75]. Pazurkowcowate żywią się gumami roślinnymi, wobec czego dysponują potężnymi siekaczami, zdolnymi do przegryzania kory drzew i docierania do gum. Ich palce kończą się raczej pazurami niż paznokciami, co umożliwia im wczepianie się w drzewa podczas żerowania[75]. Palczak madagaskarski posiada zęby jak u gryzoni oraz długie, cienkie palce trzecie – zajmuje on niszę ekologiczną dzięcioła. Puka on w drzewo, szukając larw owadów, następnie zaś wygryza w drewnie dziurę, do której wkłada swój wydłużony trzeci palec, by wydostać na zewnątrz larwy[148]. Niektóre gatunki rozwinęły dodatkowe przystosowania. Na przykład zęby mangabki siwolicej pokrywa grube szkliwo, pozwalające jej na otwieranie twardych owoców i nasion, czego nie mogą robić inne małpy[75]. Dżelada brunatna to jedyny gatunek naczelnych żywiący się głównie trawą[149].
Polowanie[edytuj | edytuj kod]

Wyrakokształtne stanowią jedyny współczesny takson obligatoryjnych mięsożerców wśród naczelnych. Spożywają one tylko owady, skorupiaki, małe kręgowce i węże (także gatunki jadowite)[150]. Kapucynki mogą wykorzystywać jako pokarm wiele różnych rodzajów materii roślinnej, jak owoce, liście, kwiaty, pąki, nektar i nasiona, ale zjadają także owady i inne bezkręgowce, ptasie jaja i niewielkie kręgowce, jak ptaki, jaszczurki, wiewiórkowate i nietoperze[98].
Szympans zwyczajny ma zróżnicowaną dietę. Poluje na pewne gatunki naczelnych, jak gerezanka ruda[122][123]. Czasami posługuje się w tym celu narzędziami. Czasami zaostrza patyki, których używa jako broni, polując na ssaki. Uznaje się to za pierwszy dowód na systematyczne użytkowanie broni u gatunku innego niż człowiek rozumny. Badacze udokumentowali dwie sytuacje, w których dzikie szympansy tworzyły z patyków „oszczepy”, by zapolować na galago senegalskie. W każdym przypadku szympans modyfikował łodygę, łamiąc ją na jednym z końców lub na obydwu i, często używając do tego zębów, zaostrzał na końcu. Narzędzie mierzyło średnio 60 cm długości oraz ok. 1 cm obwodu. Następnie szympansy dźgały swymi oszczepami wydrążenia w pniach drzew, gdzie spały galago senegalskie. W jednym przypadku szympansowi udało się wyciągnąć galago przy użyciu swego narzędzia. Z kolei szympans karłowaty jest wszystkożernym owocożercą – większość jego pokarmu stanowią owoce, ale uzupełnia swą dietę liśćmi, mięsem małych kręgowców, jak wiewiórolotkowate, polatuchy i dujkery[151], a także bezkręgowcami[152]. W pewnych warunkach bonobo zjadają inne naczelne (mangabka czarna, koczkodan barwny, koczkodan rudoogonowy)[153][154].
Drapieżnictwo[edytuj | edytuj kod]
Do drapieżników polujących na naczelne zaliczają się różne gatunki drapieżnych, szponiastych, gadów, a także inne naczelne[155]. Spośród ptaków wymienić można karakarę czarnobrzuchą polującą na młode wyjca płaszczowego, harpię wielką, harpię gujańską, wojownika czarnego polujące między innymi na ten sam gatunek. Wśród ssaków na wyjce polują hirara amerykańska, puma płowa, ocelot wielki[156].
Zdobyczą drapieżników padają nawet goryle. Zwierzęta polujące na naczelne wykorzystują różne strategie polowań. Te wykształciły wobec tego różnorodne adaptacje chroniące je przed drapieżnictwem, jak mimikra, odgłosy alarmowe czy mobbing. Kilka gatunków wykorzystuje zróżnicowane odgłosy alarmujące w zależności od tego, czy niebezpieczeństwo zbliża się z powietrza, czy też z ziemi. Drapieżnictwo mogło wyznaczyć rozmiar grup naczelnych, jako że gatunki poddane większej presji ze strony drapieżników wydają się żyć w większych grupach[155].
Narzędzia[edytuj | edytuj kod]
Wykorzystywanie narzędzi[edytuj | edytuj kod]


Istnieją liczne doniesienia o innych niż ludzie naczelnych wykorzystujących narzędzia, zarówno na wolności, jak i w niewoli. Wykorzystywanie narzędzi przez naczelne jest zróżnicowane. Służą im one podczas polowań (na ssaki, ryby, bezkręgowce), zbierania miodu, obrabiania pokarmu (orzechów, innych owoców, warzyw, nasion), zbierania wody, do sporządzania broni i chronienia się.
W 1960 Jane Goodall zaobserwowała szympansy wpychające źdźbło trawy w termitierę, a następnie wkładające je sobie do ust. Po ich odejściu Goodall zbliżyła się do kopca i powtórzyła to zachowanie, by zrozumieć, co robiły szympansy. Okazało się, że termity wchodziły na źdźbło i wgryzały się w nie. Szympans wykorzystywał więc trawę jako narzędzie do odłowu termitów[157]. Bardziej ograniczone doniesienia mówią o używaniu narzędzi na wolności przez blisko spokrewnione szympansy karłowate. Stwierdzono, że rzadko stosują one na wolności narzędzia, ale w niewoli przychodzi im to tak łatwo, jak szympansom zwyczajnym[158]. U obu gatunków z narzędzi chętniej korzystały samice[159]. Orangutany na Borneo wydostają sumy z niewielkich stawów. Antropolożka Anne Russon widziała w lasach tej wyspy, jak kilka zwierząt nauczyło się samodzielnie kłuć ryby patykami. Spanikowana zdobycz wyskakuje wprost w ręce czekającego orangutana[160]. Kilka doniesień opowiada też o gorylach wykorzystujących narzędzia na wolności. Dorosła samica Gorilla gorilla gorilla wykorzystywała gałąź jako laskę, testując głębokość wody i pomagając sobie w przekroczeniu zbiornika wodnego. Inna dorosła samica wykorzystała oderwany pień niewielkiego krzewu jako stabilizator podczas gromadzenia pokarmu, inna użyła kłody jak kładki[161].
Kapucynka brodata była pierwszą małpą zwierzokształtną, w przypadku której udokumentowano posługiwanie się narzędziami na wolności. Osobniki tego gatunku rozbijały orzechy, kładąc je na kamieniu jak na kowadle, a następnie uderzając w nie innym dużym kamieniem[162]. W Tajlandii i Birmie makak krabożerny wykorzystuje kamienie do dobierania się do orzechów, ostryg i innych małży, a także różnych rodzajów ślimaków morskich[163]. Pawiany niedźwiedzie wykorzystują kamienie jako broń. Rzucają nimi z kamienistych zboczy górskich kanionów, gdzie śpią i odpoczywają, jeśli grozi im niebezpieczeństwo. Podnoszą kamienie jedną ręką i przerzucają na drugą stronę, po czym spadają na zbocze lub dno kanionu[164].
Chociaż na wolności nie zaobserwowano, by używały narzędzi, w kontrolowanych warunkach Lemuroidea okazały się zdolne do pojęcia funkcjonalnych cech rzeczy, których uczono ich wykorzystywać jako narzędzia. Radziły sobie tak dobrze, jak Haplorrhini[165].
Wytwarzanie narzędzi[edytuj | edytuj kod]
Wytwarzanie narzędzi jest znacznie rzadsze od prostego ich używania i prawdopodobnie reprezentuje wyższe funkcjonowanie poznawcze. Niedługo po odkryciu wykorzystywania narzędzi Goodall zaobserwowała inne szympansy odzierające z liści gałązki, za pomocą których odławiały one później ryby czy owady. Przekształcenie ulistnionej gałązki w narzędzie było wielkim odkryciem. Wcześniej naukowcy uważali, że tylko ludzie wytwarzają narzędzia oraz że ta zdolność oddziela człowieka od innych zwierząt[157]. Obserwowano zarówno szympansy zwyczajne, jak i bonobo tworzące gąbki z liści i mchów z nagromadzoną wodą, których używały podczas toalety. Orangutany sumatrzańskie również widziano, jak tworzyły i wykorzystywały narzędzia. Łamały gałąź drzewa długości około 30 cm, oddzielały gałązki, strzępiły jeden z końców i wykorzystywały następnie tak stworzone narzędzie do wtykania go w dziuple drzew w poszukiwaniu termitów[166][167]. Na wolności mandryle czyściły sobie uszy zmodyfikowanym przyrządem. Sfilmowano również dużego samca mandryla w Chester Zoo w Wielkiej Brytanii, jak obierał gałązkę, by w widoczny sposób ją zwęzić, a następnie zeskrobywał nią sobie brud spod paznokci u stóp[168]. Trzymane w niewoli goryle tworzą różnorodne narzędzia[169].
Siedlisko[edytuj | edytuj kod]

Primates wyewoluowały ze zwierząt prowadzących nadrzewny tryb życia. Wiele gatunków do tej pory mieszka na drzewach. Większość gatunków zamieszkuje wilgotny las równikowy. Liczba gatunków żyjących na obszarach tropikalnych wydaje się pozytywnie korelować z wielkością opadów deszczu oraz wielkością obszarów lasów deszczowych[170]. Stanowią od 25% do 40% owocożerców (licząc biomasę) tropikalnych lasów deszczwych, odgrywając ważną rolę ekologiczną w rozprzestrzenianiu nasion wielu gatunków drzew[171].
Niektóre gatunki wiodą częściowo naziemny tryb życia. Zaliczają się doń pawiany i patas, a kilka gatunków wiedzie tryb życia w pełni lądowy. Wymienia się tu dżeladę brunatną i człowieka rozumnego. Inne niż człowiek naczelne zamieszkują zróżnicowane siedliska zalesione w zwrotnikowych rejonach Afryki, Indii, Azji Południowo-Wschodniej i Ameryki Północnej, jak lasy deszczowe, namorzyny i lasy górskie. Podaje się też przykłady naczelnych żyjących poza tropikami. Zamieszkujący tereny górskie makak japoński żyje na północy Honsiu, gdzie przez 8 miesięcy w roku ziemię pokrywa śnieg. Makak berberyjski zamieszkuje góry Atlas w Algierii i Maroko. Siedliska naczelnych (nie licząc człowieka) zajmują szeroki zakres wysokości: rokselana czarna zamieszkuje Hengduan Shan, gdzie spotkano ją na wysokości 4.700 m[172]. Goryl górski spotykany jest na wysokości 4.200 m w górach Wirunga[173]. Dżeladę zaś widywano na wysokości 5.000 m na Wyżynie Abisyńskiej. Choć większość gatunków ogólnie stroni od wody, kilka z nich dobrze pływa i dobrze czuje się na bagnach i obszarach podmokłych. Zaliczają się do nich nosacz sundajski, koczkodan nadobny i koczkodanek błotny, co wiąże się z wykształceniem niewielkich błon pławnych między palcami. Niektóre naczelne, jak makak królewski i hulmany, potrafią wykorzystać siedliska zmodyfikowane ręką człowieka. Zamieszkują nawet miasta[118][174].
Interakcje pomiędzy naczelnymi[edytuj | edytuj kod]

Bliskie interakcje pomiędzy człowiekiem a resztą naczelnych (NHP) mogą wiązać się z transmisją chorób odzwierzęcych. Herpeswirus, HBV, Poxviridae, wirus odry, wirus Ebola, wirus wścieklizny, wirus Marburg mogą przenosić się na ludzi z innych naczelnych, w pewnych przypadkach powodują one potencjalnie śmiertelne choroby u ludzi i innych naczelnych[175].
Status prawny[edytuj | edytuj kod]
Jedynie ludzie są uznawani za osoby przez Uniwersalną Deklarację Praw Człowieka ONZ[176]. Status prawny innych naczelnych stanowi natomiast przedmiot debaty. Organizacje takie, jak Great Ape Project (GAP) prowadzą kampanię na rzecz przyznania wielkim małpom przynajmniej pewnych praw[177]. W czerwcu 2008 Hiszpania stała się pierwszym krajem świata, który uznał pewne prawa naczelnych innych niż człowiek, gdzie parlamentarna komisja środowiska rekomendowała przystać na propozycje GAP, zgodnie z którymi szympansy, goryle i orangutany mają nie być wykorzystywane w eksperymentach na zwierzętach[178][179].

Wiele gatunków innych naczelnych ludzie wykorzystują jako zwierzęta domowe. Allied Effort to Save Other Primates (AESOP) szacuje, że około 15 tysięcy osobników trzymanych jest jako egzotyczne zwierzęta domowe w USA[180]. Rozwijająca się klasa średnia w Chińskiej Republice Ludowej również zwiększa na nie zapotrzebowanie[181]. Choć import naczelnych został zabroniony w USA w 1975, przemyt cały czas trwa na granicy z Meksykiem. Cena wynosi od 3000 dolarów za małpę zwierzokształtną do dziesięciokrotności tej sumy za człekokształtną[182].
Naczelne służą jako organizmy modelowe w laboratoriach, wykorzystywano je też w misjach kosmicznych[183]. Pomagają także niepełnosprawnym ludziom. Kapucynki można wytresować do pomocy ludziom z tetraplegią. Ich inteligencja, pamięć i zręczność manualna czynią je dobrymi pomocnikami[184].
Naczelne inne niż człowiek trzymane są w ogrodach zoologicznych na całym świecie. Pierwotnie ogrody zoologiczne stanowiły formę rozrywki, współcześnie skupiły się na ochronie, edukacji i badaniach. GAP nie upiera się przy wypuszczeniu wszystkich naczelnych z zoo, głównie dlatego, że urodzone w niewoli osobniki nie posiadają wiedzy i doświadczenia, które pozwalałyby im przetrwać na wolności[185].
Badania naukowe[edytuj | edytuj kod]
Poza człowiekiem tysiące naczelnych wykorzystuje się na całym świecie w badaniach naukowych z uwagi na ich psychologiczne i fizjologiczne podobieństwo do ludzi[186][187]. W szczególności mózg i oczy tych zwierząt wykazują bliższe podobieństwo do narządów ludzkich niż jakiekolwiek inne zwierzęta. Wykorzystuje się je więc w badaniach przedklinicznych, w neuronauce, oftalmologii, w badaniach toksyczności. Często wykorzystywany jest makak królewski i inne gatunki tego samego rodzaju, kotawiec, szympans, pawian, sajmiri i pazurkowcowate, zarówno urodzone na wolności, jak i w niewoli[186][188]. W 2005 GAP doniósł, że 1280 z 3100 innych niż człowiek naczelnych trzymanych w niewoli w USA było wykorzystywanych do doświadczeń[177]. W 2004 Unia Europejska wykorzystywała około 10000 takich naczelnych w eksperymentach. W 2005 w Wielkiej Brytanii przeprowadzono 4652 doświadczenia z udziałem 3115 naczelnych laboratoryjnych[189]. Rządy wielu państw wprowadziły surowe ograniczenia trzymania w niewoli naczelnych. W USA wytyczne federalne regulują w szerokim zakresie trzymanie naczelnych, karmienie, rozród[190]. Organizacje europejskie takie jak European Coalition to End Animal Experiments działają w celu zakazu wykorzystywania innych niż człowiek naczelnych w doświadczeniach w obrębie nowego europejskiego prawodawstwa dotyczącego testów na zwierzętach[191].
Ochrona[edytuj | edytuj kod]

Międzynarodowa Unia Ochrony Przyrody (IUCN) wymienia ponad jedną trzecią gatunków naczelnych jako krytycznie zagrożone wyginięciem bądź wrażliwe. Handel podlega regulacji, jako że prawie wszystkie gatunki wymienia Załącznik II CITES. Tylko 50 gatunków lub podgatunków wymienia Załącznik I, co oznacza pełną ochronę przez handlem[192][193]. Popularne zagrożenia obejmują wylesianie, fragmentację lasów, zabijanie małp ze strachu o plony[194] i polowania w celu pozyskania zwierząt dla medycyny, jako zwierząt domowych oraz żywności. Najbardziej zagraża im jednak wielkoskalowy wyręb lasów[195][196][197]. Ponad 90% gatunków żyje w lasach tropikalnych[196][198]. Lasy giną głównie przez rolnictwo, ale też przemysł drzewny, plantacje drzewne, górnictwo i budowę tam[198]. W Indonezji wielkie obszary nizinnych lasów wyrąbano w celu zwiększenia produkcji oleju palmowego. Jedna z analiz obrazów satelitarnych pokazała, że pomiędzy 1998 i 1999 spadek populacji orangutanów sumatrzańskich wyniósł 1000 osobników rocznie w samym tylko ekosystemie Leuser[199].

Większe naczelne, przekraczające masę 5 kg, podlegają większemu ryzyku zagłady, są bowiem bardziej zyskowne dla kłusowników w porównaniu z mniejszymi krewnymi[198]. Później osiągają też dojrzałość płciową, rzadziej wydają na świat potomstwo. Ich populacje odnawiają się wobec tego wolniej po uszczupleniu przez kłusowników bądź handlarzy[200]. Dane z miast afrykańskich pokazują, że połowa wszystkich białek spożywanych na tamtejszych obszarach miejskich pochodzi z bushmeat[201]. Zagrożone naczelne, jak koczkodany i mandryl równikowy, stanowią obiekty polowań na poziomie znacznie przekraczającym pozwalający na utrzymanie równowagi[201] ze względu na ich duże rozmiary, łatwy transport i zyskowność[201]. Gdy farmy wkraczają na tereny leśne, naczelne pasą się na plonach, narażając farmerów na poważne straty[202]. Te wycieczki naczelnych przyczyniają się do ich negatywnej opinii wśród lokalnej społeczności, co utrudnia wysiłki w celu ich ochrony[203].
Madagaskar, stanowiący dom dla pięciu endemicznych rodzin naczelnych, stanowi miejsce największej zagłady naczelnych w ostatnich czasach. Od kiedy ludzie przybyli tam 1.500 lat temu, przynajmniej 15 gatunków większych naczelnych wyginęło z powodu polowań i destrukcji siedlisk[17]. Należy doń większy od goryla Archaeoindris, a także całe rodziny Palaeopropithecidae i Archaeolemuridae[17].
W Azji hinduizm, buddyzm i islam zabraniają spożycia mięsa naczelnych. Pomimo tego na te zwierzęta i tak poluje się dla pożywienia[198]. Niektóre mniejsze, tradycyjne religie pozwalają na konsumpcję mięsa naczelnych[204][205]. Handel zwierzętami domowymi i medycyna tradycyjna także zwiększają popyt na nielegalne polowania[181][206][207]. Makak królewski, organizm modelowy, został objęty ochroną po rozległych łowach w latach sześćdziesiątych. Program okazał się tak efektywny, że obecnie uważa się go za szkodnika[197].

W Azji środkowej, jak też Południowej fragmentacja lasów i polowania stanowią dwa główne problemy zagrażające naczelnym. Wielkie połacie leśne są obecnie rzadkością w Ameryce Środkowej[195][208]. Zwiększa to ilość obszarów leśnych narażonych na tzw. efekt krawędzi (ang. edge effect) – wkraczanie farm, mniejsza wilgotność, zmiany florystyczne[209][210]. Ograniczenia przemieszczania się skutkują zwiększeniem chowu wsobnego, co szkodzi populacji. Prowadzi to do efektu wąskiego gardła, kiedy pozostaje niewielki procent populacji[211][212].
Wyróżnia się 21 krytycznie zagrożonych gatunków naczelnych, z których 7 pozostaje na liście IUCN od 2000 (stan na 2015). Chodzi o takie gatunki jak: sifaka srebrzysta, langur białozady, lutung jasnogłowy, duk szaronogi, rokselana zadartonosa, goryl zachodni i orangutan sumatrzański[213]. Gerezankę samotną uznano za wymarłą, jako że między 1993 a 1999 nie znaleziono żadnych śladów istnienia tego podgatunku[214]. Kilku myśliwych zabiło później kilka osobników, ale perspektywy podgatunku nadal rysują się czarno[215].
Przypisy[edytuj | edytuj kod]
- ↑ C. Linnaeus: Systema naturae per regna tria naturae, secundum classes, ordines, genera, species, cum characteribus, differentiis, synonymis, locis. Wyd. 10. T. 1. Holmiae: Impensis Direct. Laurentii Salvii, 1758, s. 20. (łac.).
- ↑ J.F. Blumenbach: Handbuch der Naturgeschichte: mit Kupfern. T. 1. Göttingen: Johann Christian Dieterich, 1779, s. 79. (niem.).
- ↑ J.F. Blumenbach: Handbuch der Naturgeschichte: mit Kupfern. Wyd. 5. Göttingen: Bey Johann Christian Dieterich, 1791, s. 57. (niem.).
- ↑ Ch.K. André: Der Zoologe, oder Compendiöse Bibliothek des Wissenswürdigsten aus der Thiergeschichte und allgemeinen Naturkunde. Cz. 2–3. Eisenach: Johann Jacob Gebauer, 1795, s. 25. (niem.).
- ↑ a b C.S. Rafinesque: Analyse de la nature, or, Tableau de l’univers et des corps organisés. Palerme: Aux dépens de l’auteur, 1815, s. 53. (fr.).
- ↑ a b J.E. Gray. On the Natural Arrangment of Vertebrose Animals. „The London Medical Repository”. 15, s. 297, 1821. (ang.).
- ↑ a b W. Ogilby. Observations upon the opposable power of the thumb in certain Mammals, considered as a zoological character, and on the natural affinities which subsist between the Bimana, Quadrumana, and Pedimana. „Proceedings of the Zoological Society of London”. 4, s. 28, 1836. (ang.).
- ↑ É.L. Trouessart. Synopsis sytematicus et geographicus mammalium. „Revue et magasin de zoologie pure et appliquée”. 3e série. 7, s. 225, 1879. (fr.).
- ↑ M. Schlosser. Beitrag zur Osteologie und systematischen Stellung der Gattung Necrolemur, sowie zur Stammesgeschichte der Primaten überhaupt. „Neues Jahrbuch für Mineralogie, Geologie und Paläontologie”. Festband 1807–1907, s. 222, 1907. (niem.).
- ↑ P.D. Gingerich: Cranial anatomy and evolution of early Tertiary Plesiadapidae (Mammalia, Primates). Ann Arbor, Michigan: Xerox University Microfilms, 1974, s. 1–305. (ang.).
- ↑ P.D. Gingerich. New North American Plesiadapidae (Mammalia, Primates) and a biostratigraphic zonation of the Middle and Upper Paleocene. „Contributions from the Museum of Paleontology, University of Michigan”. 24 (13), s. 136, 1975. (ang.).
- ↑ R. Hoffstetter. Phylogenie et classification: l’example des Primates. „Bulletin de la Société Zoologique de France”. 103, s. 183–188, 1978. (fr.).
- ↑ L.M. Van Valen. The origin of the plesiadapid primates and the nature of Purgatorius. „Evolutionary Monographs”. 15, s. 41, 1994. (ang.).
- ↑ І.В. Загороднюк. Наукові назви рядів ссавців: від описових до уніфікованих. „Вісник Львів. Ун-ту”. Серія біологічна. 48, s. 36, 2008. (ukr.).
- ↑ a b c d e f g h i Wilson Don E. & Reeder DeeAnn M. (red.) Primates. w: Mammal Species of the World. A Taxonomic and Geographic Reference (Wyd. 3.) [on-line]. Johns Hopkins University Press, 2005. (ang.) [dostęp 2 sierpnia 2011]
- ↑ Primate. W: Merriam-Webster Online Dictionary. Merriam-Webster. [dostęp 2008-07-21].
ze starofrancuskiego lub francuskiego primat, od łacińskiego słowa primat-, od primus – „pierwszy” - ↑ a b c d e f g primate, [w:] Encyclopædia Britannica [dostęp 2008-07-21] (ang.).
- ↑ O'Leary, M. A.. The placental mammal ancestor and the post–K-Pg radiation of placentals. „Science”. 339 (6120), s. 662–667, 2013. DOI: 10.1126/science.1229237. PMID: 23393258.
- ↑ a b Helen J. Chatterjee i inni, Estimating the phylogeny and divergence times of primates using a supermatrix approach, „BMC Evolutionary Biology”, 1, 9, 2009, s. 259, DOI: 10.1186/1471-2148-9-259, PMID: 19860891, PMCID: PMC2774700.
- ↑ Roscoe Stanyon i inni, Macroevolutionary Dynamics and Historical Biogeography of Primate Diversification Inferred from a Species Supermatrix, „PLoS ONE”, 7 (11), 2012, e49521, DOI: 10.1371/journal.pone.0049521, ISSN 1932-6203.
- ↑ Natalie M. Jameson i inni, Genomic data reject the hypothesis of a prosimian primate clade, „Journal of Human Evolution”, 61 (3), 2011, s. 295–305, DOI: 10.1016/j.jhevol.2011.04.004, ISSN 0047-2484.
- ↑ Luca Pozzi i inni, Primate phylogenetic relationships and divergence dates inferred from complete mitochondrial genomes, „Molecular Phylogenetics and Evolution”, 75, 2014, s. 165–183, DOI: 10.1016/j.ympev.2014.02.023, ISSN 1055-7903.
- ↑ Roscoe Stanyon i inni, A Mitogenomic Phylogeny of Living Primates, „PLoS ONE”, 8 (7), 2013, e69504, DOI: 10.1371/journal.pone.0069504, ISSN 1932-6203.
- ↑ Anon.: Encyclopædia Britannica. Wyd. 11. T. XIX. New York: Encyclopædia Britannica, 1911. [dostęp 2011-07-10].
- ↑ A.F. Dixson: The Natural History of the Gorilla. London: Weidenfeld & Nicholson, 1981. ISBN 978-0-297-77895-0.
- ↑ Clive A. Stace, Classification by molecules: What's in it for field botanists?, „Watsonia”, 28, 2010, s. 103–122 [dostęp 2010-02-07] [zarchiwizowane z adresu 2011-07-26].
- ↑ Brent D Mishler, F.J. Ayala: R. Arp: Contemporary Debates in Philosophy of Biology. 2009, s. 110–122. DOI: 10.1002/9781444314922.ch6. ISBN 978-1-4443-1492-2.
- ↑ a b M. Cartmill, F. H. Smith: The Human Lineage. John Wiley & Sons, 2011. ISBN 978-1-118-21145-8.
- ↑ a b Groves, C. P.: Primate Taxonomy. Smithsonian Institution Press, 2001. ISBN 1-56098-872-X.
- ↑ Michael J. Benton: Vertebrate palaeontology. Wiley-Blackwell, 2005, s. 371. ISBN 978-0-632-05637-8. [dostęp 2011-07-10].
- ↑ Michael J. Benton: Vertebrate palaeontology. Wiley-Blackwell, 2005, s. 378-380. ISBN 978-0-632-05637-8. [dostęp 2011-07-10].
- ↑ Linnaeus, C.: Sistema naturae per regna tria Naturae, secundum classes, ordines, genera, species, cum characteribus differentiis, synonimis locis. Tomus I. Impensis direct. Laurentii Salvii, Holmia, 1758, s. 20–32.
- ↑ Linnaeus, C.: Sistema naturae sive regna tria Naturae systematice proposita per classes, ordines, genera, & species. apud Theodorum Haak, Lugduni Batavorum, 1735, s. s.p..
- ↑ Nouvelle classification des Mammifères. W: Blainville, H.: Annales Françaises et Etrangères d'Anatomie et de Physiologie Appliquées à la Médicine et à l'Histoire Naturelle, 3. 1839, s. 268–269.
- ↑ Thorington, R. W., Jr. & Anderson, S.: Primates. W: Anderson, S. & Jones, J. K., Jr.: Orders and Families of Recent Mammals of the World. New York: John Wiley and Sons, 1984, s. 187–217.
- ↑ McKenna, M. C. & Bell, S. K.: Classification of Mammals: Above the species level. New York: Columbia University Press, 1997, s. 631. ISBN 0-231-11013-8.
- ↑ Strier, K.: Primate Behavioral Ecology. Wyd. Third. 2007, s. 50–53. ISBN 0-205-44432-6.
- ↑ N. Upham, C. Burgin, J. Widness, M. Becker, C. Parker, S. Liphardt, I. Rochon & D. Huckaby: Treeview of Mammalian Taxonomy Hierarchy. [w:] ASM Mammal Diversity Database (Version 1.11) [on-line]. American Society of Mammalogists. [dostęp 2023-09-01]. (ang.).
- ↑ C.J. Burgin: Introduction. W: Lynx Nature Books: All the Mammals of the World. Barcelona: Lynx Edicions, 2023, s. 22. ISBN 978-84-16728-66-4. (ang.).
- ↑ C.J. Burgin, D.E. Wilson, R.A. Mittermeier, A.B. Rylands, T.E. Lacher & W. Sechrest: Illustrated Checklist of the Mammals of the World. Cz. 1: Monotremata to Rodentia. Barcelona: Lynx Edicions, 2020, s. 26. ISBN 978-84-16728-34-3. (ang.).
- ↑ a b Nazwy polskie za: W. Cichocki, A. Ważna, J. Cichocki, E. Rajska-Jurgiel, A. Jasiński & W. Bogdanowicz: Polskie nazewnictwo ssaków świata. Warszawa: Muzeum i Instytut Zoologii PAN, 2015, s. 28–54. ISBN 978-83-88147-15-9. (pol. • ang.).
- ↑ a b Mittermeier, R., Ganzhorn, J., Konstant, W., Glander, K., Tattersall, I., Groves, C., Rylands, A., Hapke, A., Ratsimbazafy, J., Mayor, M., Louis, E., Rumpler, Y., Schwitzer, C. & Rasoloarison, R.. Lemur Diversity in Madagascar. „International Journal of Primatology”. 29 (6), s. 1607–1656, 2008-12. DOI: 10.1007/s10764-008-9317-y.
- ↑ a b Rylands, A. B. & Mittermeier, R. A.: The Diversity of the New World Primates (Platyrrhini). W: Garber, P. A., Estrada, A., Bicca-Marques, J. C., Heymann, E. W. & Strier, K. B.: South American Primates: Comparative Perspectives in the Study of Behavior, Ecology, and Conservation. Springer, 2009. ISBN 978-0-387-78704-6.
- ↑ a b Hartwig 2011 ↓, s. 20–21.
- ↑ Szalay i Delson 1980 ↓, s. 149.
- ↑ M. Cartmill: Primate Classification and Diversity. W: M. Platt, A Ghazanfar: Primate Neuroethology. Oxford University Press, 2010, s. 15. ISBN 978-0-19-532659-8.
- ↑ J.E. Janečka i inni, Molecular and Genomic Data Identify the Closest Living Relative of Primates, „Science”, 318 (5851), 2007, s. 792–794, DOI: 10.1126/science.1147555, PMID: 17975064, Bibcode: 2007Sci...318..792J [dostęp 2008-08-17] [zarchiwizowane z adresu 2008-06-21].
- ↑ Kavanagh, M.: A Complete Guide to Monkeys, Apes and Other Primates. New York: Viking Press, 1983, s. 18. ISBN 0-670-43543-0.
- ↑ McKenna, M. C. and Bell, S. K.: Classification of Mammals Above the Species Level. New York: Columbia University Press, 1997, s. 329. ISBN 0-231-11012-X.
- ↑ B.A. Williams, R.F. Kay, E.C. Kirk. New perspectives on anthropoid origins. „Proceedings of the National Academy of Sciences”. 107 (11), s. 4797–4804, 2010. DOI: 10.1073/pnas.0908320107. PMID: 20212104. PMCID: PMC2841917. Bibcode: 2010PNAS..107.4797W.
- ↑ B. A. Williams, R. F. Kay, E. C. Kirk. New perspectives on anthropoid origins. „Proceedings of the National Academy of Sciences”. 107 (11), s. 4797–4804, 2010. DOI: 10.1073/pnas.0908320107. PMID: 20212104. Bibcode: 2010PNAS..107.4797W. (ang.).
- ↑ Miller, E. R.; Gunnell, G. F.; Martin, R. D.. Deep Time and the Search for Anthropoid Origins". „American Journal of Physical Anthropology”. 128, s. 60–95, 2005. DOI: 10.1002/ajpa.20352.
- ↑ Lee, M.. Molecular Clock Calibrations and Metazoan Divergence Dates. „Journal of Molecular Evolution”. 49 (3), s. 385–391, 1999-08. DOI: 10.1007/PL00006562. PMID: 10473780.
- ↑ Scientists Push Back Primate Origins From 65 Million To 85 Million Years Ago. „Science Daily”, 2002-04-18. [dostęp 2008-10-24].
- ↑ Tavaré, S., Marshall, C. R., Will, O., Soligo, C. & Martin R.D.. Using the fossil record to estimate the age of the last common ancestor of extant primates. „Nature”. 416 (6882), s. 726–729, 2002-04-18. DOI: 10.1038/416726a. PMID: 11961552. Bibcode: 2002Natur.416..726T.
- ↑ Klonisch, T., Froehlich, C., Tetens, F., Fischer, B. & Hombach-Klonisch, S.. Molecular Remodeling of Members of the Relaxin Family During Primate Evolution. „Molecular Biology and Evolution”. 18 (3), s. 393–403, 2001. DOI: 10.1093/oxfordjournals.molbev.a003815. PMID: 11230540. [dostęp 2008-08-22].
- ↑ a b c d e J. Horvath i inni, Development and Application of a Phylogenomic Toolkit: Resolving the Evolutionary History of Madagascar's Lemurs, „Genome Research”, 18 (3), 2008, s. 489–499, DOI: 10.1101/gr.7265208, PMID: 18245770, PMCID: PMC2259113 [dostęp 2008-08-22].
- ↑ a b Bill Sellers: Primate Evolution. University of Edinburgh, 2000-10-20. s. 13–17. [dostęp 2008-10-23].
- ↑ a b c d Primate Evolution. W: Hartwig, W.: Primates in Perspective. Campbell, C., Fuentes, A., MacKinnon, K., Panger, M. & Bearder, S. (editors). Oxford University Press, 2007, s. 13–17. ISBN 978-0-19-517133-4.
- ↑ B. A. Williams, R. F. Kay, E. Christopher Kirk, C. F. Ross. Darwinius masillae is a strepsirrhine—a reply to Franzen et al. (2009). „Journal of Human Evolution”. 59 (5), s. 567–573; discussion 573–9, 2010. DOI: 10.1016/j.jhevol.2010.01.003. PMID: 20188396. (ang.).
- ↑ Ciochon, R. & Fleagle, J.: Primate Evolution and Human Origins. Menlo Park, California: Benjamin/Cummings, 1987, s. 72. ISBN 978-0-202-01175-2.
- ↑ a b N. Garbutt: Mammals of Madagascar, A Complete Guide. A&C Black Publishers, 2007, s. 85–86. ISBN 978-0-300-12550-4.
- ↑ a b R. A. Mittermeier, et al.: Lemurs of Madagascar. Wyd. 2. Conservation International, 2006, s. 23–26. ISBN 1-881173-88-7.
- ↑ Shekelle, M.: Evolutionary Biology of Tarsiers. 2005. [dostęp 2008-08-22]. [zarchiwizowane z tego adresu (2008-09-07)].
- ↑ T. Schmidt i inni, Rapid electrostatic evolution at the binding site for cytochrome c on cytochrome c oxidase in anthropoid primates, „Proceedings of the National Academy of Sciences of the United States of America”, 102 (18), 2005, s. 6379–6384, DOI: 10.1073/pnas.0409714102, PMID: 15851671, PMCID: PMC1088365, Bibcode: 2005PNAS..102.6379S.
- ↑ Lizzie Wade: Early Primate Weighed Less Than an Ounce. ScienceNow, 2013-06-05. [dostęp 2013-06-07]. [zarchiwizowane z tego adresu (2013-06-08)].
- ↑ R. F. Kay. Evidence for an Asian origin of stem anthropoids. „Proceedings of the National Academy of Sciences”. 109 (26), s. 10132–10133, 2012-06-26. DOI: 10.1073/pnas.1207933109. ISSN 0027-8424. Bibcode: 2012PNAS..10910132K.
- ↑ Y. Chaimanee, O. Chavasseau, K. C. Beard, A. A. Kyaw i inni. Late Middle Eocene primate from Myanmar and the initial anthropoid colonization of Africa. „Proceedings of the National Academy of Sciences”. 109 (26), s. 10293, 2012. DOI: 10.1073/pnas.1200644109. (ang.).
- ↑ L. Marivaux i inni, Anthropoid primates from the Oligocene of Pakistan (Bugti Hills): Data on early anthropoid evolution and biogeography, „Proceedings of the National Academy of Sciences of the United States of America”, 102 (24), 2005, s. 8436–8441, DOI: 10.1073/pnas.0503469102, PMID: 15937103, PMCID: PMC1150860, Bibcode: 2005PNAS..102.8436M.
- ↑ Schrago, C.G. & Russo, C.A.M.. Timing the Origin of New World Monkeys. „Molecular Biology and Evolution”. 20 (10), s. 1620–1625, 2003. DOI: 10.1093/molbev/msg172. PMID: 12832653.
- ↑ a b Céline Poux, Pascale Chevret, Dorothée Huchon, Wilfried W. de Jong & Emmanuel J. P. Douzery. Arrival and Diversification of Caviomorph Rodents and Platyrrhine Primates in South America. „Systematic Biology”. 55, s. 228-244, 2006. DOI: 10.1080/10635150500481390. (ang.).
- ↑ P.D. Gingerich: Eocene Adapidae, paleobiogeography, and the origin of South American Platyrrhini. W: Evolutionary biology of the New World monkeys and continental drift. Springer, 1980, s. 123-138.
- ↑ A. Houle, The origin of platyrrhines: An evaluation of the Antarctic scenario and the floating island model, „American Journal of Physical Anthropology”, 109 (4), 1999, s. 541–559, DOI: 10.1002/(SICI)1096-8644(199908)109:4<541::AID-AJPA9>3.0.CO;2-N, PMID: 10423268.
- ↑ Andrews, P. & Kelley, J.. Middle Miocene Dispersals of Apes. „Folia Primatologica”. 78 (5–6), s. 328–343, 2007. DOI: 10.1159/000105148. PMID: 17855786.
- ↑ a b c d e f g h i j k l m n o p q r s t u Strier, K.: Primate Behavioral Ecology. Wyd. 3. Allyn & Bacon, 2007, s. 7, 64, 71, 77, 182–185, 273–280, 284, 287–298. ISBN 0-205-44432-6.
- ↑ J. Wallis i inni, Macaca sylvanus, [w:] The IUCN Red List of Threatened Species [dostęp 2023-01-05] (ang.).
- ↑ Primate Evolution and the Emergence of Humans, [w:] Pough i inni, Vertebrate Life, wyd. 7, Pearson, 2005, s. 650, ISBN 0-13-127836-3.
- ↑ Tenaza, R.. Songs of hybrid gibbons (Hylobates lar × H. muelleri). „American Journal of Primatology”. 8 (3), s. 249–253, 1984. DOI: 10.1002/ajp.1350080307.
- ↑ a b Bernsteil, I. S.. Naturally occurring primate hybrid. „Science”. 154 (3756), s. 1559–1560, 1966. DOI: 10.1126/science.154.3756.1559. PMID: 4958933. Bibcode: 1966Sci...154.1559B.
- ↑ Sugawara, K.. Sociological study of a wild group of hybrid baboons between Papio anubis and P. hamadryas in the Awash Valley, Ethiopia. „Primates”. 20 (1), s. 21–56, 1979. DOI: 10.1007/BF02373827.
- ↑ C. J. Jolly, Tamsin Woolley-Barker, Shimelis Beyene, Todd R. Disotell i inni. Intergeneric Hybrid Baboons. „International Journal of Primatology”. 18 (4), s. 597–627, 1997. DOI: 10.1023/A:1026367307470.
- ↑ a b c d Characteristics of Primates. W: Pough, F. W., Janis, C. M. & Heiser, J. B.: Vertebrate Life. Wyd. 7. Pearson, 2005, s. 630. ISBN 0-13-127836-3.
- ↑ Campbell, B. G. & Loy, J. D.: Humankind Emerging (8th edition). Allyn & Bacon, 2000, s. 85. ISBN 0-673-52364-0.
- ↑ a b Aiello, L. & Dean, C.: An Introduction to Human Evolutionary Anatomy. Academic Press, 1990, s. 193. ISBN 0-12-045590-0.
- ↑ a b White, T. & Kazlev, A: Archonta: Primates. Palaeos, 2006-01-08. [dostęp 2008-06-03]. [zarchiwizowane z tego adresu (2008-05-12)].
- ↑ PA Garber, JA Rehg, The ecological role of the prehensile tail in white-faced capuchins (Cebus capucinus), „American Journal of Physical Anthropology”, 110 (3), 1999, s. 325–39, DOI: 10.1002/(SICI)1096-8644(199911)110:3<325::AID-AJPA5>3.0.CO;2-D, PMID: 10516564.
- ↑ Russo GA, Young JW. Tail growth tracks the ontogeny of prehensile tail use in capuchin monkeys (Cebus albifrons and C. apella). „American Journal of Physical Anthropology”. 146 (3), s. 465–473, 2011. DOI: 10.1002/ajpa.21617. PMID: 21953012.
- ↑ Friderun Ankel-Simons: Primate Anatomy: An Introduction. Academic Press, 2010-07-27. ISBN 978-0-08-046911-9.
- ↑ a b c d e f g Primates. W: David Macdonald: The Encyclopedia of Mammals. The Brown Reference Group plc, 2006, s. 290–307. ISBN 0-681-45659-0.
- ↑ a b c d e f Myers, P: „Primates” (On-line). Animal Diversity Web, 1999. [dostęp 2008-06-03].
- ↑ Ash, M. M., Nelson, S. J. & Wheeler, R. C.: Wheeler’s Dental Anatomy, Physiology, and Occlusion. W.B. Saunders, 2003, s. 12. ISBN 978-0-7216-9382-8.
- ↑ a b c Yoav Gilad, Victor Wiebe, Molly Przeworski, Doron Lancet & Svante Pääbo. Loss of Olfactory Receptor Genes Coincides with the Acquisition of Full Trichromatic Vision in Primates. „PloS Biology”. 2, s. e5, 2004. DOI: 10.1371/journal.pbio.0020005. (ang.).
- ↑ Gustavo Glusman, Itai Yanai, Irit Rubin & Doron Lancet. The Complete Human Olfactory Subgenome. „Genome Research”. 11, s. 685–702, 2001. DOI: 10.1101/gr.171001. (ang.).
- ↑ C.A. Arrese i inni, Cone topography and spectral sensitivity in two potentially trichromatic marsupials, the quokka (''Setonix brachyurus'') and quenda (''Isoodon obesulus''), „Proceedings of Biological Science”, 272 (1565), 2005, s. 791–6, DOI: 10.1098/rspb.2004.3009, PMID: 15888411, PMCID: PMC1599861.
- ↑ J.K. Bowmaker i inni, Photosensitive and photostable pigments in the retinae of Old World monkeys, „Journal of Experimental Biology”, 156 (1), 1991, s. 1–19, ISSN 0022-0949, PMID: 2051127 [dostęp 2008-06-16].
- ↑ a b A.K. Surridge, D. Osorio, N.I. Mundy, Evolution and selection of trichromatic vision in primates, „Trends in Ecology and Evolution”, 4, 18, 2003, s. 198–205, DOI: 10.1016/S0169-5347(03)00012-0.
- ↑ Peter W. Lucas i inni, Evolution and function of routine trichromatic vision in primates, „Evolution”, 57 (11), 2003, s. 2636–43, DOI: 10.1554/03-168, PMID: 14686538.
- ↑ a b c d e Sussman, R. W.: Primate Ecology and Social Structure, Volume 2: New World Monkeys. Needham Heights, MA: Pearson Custom Publishing & Prentice Hall, 2003, s. 77–80, 132–133, 141–143. ISBN 0-536-74364-9.
- ↑ K. Ralls. Mammals in Which Females are Larger Than Males. „The Quarterly Review of Biology”. 51 (2), s. 245–276, 1976. DOI: 10.1086/409310. PMID: 785524.
- ↑ Lindstedtand & Boyce, Mark S. Boyce. Seasonality, Fasting Endurance, and Body Size in Mammals. „The American Naturalist”. 125 (6), s. 873, 1985. DOI: 10.1086/284385.
- ↑ Frisch, J. E. Sex-differences in the canines of the gibbon (Hylobates lar). „Primates”. 4 (2), s. 1–10, 1963. DOI: 10.1007/BF01659148.
- ↑ Kay, R. F. The functional adaptations of primate molar teeth. „American Journal of Physical Anthropology”. 43 (2), s. 195–215, 1975. DOI: 10.1002/ajpa.1330430207. PMID: 810034.
- ↑ Sexual selection, dimorphism, and social organization in the primates. W: Crook, J. H.: Sexual selection and the descent of man. Campbell, B. G. (editor). Aldine Transaction, 1972, s. 246. ISBN 978-0-202-02005-1.
- ↑ P. O’Higgins, M. Collard, Sexual dimorphism and facial growth in papionine monkeys, „Journal of Zoology”, 257 (2), 2002, s. 255–72, DOI: 10.1017/S0952836902000857.
- ↑ a b J.M. Cheverud, M.M. Dow, W. Leutenegger, The quantitative assessment of phylogenetic constraints in comparative analyses: Sexual dimorphism in body weight among primates, „Evolution”, 6, 39, 1985, s. 1335–1351, DOI: 10.2307/2408790, JSTOR: 2408790.
- ↑ W. Leutenegger, J.M. Cheverud, Correlates of sexual dimorphism in primates: Ecological and size variables, „International Journal of Primatology”, 4, 3, 1982, s. 387–402, DOI: 10.1007/BF02693740.
- ↑ a b Plavcan, J. M. Sexual dimorphism in primate evolution. „American Journal of Physical Anthropology”. 33, s. 25–53, 2001. DOI: 10.1002/ajpa.10011. PMID: 11786990.
- ↑ Sussman, R. W.: Primate Ecology and Social Structure Volume 1: Lorises, Lemurs and Tarsiers. Needham Heights, MA: Pearson Custom Publishing & Prentice Hall, 1999, s. 78, 89–90, 108, 121–123, 233. ISBN 0-536-02256-9.
- ↑ S.D. Glazier, C.A. Flowerday: Selected Readings in the Anthropology of Religion: Theoretical and Methodological Essays. Greenwood Publishing Group, 2003, s. 53. ISBN 978-0-313-30090-5.
- ↑ Peter Kappeler, C. van Schaik, Primate social systems, 2003.
- ↑ Mutualism, kinship and social evolution. W: Wrangham, R. W.: Current Problems in Sociobiology. Cambridge University Press, 1982, s. 269–89. ISBN 0-521-24203-7.
- ↑ The Atelines. W: Fiore, A. D. & Campbell, C. J.: Primates in Perspective. Campbell, C. J., Fuentes, A., MacKinnon, K. C., Panger, M. & Bearder, S. K. (editors). Oxford University Press, 2007, s. 175. ISBN 978-0-19-517133-4.
- ↑ The Hylobatidae. W: Bartlett, T. Q.: Primates in Perspective. Campbell, C. J., Fuentes, A., MacKinnon, K. C., Panger, M. & Bearder, S. K. (editors). Oxford University Press, 2007, s. 283. ISBN 978-0-19-517133-4.
- ↑ Orangutans in Perspective. W: Knott, C. D. & Kahlenberg, S. M.: Primates in Perspective. Campbell, C. J., Fuentes, A., MacKinnon, K. C., Panger, M. & Bearder, S. K. (editors). Oxford University Press, 2007, s. 294. ISBN 978-0-19-517133-4.
- ↑ a b Charpentier MJ, Widdig A, Alberts SC. Inbreeding depression in non-human primates: a historical review of methods used and empirical data. „Am. J. Primatol.”. 69 (12), s. 1370–86, 2007. DOI: 10.1002/ajp.20445. PMID: 17486606.
- ↑ Ralls K, Ballou J.. Effect of inbreeding on infant mortality in captive primates. „International Journal of Primatology”. 3 (4), s. 491-505, 1982. DOI: 10.1007/BF02693747.
- ↑ Constable J. L. i inni, Noninvasive paternity assignment in Gombe chimpanzees, „Molecular Ecology”, 5, 10, 2001, s. 1279–300, DOI: 10.1046/j.1365-294X.2001.01262.x, PMID: 11380884.
- ↑ a b c d e Rowe, N.: The Pictorial Guide to the Living Primates. Pogonias Press, 1996, s. 4, 139, 143, 154, 185, 223. ISBN 0-9648825-0-7.
- ↑ a b Primate Societies. W: Pough, F. W., Janis, C. M. & Heiser, J. B.: Vertebrate Life. Wyd. 7. Pearson, 2005, s. 621–623. ISBN 0-13-127836-3.
- ↑ Smuts, B.B., Cheney, D.L. Seyfarth, R.M., Wrangham, R.W., & Struhsaker, T.T. (Red.) (1987). Primate Societies. Chicago: University of Chicago Press for articles on the structure and function of various primate societies.
- ↑ Interactions between African Crowned Eagles and Their Prey Community. W: Shultz, S. & Thomsett, S.: Monkeys of Tai Forest, An African Primate Community. McGraw, W., Zuberbuhler, K. & Noe, R. (editors). Cambridge University Press, 2007, s. 181. ISBN 0-521-81633-5.
- ↑ a b Interactions between Red Colobus Monkeys and Chimpanzees. W: Bshary, R.: Monkeys of the Taï Forest: an African primate community. McGraw, W., Zuberbuhler, K. & Noe, R. (red.). Cambridge University Press, 2007, s. 155–170. ISBN 0-521-81633-5.
- ↑ a b Stanford, C.: Chimpanzee and red colobus : the ecology of predator and prey. Harvard University Press, 1998, s. 130–138, 233. ISBN 0-674-00722-0.
- ↑ a b Social Manipulation Within and Between Troops Mediates Primate Group Movement. W: Boinski, S.: On the Move : how and why animals travel in groups. Boinski, S. and Garber, P. (editors). University of Chicago Press, 2000, s. 447–448. ISBN 0-226-06340-2.
- ↑ C. Boesch, H. Boesch, Tool Use and Tool Making in Wild Chimpanzees, „Folia Primatol”, 1–2, 54, 1990, s. 86–99, DOI: 10.1159/000156428, PMID: 2157651.
- ↑ G. C. Westergaard, A. L. Lundquist, Michael Katherine Haynie, Heather E. Kuhn i inni. Why some capuchin monkeys (Cebus apella) use probing tools (and others do not). „Journal of Comparative Psychology”. 112 (2), s. 207–211, 1998. DOI: 10.1037/0735-7036.112.2.207. PMID: 9642788.
- ↑ F.B.M. de Waal, J.M. Davis, Capuchin cognitive ecology: cooperation based on projected returns, „Neuropsychologia”, 2, 41, 2003, s. 221–228, DOI: 10.1016/S0028-3932(02)00152-5, PMID: 12459220.
- ↑ L.A. Paar i inni, Recognizing facial cues: Individual discrimination by chimpanzees (''Pan troglodytes'') and rhesus monkeys (''Macaca mulatta''), „Journal of Comparative Psychology”, 1, 114, 2000, s. 47–60, DOI: 10.1037/0735-7036.114.1.47, PMID: 10739311, PMCID: PMC2018744.
- ↑ L.A. Paar, F.B.M. de Waal, Visual kin recognition in chimpanzees, „Nature”, 6737, 399, 1999, s. 647–648, DOI: 10.1038/21345, PMID: 10385114, Bibcode: 1999Natur.399..647P.
- ↑ Fujita K.K. i inni, Discrimination of macaques by macaques: The case of sulawesi species, „Primates”, 3, 38, 1997, s. 233–245, DOI: 10.1007/BF02381612.
- ↑ Call, J.. Object permanence in orangutans (Pongo pygmaeus), chimpanzees (Pan troglodytes), and children (Homo sapiens). „Journal of Comparative Psychology”. 115 (2), s. 159–171, 2001. DOI: 10.1037/0735-7036.115.2.159. PMID: 11459163.
- ↑ Itakura S.S., Tanaka M.M., Use of experimenter-given cues during object-choice tasks by chimpanzees (''Pan troglodytes''), an orangutan (''Pongo pygmaeus''), and human infants (''Homo sapiens''), „Journal of Comparative Psychology”, 2, 112, 1998, s. 119–126, DOI: 10.1037/0735-7036.112.2.119, PMID: 9642782.
- ↑ S. Gouteux, C. Thinus-Blanc, J. Vauclair, Rhesus monkeys use geometric and nongeometric information during a reorientation task, „Journal of Experimental Psychology: General”, 3, 130, 2001, s. 505–519, DOI: 10.1037/0096-3445.130.3.505.
- ↑ Tomasello, M. & Call, J.: Primate Cognition. Oxford University Press US, 1997. ISBN 978-0-19-510624-4.
- ↑ a b c R. O. Deaner, C. P. van Schaik, V. E. Johnson. Do some taxa have better domain-general cognition than others? A metaanalysis of nonhuman primate studies. „Evolutionary Psychology”. 4, s. 149–196, 2006. [dostęp 2011-07-04].
- ↑ a b c S. M. Reader, Y. Hager, K. N. Laland. The evolution of primate general and cultural intelligence. „Philosophical Transactions of the Royal Society B”. 366 (1567), s. 1017–1027, 2011. DOI: 10.1098/rstb.2010.0342. [dostęp 2011-07-04].
- ↑ E.R. Liman, H. Innan, Relaxed selective pressure on an essential component of pheromone transduction in primate evolution, „Proceedings of the National Academy of Sciences of the United States of America”, 100 (6), 2003, s. 3328–3332, DOI: 10.1073/pnas.0636123100, PMID: 12631698, PMCID: PMC152292, Bibcode: 2003PNAS..100.3328L [dostęp 2008-07-23].
- ↑ Nonhuman Primate Communication. W: Egnor, R., Miller, C. & Hauser, M.D.: Encyclopedia of Language and Linguistics. Wyd. 2nd. Elsevier, 2004. ISBN 0-08-044299-4.
- ↑ M.A. Ramsier i inni, Primate communication in the pure ultrasound, „Biology Letters”, 8 (4), 2012, s. 508–511, DOI: 10.1098/rsbl.2011.1149, PMID: 22319094.
- ↑ Opie, Christopher; Atkinson, Quentin D.; Dunbarc, Robin I. M.; Shultz, Susanne. Male infanticide leads to social monogamy in primates. „Proceedings of the National Academy of Sciences”. 110 (33), s. 13328–13332, 2013. DOI: 10.1073/pnas.1307903110.
- ↑ De Ruiter, Jan R.; Van Hooff, Jan A. R. A. M.; Scheffrahn, Wolfgang. Social and genetic aspects of paternity in wild long-tailed macaques (Macaca fascicularis). „Behaviour”. 129 (3–4), s. 203–24, 1994. JSTOR: 4535195.
- ↑ Peter M. Kappeler, Nests, Tree Holes, and the Evolution of Primate Life Histories, „American Journal of Primatology”, 46 (1), 1998, s. 7–33, DOI: 10.1002/(SICI)1098-2345(1998)46:1<7::AID-AJP3>3.0.CO;2-#, PMID: 9730211.
- ↑ Caroline Ross. Park or ride? Evolution of infant carrying in primates.. „Internationaljouurnal of Primatology”. 22 (5), s. 749–771, 1991. Kluwer Academic Publishing. DOI: 10.1023/A:1012065332758.
- ↑ Zoe Mintz: Humans And Primates Burn 50 Percent Fewer Calories Each Day Than Other Mammals. [w:] www.ibtimes.com [on-line]. IBT Media Inc., 2014-01-14. [dostęp 2014-01-14].
- ↑ Walker M. L., Herndon J. G., Menopause in nonhuman primates?, „Biology of Reproduction”, 3, 79, 2008, s. 398–406, DOI: 10.1095/biolreprod.108.068536, PMID: 18495681, PMCID: PMC2553520.
- ↑ K. Milton. Diet and Primate Evolution. „Scientific American”. 269 (2), s. 86–93, 1993. DOI: 10.1038/scientificamerican0893-86. PMID: 8351513.
- ↑ J.I. Pollock, R.J. Mullin, Vitamin C biosynthesis in prosimians: Evidence for the anthropoid affinity of Tarsius, „American Journal of Physical Anthropology”, 1, 73, 1986, s. 65–70, DOI: 10.1002/ajpa.1330730106, PMID: 3113259 [dostęp 2015-06-25] [zarchiwizowane z adresu 2012-06-28].
- ↑ G.W. Milliken, J.P. Ward, C.J. Erickson, Independent digit control in foraging by the aye-aye (''Daubentonia madagascariensis''), „Folia Primatologica”, 4, 56, 1991, s. 219–224, DOI: 10.1159/000156551, PMID: 1937286.
- ↑ C. Hiller: Theropithecus gelada. [w:] Animal Diversity Web [on-line]. 2000. [dostęp 2008-08-08].
- ↑ Introduction. W: Wright, P., Simmons, E. & Gursky, S .: Tarsiers Past, Present and Future. Wright, P., Simmons, E. & Gursky, S. (editors). Rutgers University Press, 2003, s. 1. ISBN 0-8135-3236-1.
- ↑ Ihobe H. Observations on the meat-eating behavior of wild bonobos (Pan paniscus) at Wamba, Republic of Zaire. „Primates”. 33 (2), s. 247–250, 1992. DOI: 10.1007/BF02382754.
- ↑ Rafert, J. & E.O. Vineberg (1997). "Bonobo Nutrition – relation of captive diet to wild diet," Bonobo Husbandry Manual, American Association of Zoos and Aquariums
- ↑ Surbeck M. i inni, Evidence for the consumption of arboreal, diurnal primates by bonobos (''Pan paniscus''), „American Journal of Primatology”, 71 (2), 2008, s. 171–174, DOI: 10.1002/ajp.20634, PMID: 19058132.
- ↑ Surbeck M., Hohmann G., Primate hunting by bonobos at LuiKotale, Salonga National Park, „Current Biology”, 19, 18, 2008, R906–7, DOI: 10.1016/j.cub.2008.08.040, PMID: 18957233.
- ↑ a b Predation. W: Fichtel, Claudia: The Evolution of Primate Societies. Mitani, John C.; Call, Josep; Kappeler, Peter M.; Palombit, Ryne A.; Silk, Joan B (editors). University of Chicago Press, 2012, s. 169–84. ISBN 0-226-53172-4.
- ↑ Tracie McKinney. Anthropogenic change and primate predation risk: crested caracaras (Caracara plancus) attempt predation on mantled howler monkeys (Alouatta palliata). „Neotropical Primates”. 16, s. 24-27, 2009. BioOne. (ang.).
- ↑ a b Tool use, hunting & other discoveries. The Jane Goodall Institute. [dostęp 2013-08-01].
- ↑ Bonobos. ApeTag, 2010. [dostęp 2013-08-03]. [zarchiwizowane z tego adresu (2013-11-02)].
- ↑ Gruber, T., Clay, Z. and Zuberbühler, K.. A comparison of bonobo and chimpanzee tool use: evidence for a female bias in the Pan lineage. „Animal Behaviour”. 80 (6), s. 1023–1033, 2010. DOI: 10.1016/j.anbehav.2010.09.005.
- ↑ Bower, B.: Orangutans use simple tools to catch fish. 2011. [dostęp 2013-08-05].
- ↑ Breuer, T., Ndoundou-Hockemba, M. and Fishlock, V.. First observation of tool use in wild gorillas. „PLoS Biol.”. 3 (11), s. e380, 2005. DOI: 10.1371/journal.pbio.0030380. PMID: 16187795. PMCID: PMC1236726.
- ↑ D. Fragaszy i inni, Wild capuchin monkeys (''Cebus libidinosus'') use anvils and stone pounding tools, „American Journal of Primatology”, 4, 64, 2004, s. 359–366, DOI: 10.1002/ajp.20085, PMID: 15580579.
- ↑ M.D. Gumert, M. Kluck, S. Malaivijitnond. The physical characteristics and usage patterns of stone axe and pounding hammers used by long-tailed macaques in the Andaman Sea region of Thailand. „American Journal of Primatology”. 71 (7), s. 594–608, 2009. DOI: 10.1002/ajp.20694. PMID: 19405083.
- ↑ Hamilton, W.J., Buskirk, R.E. and Buskirk, W.H.. Defensive stoning by baboons. „Nature”. 256 (5517), s. 488–489, 1975. DOI: 10.1038/256488a0.
- ↑ C. Fichtel, P. M. Kappeler: Chapter 19: Human universals and primate symplesiomorphies: Establishing the lemur baseline. W: P. M. Kappeler, J. B. Silk: Mind the Gap: Tracing the Origins of Human Universals. Springer, 2010. ISBN 978-3-642-02724-6.
- ↑ Sumatran orangutans. OrangutanIslands.com. [dostęp 2013-08-02]. [zarchiwizowane z tego adresu (2013-11-26)].
- ↑ van Schaik, C., Fox, E. and Sitompul, A.. Manufacture and use of tools in wild Sumatran orangutans. „Naturwissenschaften”. 83 (4), s. 186–188, 1996. DOI: 10.1007/BF01143062. PMID: 8643126.
- ↑ Victoria Gill: Mandrill monkey makes 'pedicuring' tool. BBC, 2011-07-22. [dostęp 2013-08-11]. [zarchiwizowane z tego adresu (2018-07-15)].
- ↑ Vancatova, M.: Gorillas and Tools – Part I. 2008. [dostęp 2013-08-04]. [zarchiwizowane z tego adresu (2014-02-03)].
- ↑ K. Reed, J. Fleagle, Geographic and climatic control of primate diversity, „Proceedings of the National Academy of Sciences of the United States of America”, 92 (17), 1995, s. 7874–7876, DOI: 10.1073/pnas.92.17.7874, PMID: 7644506, PMCID: PMC41248, Bibcode: 1995PNAS...92.7874R.
- ↑ Primate Seed Dispersal. W: Chapman, C. & Russo, S.: Primates in Perspective. Campbell, C. J., Fuentes, A., MacKinnon, K. C., Panger, M. & Bearder, S. K. (editors). Oxford University Press, 2007, s. 510. ISBN 978-0-19-517133-4.
- ↑ Long, Y. C., Kirkpatrick, R. C., Zhong, T., and Xiao, L.. Report on the distribution, population, and ecology of the Yunnan snub-nosed monkey (Rhinopithecus bieti). „Primates”. 35 (2), s. 241–250, 1994. DOI: 10.1007/BF02382060.
- ↑ Schaller, G. B.: The Mountain Gorilla: Ecology and Behavior. Chicago: University Chicago Press, 1963. ISBN 978-0-226-73635-8.
- ↑ Wolfe, L. D. & Fuentes, A.: Ethnoprimatology. W: Campbell, C. J., Fuentes, A., MacKinnon, K. C., Panger, M. & Bearder, S. K.: Primates in Perspective. Oxford University Press, 2007, s. 692. ISBN 978-0-19-517133-4.
- ↑ Renquist, D. M. & Whitney, R. A.. Zoonoses Acquired from Pet Primates. „Veterinary Clinics of North America. Small Animal Practice”. 17 (1), s. 219–240, 1987. [dostęp 2015-08-30].
- ↑ The Universal Declaration of Human Rights. United Nations, 1948. [dostęp 2008-12-02].
- ↑ a b Cavalieri, P. & Singer, P.: Declaration on Great Apes. Great Ape Project. [dostęp 2008-06-16]. [zarchiwizowane z tego adresu (2008-08-20)].
- ↑ Glendinning, L.: Spanish parliament approves 'human rights' for apes. The Guardian, 2008-06-26. [dostęp 2008-11-10].
- ↑ Singer, P.: Of great apes and men. The Guardian, 2008-07-18. [dostęp 2008-11-10].
- ↑ M. Mott: The Perils of Keeping Monkeys as Pets. National Geographic, 2003-09-16. [dostęp 2013-02-06]. [zarchiwizowane z tego adresu (2013-06-08)].
- ↑ a b Workman, C.. Primate conservation in Vietnam: toward a holistic environmental narrative. „American Anthropologist”. 106 (2), s. 346–352, 2004. DOI: 10.1525/aa.2004.106.2.346.
- ↑ IPPL News: The US Pet Monkey Trade. International Primate Protection League, 2003. [dostęp 2008-08-04].
- ↑ Bushnell, D.: The Beginnings of Research in Space Biology at the Air Force Missile Development Center, 1946–1952. [w:] History of Research in Space Biology and Biodynamics [on-line]. NASA, 1958. [dostęp 2008-08-18].
- ↑ Blumenthal, D.: Monkeys as Helpers To Quadriplegics At Home. [w:] The New York Times [on-line]. 1987-06-17. [dostęp 2008-10-08].
- ↑ Newman, James L.: Encountering Gorillas: A Chronicle of Discovery, Exploitation, Understanding, and Survival. Plymouth, United Kingdom: Rowman and Littlefield, 2013, s. 173. ISBN 978-1-4422-1957-1.
- ↑ a b The supply and use of primates in the EU. European Biomedical Research Association, 1996. [dostęp 2008-08-18]. [zarchiwizowane z tego adresu (2012-01-17)].
- ↑ F.C. Chen, W.H. Li, Genomic divergences between humans and other hominoids and the effective population size of the common ancestor of humans and chimpanzees, „American Journal of Human Genetics”, 2, 68, 2001, s. 444–456, DOI: 10.1086/318206, PMID: 11170892, PMCID: PMC1235277.
- ↑ Conlee, K. M., Hoffeld, E. H. & Stephens, M. L.. A Demographic Analysis of Primate Research in the United States. „ATLA (Alternatives to Laboratory Animals)”. 32 (Sup 1), s. 315–322, 2004. [dostęp 2008-10-08]. [zarchiwizowane z adresu].
- ↑ Presented to Parliament by the Secretary of State for the Home Department by Command of Her Majesty: Statistics of scientific procedures on living animals: Great Britain 2005. The Stationery Office, 2006. ISBN 0-10-168772-9. [dostęp 2008-06-16].
- ↑ Nonhuman Primates: Research Animals. [w:] Animal Welfare Information Center [on-line]. United States Department of Agriculture. [dostęp 2008-07-14]. [zarchiwizowane z tego adresu (2008-10-03)].
- ↑ Directive 86/609. European Coalition to End Animal Experiments. [dostęp 2008-10-08]. [zarchiwizowane z tego adresu (2008-09-29)].
- ↑ IFAW: Born to be wild: Primates are not pets. International Fund for Animal Welfare, 2005. [dostęp 2011-02-26].
- ↑ CITES: Appendices I, II and III. Convention on International Trade in Endangered Species of Wild Fauna and Flora, 2010-10-14. [dostęp 2012-04-02].
- ↑ The Sierra Leone monkey drives. W: Grubb, P.: Mammals of Ghana, Sierra Leone, and the Gambia. St. Ives: Trendrine, 1998, s. 214–219. ISBN 0-9512562-4-6.
- ↑ a b C.A. Chapman, C.A. Peres, Primate conservation in the new millennium: the role of scientists, „Evolutionary Anthropology”, 10, 2001, s. 16–33, DOI: 10.1002/1520-6505(2001)10:1<16::AID-EVAN1010>3.0.CO;2-O.
- ↑ a b Conservation of primates and their habitats. W: Mittermeier, R. A. & Cheney, D. L.: Primate Societies. Smuts, B. B., Cheney, D. L., Seyfarth, R. M., Wrangham, R. W. & Struhsaker, T. T.(editors). Chicago: University of Chicago Press, 1987, s. 477–490.
- ↑ a b Southwick, C. H. & Siddiqi, M. F.. Status, conservation and management of primates in India. „Envis Bulletin: Wildlife and Protected Areas”. 1 (1), s. 81–91, 2001. [dostęp 2008-08-04]. [zarchiwizowane z adresu].
- ↑ a b c d Cowlishaw, G. & Dunbar, R.: Primate Conservation Biology. Chicago: University of Chicago Press, 2000. ISBN 978-0-226-11637-2.
- ↑ C.P. Van Schaik, K.A. Monk, J.M.Y. Robertson, Dramatic decline in orangutan numbers in the Leuser Ecosystem, northern Sumatra, „Oryx”, 35 (1), 2001, s. 14–25, DOI: 10.1046/j.1365-3008.2001.00150.x.
- ↑ A. Purvis i inni, Predicting extinction risk in declining species, „Proceedings of the Royal Society”, 1456, 267, 2000, s. 1947–1952, DOI: 10.1098/rspb.2000.1234, PMID: 11075706, PMCID: PMC1690772.
- ↑ a b c J.E. Fa i inni, Impact of market hunting on mammal species in Equatorial Guinea, „Conservation Biology”, 9 (5), 1995, s. 1107–1115, DOI: 10.1046/j.1523-1739.1995.9051107.x.
- ↑ Hill, C. M.. Crop-raiding by wild vertebrates: The farmer's perspective in an agricultural community in western Uganda. „International Journal of Pest Management”. 43 (1), s. 77–84, 1997. DOI: 10.1080/096708797229022.
- ↑ Hill, C. M.. Primate conservation and local communities: Ethical issues and debates. „American Anthropologist”. 104 (4), s. 1184–1194, 2002. DOI: 10.1525/aa.2002.104.4.1184.
- ↑ Choudhury, A.. Primates in Northeast India: an overview of their distribution and conservation status. „Envis Bulletin: Wildlife and Protected Areas”. 1 (1), s. 92–101, 2001. [dostęp 2008-08-04]. [zarchiwizowane z adresu 2004-11-16].
- ↑ H.N. Kumara, M. Singh, Distribution and abundance of primates in rainforests of the Western Ghats, Karnataka, India and the conservation of ''Macaca silenus'', „International Journal of Primatology”, 25 (5), 2004, s. 1001–1018, DOI: 10.1023/B:IJOP.0000043348.06255.7f.
- ↑ Nijman, V.. Conservation of the Javan gibbon Hylobates moloch: population estimates, local extinction, and conservation priorities. „The Raffles Bulletin of Zoology”. 52 (1), s. 271–280, 2004. [dostęp 2008-08-04].
- ↑ T.G. O'Brien i inni, Abundance and distribution of sympatric gibbons in a threatened Sumatran rain forest, „International Journal of Primatology”, 25 (2), 2004, s. 267–284, DOI: 10.1023/B:IJOP.0000019152.83883.1c.
- ↑ A. Estrada, R. Coates-Estrada, D. Meritt, Non-flying mammals and landscape changes in the tropical forest region of Los Tuxtlas, Mexico, „Ecography”, 17 (3), 1994, s. 229–241, DOI: 10.1111/j.1600-0587.1994.tb00098.x.
- ↑ The nature of fragmentation.. W: Marsh, L. K.: Primates in Fragments: Ecology and Conservation. Marsh, L. K. (editor). New York: Kluwer Academic/Plenum Publishers, 2003, s. 1–10. ISBN 0-306-47696-7.
- ↑ Turner, I. M.. Species loss in fragments of tropical rain forest: a review of the evidence. „Journal of Applied Ecology”. 33 (2), s. 200–209, 1996. DOI: 10.2307/2404743. JSTOR: 2404743.
- ↑ Primates of the Brazilian Atlantic forest: the influence of forest fragmentation on survival. W: Chiarello, A.G.: Primates in Fragments: Ecology and Conservation. Marsh, L. K. (editor). New York: Kluwer Academic/Plenum Publishers, 2003, s. 99–121. ISBN 978-0-306-47696-9.
- ↑ Socioecology, population fragmentation, and patterns of genetic loss in endangered primates. W: Pope, T.R.: Conservation Genetics: Case Histories from Nature. Avise, J. & Hamrick, J. (editors). Norwell: Kluwer Academic Publishers, 1996, s. 119–159. ISBN 978-0-412-05581-2.
- ↑ Russell A. Mittermeier i inni, Primates in Peril: The World's 25 Most Endangered Primates 2008–2010, Arlington, VA.: IUCN/SSC Primate Specialist Group (PSG), International Primatological Society (IPS), and Conservation International (CI), 2009, s. 23–26, ISBN 978-1-934151-34-1.
- ↑ J.F. Oates i inni, Extinction of a West African Red Colobus Monkey, „The Journal of the Society for Conservation Biology”, 14 (5), 2000, s. 1526–1532, DOI: 10.1046/j.1523-1739.2000.99230.x.
- ↑ McGraw, W. S.. Update on the Search for Miss Waldron's Red Colobus Monkey. „International Journal of Primatology”. 26 (3), s. 605–619, 2005. DOI: 10.1007/s10764-005-4368-9.
Bibliografia[edytuj | edytuj kod]
- M. Cartmill: Primate Classification and Diversity. W: M. Platt, A Ghazanfar: Primate Neuroethology. Oxford University Press, 2010, s. 10-30. ISBN 978-0-19-532659-8.
- W. Hartwig: Chapter 3: Primate evolution. W: C. J. Campbell, A. Fuentes, K. C. MacKinnon, S. K. Bearder, R. M Stumpf: Primates in Perspective. Wyd. 2. Oxford University Press, 2011, s. 19–31. ISBN 978-0-19-539043-8.
- F.S. Szalay, E. Delson: Evolutionary History of the Primates. Academic Press, 1980. ISBN 978-0126801507. OCLC 893740473.
