Tytan (pierwiastek)
| skand ← tytan → wanad | |||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | |||||||||||||||||||||||||||||||||||||||||||||||||
| srebrzystobiały | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
Widmo emisyjne tytanu | |||||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||||||||
| Nazwa, symbol, l.a. |
tytan, Ti, 22 | ||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Grupa, okres, blok | |||||||||||||||||||||||||||||||||||||||||||||||||
| Stopień utlenienia |
III, IV | ||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości metaliczne | |||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości tlenków | |||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atomowa |
47,867 ± 0,001[4] | ||||||||||||||||||||||||||||||||||||||||||||||||
| Stan skupienia |
stały | ||||||||||||||||||||||||||||||||||||||||||||||||
| Gęstość |
4507 kg/m³ | ||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura topnienia | |||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura wrzenia |
3287 °C[1] | ||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą warunków normalnych (0 °C, 1013,25 hPa) | |||||||||||||||||||||||||||||||||||||||||||||||||
Tytan (Ti, łac. titanium) – pierwiastek chemiczny z grupy metali przejściowych w układzie okresowym o liczbie atomowej 22.
Lekki metal o szarawym kolorze. Ma wysoką wytrzymałość mechaniczną, jest odporny na korozję (w tym również wody morskiej i chloru). Tytan jest dodawany do żelaza, aluminium, wanadu, molibdenu i innych. Stopy tytanu są wykorzystywane w przemyśle lotniczym (silniki odrzutowe), militarnym, procesach metalurgicznych, motoryzacyjnym, medycznym (protezy dentystyczne, ortopedyczne klamry), sportów ekstremalnych i innych[5]. Został odkryty w Wielkiej Brytanii przez Williama Gregora w 1791 r. Nazwę pochodzącą od bóstw z mitologii greckiej zawdzięcza Martinowi Heinrichowi Klaprothowi.
Występuje w skorupie ziemskiej w ilościach rzędu 0,61%, w postaci minerałów: ilmenitu, rutylu i tytanitu, które są szeroko rozpowszechnione na całej Ziemi[5]. Metaliczny tytan otrzymywany jest przez przerób rud w procesie Krolla[6]. Jego najbardziej rozpowszechniony związek – dwutlenek tytanu znajduje zastosowanie w produkcji białych pigmentów[7]. Inne związki zawierające tytan to czterochlorek tytanu używany do zasłon dymnych oraz jako katalizator i trójchlorek tytanu, który znajduje zastosowanie jako katalizator w produkcji polipropylenu[5].
Dwie najbardziej użyteczne własności tytanu to jego odporność na korozję oraz najwyższy stosunek wytrzymałości mechanicznej do masy[8]. Znane są dwie odmiany alotropowe pierwiastka[9]. Ma pięć trwałych izotopów o masach atomowych od 46 do 50[10]. Właściwości fizykochemiczne tytanu są podobne do cyrkonu.
Historia[edytuj | edytuj kod]
Tytan został odkryty w Kornwalii w Wielkiej Brytanii w 1791 przez pastora i geologa amatora Williama Gregora, który zauważył obecność nieznanego pierwiastka w ilmenicie – czarnym piasku ze strumienia płynącego nieopodal jego parafii. Piasek ten był przyciągany przez magnes. Dokładniejsza jego analiza wykazała obecność dwóch substancji: tlenku żelaza (wyjaśniając przyciąganie magnesem) oraz 45,25% białego tlenku, którego nie mógł zidentyfikować. Gregor, zdając sobie sprawę, że niezidentyfikowany tlenek zawierał metal, który nie pasował do właściwości jakiegokolwiek znanego pierwiastka, poinformował o swoim odkryciu Królewskie Towarzystwo Geologiczne w Kornwalii i niemieckie czasopismo naukowe Annalen Crell[11].

Tlenek tytanu został niezależnie odkryty w 1795 przez niemieckiego chemika Martina Heinricha Klaprotha w rutylu na Węgrzech[12]. Klaproth postanowił nazwać go tytanem, zaczerpując nazwę z mitologii greckiej[11]. Po usłyszeniu o odkryciu Gregora nowej substancji, nabył jej próbki i potwierdził odkrycie tytanu.

Przez wiele lat próbowano otrzymać czysty tytan, jednak zwyczajne sposoby polegające na ogrzewaniu tlenku w obecności węgla nie przynosiły rezultatów, ponieważ tworzył się węglik tytanu zamiast spodziewanej redukcji do metalu. Dopiero w 1910 Matthew A. Hunter otrzymał czysty (99,9%) metaliczny tytan poprzez ogrzewanie TiCl
4 z sodem w bombie stalowej w temperaturze 700–800 °C. Do 1946 tytan nie był używany poza laboratorium, dopóki William Justin Kroll nie opracował opłacalnego sposobu otrzymywania metalicznego tytanu poprzez redukcję czterochlorku tytanu magnezem. Technologia ta została nazwana procesem Krolla. Pomimo badań nad tańszym i wydajniejszym sposobem otrzymywania tytanu, proces Krolla jest do dzisiaj używany do komercyjnego pozyskiwania metalu.
Tytan o bardzo wysokiej czystości został otrzymany przez Anton Eduard van Arkela i Jan Hendrik de Boera w procesie jodkowym w 1925. Rafinację tytanu prowadzi się w próżni w zamkniętym reaktorze. Pary jodu reagują z technicznym tytanem, tworząc czterojodek tytanu, który następnie ulega rozkładowi na ogrzanym oporowo cienkim drucie wolframowym, pogrubiając go w miarę trwania procesu.
W latach 50. i 60. XX w. Związek Sowiecki zapoczątkował wykorzystywanie tytanu do celów militarnych (m.in. w okrętach podwodnych K-278 Komsomolec i projektu 705). We wczesnych latach 50. XX wieku tytan był szeroko stosowany w lotnictwie wojskowym, szczególnie w odrzutowcach o wysokich parametrach silnika zaczynając od F100 Super Sabre i Lockheed A-12. W Stanach Zjednoczonych Departament Obrony zdał sobie sprawę ze strategicznego znaczenia tytanu i rozpoczął magazynowanie tego metalu.
W 2006 Agencja Obrony Stanów Zjednoczonych przyznała 5,7 mln dolarów konsorcjum dwóch spółek, dla opracowania nowego procesu otrzymywania tytanu sproszkowanego[13].
Właściwości[edytuj | edytuj kod]
Fizyczne[edytuj | edytuj kod]
Tytan jest stosunkowo lekkim metalem (gęstość 4507 kg/m³) o dużej wytrzymałości mechanicznej. Przy wysokiej czystości jest ciągliwy (zwłaszcza w atmosferze redukcyjnej)[14]. Charakteryzuje się wysoką temperaturą topnienia: 1668 °C. Jest błyszczący, ma biały, metaliczny kolor.
Handlowy tytan o czystości 99,2% ma wytrzymałość na rozciąganie 434 MPa, porównywalną z rozciągliwością stali, jednak jest lżejszy od niej o 45%. Tytan jest cięższy od aluminium o 60%, ale charakteryzuje się ponad dwukrotnie większą wytrzymałością mechaniczną niż najpopularniejszy stop Al: 6061-T6. Pewne stopy tytanu (np. Beta C) mają wytrzymałość na rozciąganie ponad 1380 MPa (spada ona przy podgrzaniu powyżej temperatury 430 °C)[15].
Ma wysoką twardość (jednak nie tak wysoką jak niektóre hartowane stale), jest trudny w obróbce mechanicznej[11].
Metal ma dwie odmiany alotropowe: Ti-α – krystalizujący w układzie heksagonalnym do temperatury 882 °C; powyżej tej temperatury występuje Ti-β – krystalizujący w układzie regularnym przestrzennie centrowanym. Pojemność cieplna Ti-α gwałtownie wzrasta wraz z podgrzewaniem, po przekroczeniu temperatury 882 °C i przemianie w Ti-β pojemność cieplna kształtuje się na stałym poziomie[16].
Jest paramagnetykiem. Wykazuje stosunkowo niską przewodność elektryczną i cieplną.
Przejawia znaczną promieniotwórczość wzbudzoną po naświetleniu deuteronami. Produktami tej reakcji są pozytony i twarde promieniowanie gamma[6].
Chemiczne[edytuj | edytuj kod]
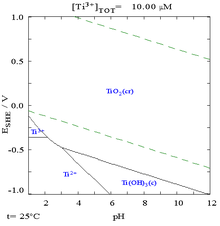
Wykazuje doskonałą odporność na korozję, prawie taką samą jak platyna. Jest także odporny na działanie rozcieńczonych kwasów np. siarkowego, solnego i większości kwasów organicznych, chloru gazowego oraz roztworów zasadowych i morskiej wody[9]. Czysty tytan roztwarzają stężone kwasy. Jest jednym z nielicznych pierwiastków, które gwałtownie reagują z czystym azotem. Reakcja przebiega powyżej temperatury 800 °C z wytworzeniem azotku tytanu.
Wykres Pourbaix dla tytanu ukazuje bardzo wysoką reaktywność termodynamiczną przy niskiej aktywności z wodą i tlenem[17].
Na skutek kontaktu tytanu z tlenem na jego powierzchni tworzy się pasywacyjna warstwa tlenku tytanu o grubości ok. 2 nm (po czterech latach osiąga grubość 25 nm). Warstwa ta dodatkowo zwiększa odporność na korozję[11].
Występowanie[edytuj | edytuj kod]
| Producent | Tysiące ton | % całości |
|---|---|---|
| Australia | 1291,0 | 30,6 |
| Republika Południowej Afryki | 850,0 | 20,1 |
| Kanada | 767,0 | 18,2 |
| Norwegia | 382,9 | 9,1 |
| Ukraina | 357,0 | 8,5 |
| Pozostałe państwa | 573,1 | 13,6 |
| Cały świat | 4221,0 | 100 |
Z powodu zaokrągleń suma nie wynosi dokładnie 100%
Tytan zawsze występuje w rudach innych pierwiastków. Jest dziewiąty pod względem występowania na Ziemi (0,63%), siódmy spośród metali[16]. Na 801 skał przebadanych przez United States Geological Survey, tytan zawarty był w 784[16]. Jego udział w ziemiach wynosi w przybliżeniu 0,5–1,5%[16].
Jest szeroko rozpowszechniony, występuje głównie pod postacią minerałów: anatazytu, brukitu, ilmenitu, perowskitu, rutylu, tytanitu (sfen) oraz w wielu rudach żelaza. Z powyższych minerałów tylko ilmenit i rutyl mają znaczenie ekonomiczne (pod warunkiem eksploatacji rudy o odpowiednio wysokiej zawartości tytanu). Znaczące złoża tytanu (ilmenitu) znajdują się w zachodniej Australii, Kanadzie, Nowej Zelandii, Norwegii i Ukrainie. Duże ilości rutylu są eksploatowane w Ameryce Północnej i Republice Południowej Afryki. Roczna produkcja wynosi 90 000 ton metalu i 4,3 milionów ton dwutlenku tytanu. Całkowite zasoby tytanu na Ziemi szacuje się na ponad 600 milionów ton[11].
Tytan jest zawarty w meteorytach, jego obecność zauważono na Słońcu i gwiazdach typu M (najchłodniejszy typ gwiazd o temperaturze powierzchni około 3200 °C). Skały dostarczone przez Apollo 17 z Księżyca zawierają 12,1% tytanu[6].
Produkcja[edytuj | edytuj kod]

Otrzymywanie metalicznego tytanu zachodzi w pięciu głównych etapach[18]:
- przeróbka rud tytanu;
- otrzymywanie czterochlorku tytanu TiCl
4; - proces Krolla – redukcja TiCl
4 magnezem; - oczyszczanie tytanu – proces jodkowy;
- topienie tytanu.
Ponieważ tytan reaguje z tlenem przy wysokich temperaturach (610 °C), nie może być otrzymywany przez redukcję bieli tytanowej. Dlatego do celów handlowych stosuje się kosztowny proces Krolla (stosunkowo wysoka wartość rynkowa tytanu jest spowodowana głównie zastosowaniem w tym procesie innego drogiego metalu – magnezu)[16]. Przemysłowa produkcja czterochlorku tytanu polega na chlorowaniu przy jednoczesnej redukcji zbrykietowanego z węglem surowca tytanowego (rutylu lub ilmenitu) w szybowym piecu elektrycznym.
Reakcje zachodzące podczas procesu Krolla:
Techniczny tytan otrzymany w procesie Krolla powinien być rafinowany. Zasada procesu pozwalającego na otrzymanie czystego tytanu polega na rozkładzie termicznym czterojodku tytanu.
- TiI
4 → Ti + 2I
2
- TiI
W wysokich temperaturach (około 1400 °C) i przy określonym ciśnieniu reakcja ta przebiega w kierunku dysocjacji czterojodku tytanu, natomiast niskie temperatury sprzyjają jego tworzeniu. Zaletą tego procesu jest otrzymanie czystego tytanu niezawierającego domieszek (tlen, azot, węgiel) obniżających jego własności mechaniczne.
Proces topienia tytanu stanowi poważny problem. Trudności sprawiają wysoka temperatura topienia (1668 °C) i duża aktywność chemiczna w tej temperaturze. Ponadto stopiony tytan reaguje niemal ze wszystkimi materiałami ogniotrwałymi. Jedynie dwutlenek toru, rekrystalizowany tlenek wapnia i grafit są odporne na jego działanie. Topienie tytanu odbywa się w piecach łukowych, indukcyjnych, plazmowych oraz elektronowych. Te ostatnie wydają się najbardziej perspektywiczne[potrzebny przypis].
Związki chemiczne tytanu[edytuj | edytuj kod]
Tytan w związkach chemicznych występuje najczęściej na IV stopniu utlenienia, rzadziej na stopniu III[19].

Dwutlenek tytanu (TiO
2) jest najpopularniejszym związkiem tytanu. Znajduje on szerokie zastosowanie:
- przemysł metalurgiczny – do produkcji elektrod, stopów, radioelementów ceramicznych;
- przemysł barw i lakierów – bardzo dobra intensywność kolorów[7];
- przemysł papierniczy – wysoka jakość białego papieru;
- przemysł włókien szklanych – zastosowanie dzięki nietoksyczności, małej reaktywności chemicznej;
- przemysł wyrobów gumowych – do produkcji naturalnego i sztucznego kauczuku;
- przemysł spożywczy – barwnik, oznaczony jako E171[20].
Azotek tytanu (TiN) nanosi się na narzędzia tnące, formujące i ślizgowe. Warstwa TiN o grubości od 0,5 do kilku mikrometrów daje wzrost twardości powierzchniowej do 2400 HV. Czas pracy narzędzi ulega znacznemu wydłużeniu (do kilkunastu razy). Powłoki z TiN są natryskiwane plazmowo na elementy robocze łopatek turbin, silników i narzędzi skrawających.
Czterochlorek tytanu (TiCl
4) jest bezbarwną cieczą, używaną w procesie produkcji dwutlenku tytanu do farb lub redukowany magnezem bezpośrednio do tytanu. Tytan tworzy również trójchlorek tytanu TiCl
3, który jest używany jak czynnik redukcyjny.
Węglik tytanu (TiC) ma szereg niepospolitych właściwości, tj. wysoką twardość (ok. 90 HRC), niski współczynnik tarcia, wysoką temperaturę topienia, dobrą odporność korozyjną i cieplną (zachowuje własności skrawalne do ok. 1000 °C). Stosowany jest w przemyśle narzędziowym, kosmicznym i energetyce atomowej. Węglik tytanu znalazł też zastosowanie w kompozytach diamentowo-węglikowych przeznaczonych na ostrza skrawające.
Tytaniany cechuje wysoka przenikalność elektryczna. Tytanian wapnia (CaTiO
3) i tytanian magnezu (MgTiO
3) znalazły zastosowanie w ceramice kondensatorowej. Tytanian baru (BaTiO
3) ma właściwości piezoelektryczne i ferroelektryczne. Stosowany jest w urządzeniach ultradźwiękowych, mikrofonach i urządzeniach do zapalania gazu w kuchenkach. Tytanian strontu (SrTiO
3) stosowany jest do produkcji szkła o dużym współczynniku załamania światła: do wyrobu soczewek, pryzmatów i biżuterii. Tytanian sodu (Na
2TiO
3) wchodzi w skład mas do pokrywania prętów spawalniczych[7].
Izotopy[edytuj | edytuj kod]
Występujący w przyrodzie tytan ma pięć stabilnych izotopów: 46
Ti, 47
Ti, 48
Ti, 49
Ti oraz 50
Ti, przy czym 48
Ti stanowi 73,8% składu izotopowego. Jedenaście znanych izotopów charakteryzuje promieniotwórczość. Najbardziej stabilnym z radioaktywnych izotopów jest 44
Ti o okresie połowicznego rozpadu wynoszącym 63 lata, 45
Ti o czasie rozpadu 184,8 minut, 51
Ti – 5,76 minut, oraz 52
Ti – 1,7 minuty. Czas połowicznego rozpadu pozostałych izotopów jest krótszy niż 33 sekundy, a dla większości krótszy niż 0,5 sekundy. Izotopy tytanu mają masę atomową od 39,99 (40
Ti) do 57,966 u (58
Ti)[10].
Znaczenie biologiczne[edytuj | edytuj kod]

Tytan jest nietoksyczny nawet w dużych dawkach i nie ma żadnego wpływu na organizm ludzki. Dwutlenek tytanu, który jest często stosowany w przemyśle żywnościowym, kosmetycznym i farmaceutycznym, jest toksyczny, szczególnie gdy występuje w postaci nanocząstek[21]. Szacuje się, że każdego dnia człowiek spożywa 0,8 mg tytanu, ale większość nie jest przyswajana przez organizm. Ma tendencję do akumulacji w tkankach zawierających krzemionkę. Większość roślin zawiera około 1 ppm tytanu, natomiast skrzyp i pokrzywa może zawierać nawet do 80 ppm[11].
Tytan pod postacią proszku lub wiórów może ulec zapaleniu, a rozpylony w powietrzu grozi wybuchem. Woda i dwutlenek węgla są nieefektywne w gaszeniu tytanu; jedynie skuteczne w takim przypadku są suche materiały przeciwpożarowe (klasa D materiałów przeciwpożarowych)[7].
Tytan może zapalić się, kiedy świeża, nieutleniona powierzchnia pozostanie w kontakcie z ciekłym tlenem. Do zapalenia może dojść przy uderzeniu twardym przedmiotem lub przy odkształceniu mechanicznym po powstaniu pęknięcia. Takie zachowanie tytanu powoduje ograniczenie dla jego stosowania z ciekłym tlenem (np. w przemyśle lotniczym i kosmonautycznym).
Większość soli tytanu jest nieszkodliwa, ale jego związki z chlorem, takie jak: TiCl
2, TiCl
3 i TiCl
4 są niebezpieczne. Dwuchlorek pod postacią czarnych kryształów ulega samozapaleniu, natomiast czterochlorek jest lotnym, dymiącym płynem. Wszystkie chlorki tytanu są żrące.
Zastosowanie tytanu[edytuj | edytuj kod]
Pigmenty i powłoki[edytuj | edytuj kod]

Około 95% wydobytych rud tytanowych jest przeznaczonych na otrzymywanie dwutlenku tytanu TiO
2. Z racji jego intensywnej bieli najczęściej stosuje się go jako pigment w farbach, papierze, paście do zębów oraz chirurgii plastycznej[22]. Używany również jako dodatek do cementu, w kamieniach szlachetnych[23] oraz jako dodatek wzmacniający kompozyty grafitowe stosowane do wędek oraz kijów golfowych.
Proszek TiO
2 jest chemicznie obojętny, nieprzezroczysty. W stanie wolnym występuje pod postacią minerałów: anatazu, brukitu i rutylu[14]. Farba wytworzona z dwutlenku tytanu jest odporna na niskie temperatury oraz na działanie środowiska morskiego[7]. Czysty dwutlenek tytanu ma bardzo wysoki wskaźnik załamywania światła i rozszczepia światło silniej niż diament[6].
Jest wykorzystywany jako filtr oczyszczający powietrze, stosowany również jako błona naniesiona na okna chroniąca przed działaniem promieni UV[24].
Stopy z dodatkiem tytanu[edytuj | edytuj kod]
Stale mikrostopowe o podwyższonej wytrzymałości[edytuj | edytuj kod]

Są to stale o zmniejszonej zawartości węgla, a także obniżonym poziomem zanieczyszczeń (siarka, fosfor), o podwyższonej zawartości manganu, w których przez dodawanie niewielkich ilości dodatków stopowych, takich jak: tytan, niob i wanad, uzyskuje się znaczny wzrost wytrzymałości. Działanie tytanu związane jest z tworzeniem z azotem i węglem bardzo stabilnych węglików i azotków. Jego dodatek do stali w ilości 0,01–0,02% powoduje wydzielenie podczas walcowania na granicach ziaren austenitu przede wszystkim azotku tytanu, który nie pozwala na rozrost ziaren austenitu nawet w temperaturze 1200 °C. Tytan również wpływa pozytywnie na spawalność blach.
Stale zawierające oprócz niobu dodatek tytanu w ilości około 0,015% o wytrzymałości blisko 500 MPa stosowane są na rurociągi pracujące w warunkach arktycznych (obniżenie progu kruchości w niskich temperaturach).
Stale maraging [SM][edytuj | edytuj kod]
Stale maraging zawierają 20–25% Ni z dodatkami 1,3–1,6% Ti, 0,15–0,30% Al, 0,3–0,5% Nb. Tytan w tych stopach stanowi składnik umacniający, dzięki tworzeniu w czasie starzenia licznych dyspersyjnych wydzieleń (Ni
3Ti, NiTi i inne). Stale SM stosuje się w budowie statków kosmicznych, w lotnictwie (produkcja foteli wyrzucanych, podwozi samolotów, konstrukcja samolotu myśliwskiego Mirage F1), w przemyśle zbrojeniowym (lufy dział szybkostrzelnych, lufy broni palnej), budowie maszyn i urządzeń (elementy turbin parowych), korbowody (Ferrari F355/360M/550M, Porsche 911 GT3, Honda NSX), wały napędowe samochodów wyścigowych, elementy wagonów kolejowych, cienkościenne naczynia ciśnieniowe o średnicy do 4 m oraz kotły i rury o dużych średnicach pracujące w podwyższonych temperaturach i pod ciśnieniem do 2 GPa[25][26].
Jedną z najistotniejszych własności tytanu jest odporność na działanie wody morskiej. Wykorzystane to zostało do budowy rurociągów transportujących wodę używaną do chłodzenia rafinerii i zakładów chemicznych pracujących w pobliżu morza. W końcu lat 90. XX wieku na świecie zainstalowanych było blisko 100 milionów metrów bieżących rurociągów wykonanych z tytanu[27].
Tytan stosuje się też do produkcji pomp wody morskiej, śrub okrętowych i zaworów, a dzięki swym paramagnetycznym właściwościom do budowy niemagnetycznych statków badawczych, używanych do pomiarów geofizycznych.
Stopy tytanu ze względu na swą odporność na korozję, jak i możliwość przenoszenia dużych ciśnień (praca na głębokości do 3700 m), uważane są za najbardziej perspektywiczny materiał na kadłuby okrętów podwodnych i batyskafów[28][26].
Blacha cynkowo-tytanowa[edytuj | edytuj kod]
Blachy cynkowo-tytanowe wykonuje się z cynku o wysokiej czystości, z dodatkiem tytanu (0,06–0,2%) i miedzi (0,08–1,0%), przy czym zawartość glinu nie powinna przekraczać 0,015% (wg normy PN-EN 988). Dzięki pasywacji jest odporna na korozję, ma dobre właściwości mechaniczne i daje się łatwo formować. Stosowana jest do wykonywania pokryć dachowych, obróbek blacharskich, do wykonywania systemów odprowadzania wody oraz innych elementów zewnętrznych budynków[29].
Architektura i zastosowania konsumenckie[edytuj | edytuj kod]

Tytan znajduje zastosowanie w przemyśle motoryzacyjnym, a w szczególności w branży samochodów sportowych i motocykli, gdzie przywiązuje się dużą wagę do redukcji masy pojazdu przy utrzymaniu wysokiej wytrzymałości mechanicznej. Tytan jest jeszcze zbyt drogim metalem, aby był używany w najpopularniejszych samochodach (o niewygórowanej cenie). Przykładem zastosowania elementów tytanowych są rury wydechowe w późnych wersjach w Chevrolet Corvette, tłumiki w motocyklach sportowych i inne[30].
Parker Pen Company (firma produkująca długopisy i pióra) wypuściła w 1970 serię T-1 wiecznych piór z tytanu, a rok później na rynku pokazały się tytanowe pióra kulkowe. Produkcji zaprzestano w 1972 z powodu zbyt dużej ceny tytanu. Obecnie pióra z serii T-1 są bardzo cenione i zbierane przez kolekcjonerów.
Od 1999 dostępne są młotki z obuchem tytanowym. Ich mała waga umożliwia zastosowanie dłuższego trzonka, dzięki czemu wbijanie gwoździ staje się szybsze i skuteczniejsze oraz mniej męczące. Tytan niweluje wstrząsy przenoszone z narzędzia na wbijającego; generuje zaledwie 3% odskok obucha, podczas gdy stalowy młotek generował aż 29%.
Tytan i jego stopy wykorzystywane są do produkcji sprzętu sportowego. Stosuje się je wszędzie tam, gdzie konieczne jest uzyskanie dużej wytrzymałości przy minimalnej masie wyrobu. Najpopularniejsze wyroby tytanowe to: sprzęt alpinistyczny[31], ramy rowerowe (doskonale tłumiące drgania, sprężyste i odporne na zmęczenie), rakiety tenisowe, wyczynowe sanki, narty, kije golfowe, kije hokejowe, kije do krykieta, osłony hełmów do rugby czy sprzęt wędkarski. Stopy tytanu można znaleźć w oprawkach okularów (lekkie, wytrzymałe i niepowodujące alergii skórnej, ale o wysokiej cenie) czy w podkowach głównie dla koni wyścigowych oraz sporadycznie zaprzęgowych. Stopy tytanu stosuje się do produkcji osprzętu w żeglarstwie (okucia, bloki, elementy kabestanów, olinowanie stałe).
Tytan bywa stosowany w rozwiązaniach architektonicznych. Przykładem mogą być Muzeum Guggenheima w Bilbao i Cerritos Millennium Library (pierwsze budynki w Ameryce Północnej i Europie pokryte panelami tytanowymi)[32].
Tytan wykorzystywany jest przez artystów do tworzenia rzeźb (czterdziestometrowy pomnik Jurija Gagarina w Moskwie)[33], detali dekoracyjnych oraz w elementach mebli.
Tytan znajduje zastosowanie w produkcji broni palnej, gdzie zastępuje stal i stopy aluminium (np. bęben rewolweru).
Inżynieria biomedyczna[edytuj | edytuj kod]
Właściwości biologiczne i fizykochemiczne tytanu spowodowały znaczący przełom w biomedycynie. Tytan stosowany jest w protetyce dentystycznej. Ma kilkakrotnie niższe niż tradycyjne materiały protetyczne przewodnictwo cieplne, dużą twardość, wytrzymałość mechaniczną oraz trwałość. Poza tym bardzo rzadko wywołuje reakcje alergiczne i jest odporny na korozję[11]. Do leczenia złamań kości stosuje się stopy tytanu z Al, Nb i Ta oraz tytanu z Al i Nb. Na przykład tzw. klamry Blounta, których żywotność wynosi około 20 lat, wykonane są ze stopu tytanu (43–47%) z niklem (53–57%) charakteryzującego się pamięcią kształtu. Innym zastosowaniem stopów Ni-Ti są płytki implantacyjne oraz urządzenia do leczenia zgryzu u dzieci[11]. Tytan wykorzystywany jest również w produkcji narzędzi chirurgicznych, wózków inwalidzkich oraz kul.
Ponieważ tytan nie jest ferromagnetykiem, pacjenci z implantami tytanowymi mogą być bezpiecznie badani tomografem MRI (obrazowanie rezonansu magnetycznego). Przygotowując tytan do wszczepienia, oczyszcza się go w strumieniu plazmy, po skończonym procesie ulega natychmiastowemu utlenieniu[11].
Metal ten zyskuje coraz większą popularność w piercingu jako materiał na (kolczyki, ćwieki itp.)[34], a jego kolor można odpowiednio zmieniać poprzez anodowanie[35].
Lotnictwo[edytuj | edytuj kod]

Stopy tytanu stanowią perspektywiczny materiał dla samolotów przyszłości. Z uwagi na największy współczynnik wytrzymałości do ciężaru właściwego[9], wysoką odporność na korozję[6] i wysoką temperaturę topnienia wykorzystywane są w przemyśle lotniczym, morskim, kosmicznym oraz w pociskach[7][6]. 2/3 produkowanego tytanu zużywane jest, jako stop z aluminium, wanadem i innymi dodatkami, w silnikach lotniczych i pokryciach samolotów[11]. Stopy tytanu używane są do produkcji większości elementów głowic wirników w helikopterach.
SR-71 „Blackbird” był jednym z pierwszych samolotów wykonanym w dużym stopniu ze stopów tytanu, torując jednocześnie drogę do zastosowań tytanu w samolotach pasażerskich. Szacuje się, że w Boeingu 777 znajduje się 58 ton tytanu, 43 ton w 747, 18 ton w 737, 24 ton w Airbusie A340, 17 ton w A330 i 12 ton w A320. A380 zawiera 77 ton tytanu, w tym około 11 ton w silnikach[36]. W konstrukcji Ił-86 jest ponad 20 ton stopów tytanu[36].
W naddźwiękowym samolocie Tupolew Tu-144 użyto kilka tysięcy części z tytanu i jego stopów. Tytan stosowany był do budowy silnika Concorde. Zastąpienie stopów aluminium stopami tytanu umożliwia zmniejszenie całkowitej masy samolotu o 20–25%. Stop 6AL-4V znalazł się w około połowie wszystkich zastosowań tytanu związanych z przemysłem lotniczym[37].
Biżuteria[edytuj | edytuj kod]
Ze względu na odporność chemiczną bywa używany w jubilerstwie, choć wcześniej był uznawany za metal zbyt trudny do obróbki i kształtowania skomplikowanych i precyzyjnych wzorów. Jednym z najszybciej rosnących segmentów rynku jubilerskiego są obrączki ślubne i zaręczynowe wykonane z tytanu oraz koperty i bransolety zegarków ręcznych. Wyroby tytanowe nie wywołują reakcji alergicznej oraz nie ciemnieją w środowiskach wodnych (np. basenach).
Przypisy[edytuj | edytuj kod]
- ↑ a b David R. Lide (red.), CRC Handbook of Chemistry and Physics, wyd. 90, Boca Raton: CRC Press, 2009, s. 4-38, ISBN 978-1-4200-9084-0 (ang.).
- ↑ Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4.
- ↑ Titanium (nr 305812) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2011-10-04]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Thomas Prohaska i inni, Standard atomic weights of the elements 2021 (IUPAC Technical Report), „Pure and Applied Chemistry”, 94 (5), 2021, s. 573–600, DOI: 10.1515/pac-2019-0603 (ang.).
- ↑ a b c Encyclopædia Britannica Concise: Titanium. 2007.
- ↑ a b c d e f Titanium [online], Los Alamos National Laboratory [zarchiwizowane z adresu 2006-12-30].
- ↑ a b c d e f Robert E. Krebs: The History and Use of Our Earth’s Chemical Elements: A Reference Guide. Wyd. 2. Westport, CT: Greenwood Press, 2006. ISBN 0-313-33438-2.
- ↑ Matthew J. Donachie, Jr.: Titanium. A Technical Guide. Metals Park, OH: ASM International, 1988, s. 11. ISBN 0-87170-309-2.
- ↑ a b c Titanium, [w:] Columbia Encyclopedia, New York: Columbia University Press, 2000–2006, ISBN 0-7876-5015-3.
- ↑ a b Barbalace, Kenneth L: Periodic Table of Elements: Ti – Titanium. 2006. [zarchiwizowane z tego adresu (2012-07-14)].
- ↑ a b c d e f g h i j John Emsley: Nature’s Building Blocks: An A-Z Guide to the Elements. Oxford: Oxford University Press, 2001, s. 451–455. ISBN 0-19-850341-5.
- ↑ Origins of the Element Names: Names Derived from Mythology or Superstition. homepage.mac.com. [zarchiwizowane z tego adresu (2002-01-21)]..
- ↑ DuPont, U.S. Defense Agency Awards $5.7 Million to DuPont and MER Corporation for New Titanium Metal Powder Process [online], 9 grudnia 2006.
- ↑ a b titanium, [w:] Encyclopædia Britannica [dostęp 2006-12-29] (ang.).
- ↑ Appendix J, Table J.2. W: Matthew J. Donachie, Jr.: Titanium. A Technical Guide. Metals Park, OH: ASM International, 1988. ISBN 0-87170-309-2.
- ↑ a b c d e Barksdale, Jelks: The Encyclopedia of the Chemical Elements. Skokie, Illinois: Reinhold Book Corporation, 1968, s. 732–738 „Titanium”. LCCCN 68-29938.
- ↑ Ignasi Puigdomenech, Hydra/Medusa Chemical Equilibrium Daabase and Plotting Software (2004) KTH Royal Institute of Technology, freely downloadable software at www.kth.set.
- ↑ Rozdział 4. W: Matthew J. Donachie, Jr.: Titanium. A Technical Guide. Metals Park, OH: ASM International, 1988. ISBN 0-87170-309-2.
- ↑ N.N. Greenwood, A. Earnshaw: Chemistry of the elements. Oxford; New York: Pergamon Press, 1984, s. 958, 970. ISBN 0-08-022057-6.
- ↑ E 171. www.pfpz.pl. [dostęp 2010-12-27]. (pol.).
- ↑ Matej Skocaj i inni, Titanium dioxide in our everyday life; is it safe?, „Radiology and Oncology”, 45 (4), 2011, s. 227–247, DOI: 10.2478/v10019-011-0037-0, PMID: 22933961, PMCID: PMC3423755.
- ↑ United States Geological Survey: USGS Minerals Information: Titanium. 2006-12-21. [dostęp 2006-12-29].
- ↑ Gary A. Smook: Handbook for Pulp & Paper Technologists (3rd edition). Angus Wilde Publications, 2002, s. 223. ISBN 0-9694628-5-9.
- ↑ Lisa Stevens i inni, Photocatalytic Oxidation of Organic Pollutants Associated with Indoor Air Quality [online], 1998 [zarchiwizowane z adresu 2010-03-18].
- ↑ Ciszewski i Przetakiewicz 1993 ↓.
- ↑ a b Froes 1987 ↓.
- ↑ Kane R.L.: Titanium in Seawater Piping. JOM, 1987.
- ↑ Okrętowe turbozespoły spalinowe. Materiały stosowane w konstrukcjach OTZS. [dostęp 2007-11-28]. [zarchiwizowane z tego adresu (2007-06-11)].
- ↑ Blacha cynkowo-tytanowa. Podręcznik stosowania, ZM „Silesia” SA, s. 3–5 [dostęp 2021-02-24].
- ↑ Titanium Exhausts [online], National Corvette Museum [zarchiwizowane z adresu 2009-02-13].
- ↑ Karabinki wspinaczkowe [online], www.karabinki.wspinaczkowe.com.pl [zarchiwizowane z adresu 2014-01-09].
- ↑ Denver Art Museum, Frederic C. Hamilton Building. SPG Media, 2006. [dostęp 2006-12-26].
- ↑ Yuri Gagarin [online], Microsoft Encarta, 2006.
- ↑ Janet Yagoda Shagam, Body Piercing Safety [online], hospitals.unm.edu.
- ↑ Robert S. Alwitt, Anodizing, [w:] Electrochemistry Encyclopedia [online], 2002 [zarchiwizowane z adresu 2013-10-14] (ang.).
- ↑ a b Vardan Sevan, Rosoboronexport controls titanium in Russia [online], Sevanco Strategic Consulting, 23 września 2006 [zarchiwizowane z adresu 2012-11-11].
- ↑ Matthew J. Donachie, Jr.: Titanium. A Technical Guide. Metals Park, OH: ASM International, 1988, s. 13. ISBN 0-87170-309-2.
Bibliografia[edytuj | edytuj kod]
- J. Kaczyński, Tytan, Warszawa: Wydawnictwo Naukowo Techniczne, 1961.
- Bylica A., Sieniawski J., Tytan i jego stopy, PWN, 1985.
- Bohdan Ciszewski, Wojciech Przetakiewicz, Nowoczesne materiały w technice, Bellona, 1993, ISBN 978-83-11-08236-6.
- F.H. Froes, Titanium Products and Applications, „JOM”, 39 (3), 1987, s. 12–14, DOI: 10.1007/bf03258872.
- L.A. Dobrzański, Podstawy nauki o materiałach i metaloznawstwie, Warszawa: Wydawnictwo Naukowo Techniczne, 2002, ISBN 83-20427-93-2.
- L.A. Dobrzański, Metalowe materiały inżynierskie, Warszawa: Wydawnictwo Naukowo Techniczne, 2004, ISBN 83-204-3045-3.
| Układ okresowy pierwiastków | ||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3[i] | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||||
| 8 | Uue | Ubn | ✱ | |||||||||||||||||||||||||||||||||||||||||
| ✱ | Ubu | Ubb | Ubt | Ubq | Ubp | Ubh | Ubs | ...[ii] | ||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||


